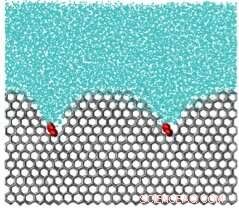
Une simulation d'une molécule inhibant la glace. La molécule, en rouge, est comme un poids à la surface du cristal de glace, le courbant et empêchant la croissance de cristaux de glace. Crédit :Université de l'Utah
Les thérapies cellulaires sont très prometteuses pour révolutionner le traitement des cancers et des maladies auto-immunes. Mais cette industrie de plusieurs milliards de dollars nécessite un stockage à long terme des cellules dans des conditions cryogéniques ultra-froides, tout en s'assurant qu'ils continueront à fonctionner après décongélation. Cependant, ces températures froides déclenchent la formation et la croissance de la glace, qui peut percer et déchirer les cellules. Recherche publiée dans le Journal de l'American Chemical Society par les chimistes de l'Université de l'Utah, Pavithra Naullage et Valeria Molinero, jette les bases de la conception de polymères efficaces qui peuvent empêcher la formation de glace qui endommage les cellules.
L'antigel de la nature
Les stratégies actuelles de cryoconservation des cellules et des organes consistent à les baigner avec de grandes quantités de diméthylsulfoxyde, un produit chimique toxique qui gâche la formation de glace mais stresse les cellules, diminuant leurs chances de survie.
La nature, cependant, a trouvé un moyen de maintenir les organismes en vie dans des conditions de froid extrême :les protéines antigel. Poisson, les insectes et autres organismes à sang froid ont développé de puissantes glycoprotéines antigel qui se lient aux cristallites de glace et les empêchent de croître et d'endommager les cellules.
Le domaine croissant des thérapies cellulaires exige le développement d'inhibiteurs puissants de la recristallisation de la glace qui peuvent rivaliser en activité avec les glycoprotéines antigel naturelles mais n'ont pas le coût et la toxicité du diméthylsulfoxyde. Cette demande a propulsé la synthèse de polymères qui imitent l'action des glycoprotéines antigel. Mais l'inhibiteur synthétique de recristallisation de la glace le plus puissant trouvé à ce jour, alcool polyvinylique (PVA), est de plusieurs ordres de grandeur moins puissant que les glycoprotéines naturelles.
« Les efforts visant à identifier des inhibiteurs plus puissants de la croissance de la glace semblent être au point mort, comme il n'y a pas encore de compréhension moléculaire des facteurs qui limitent l'efficacité d'inhibition de la recristallisation de la glace des polymères, " dit Molinero.
Une variable de conception polymère cachée
Comment les molécules empêchent-elles les cristaux de glace de grossir ? Les molécules qui se lient fortement à la glace épinglent sa surface, comme des pierres sur un oreiller, ce qui fait que le front de glace développe une surface incurvée autour des molécules. Cette courbure déstabilise le cristal de glace, stopper sa croissance. Les molécules qui restent liées à la glace plus longtemps que le temps nécessaire à la croissance des cristaux de glace réussissent à empêcher une croissance et une recristallisation supplémentaires.
Molinero et Naullage ont utilisé des simulations moléculaires à grande échelle pour élucider les fondements moléculaires de la façon dont la flexibilité, la longueur et la fonctionnalisation des polymères contrôlent leur liaison à la glace et leur efficacité pour empêcher la croissance de la glace. Leur étude montre que le temps de liaison des molécules à la surface de la glace est contrôlé par la force de leur liaison à la glace couplée à la longueur du polymère et à la vitesse à laquelle elles se propagent à la surface de la glace.
"Nous avons constaté que l'efficacité des polymères flexibles pour arrêter la croissance de la glace est limitée par la lente propagation de leur liaison à la glace, " dit Molinero.
L'étude dissèque les divers facteurs qui contrôlent la liaison des polymères flexibles à la glace et qui expliquent l'écart de puissance du PVA et des glycoprotéines antigel naturelles. En un mot, chaque bloc de glycoprotéines antigel se lie plus fortement à la glace que le PVA, et sont également favorisés par leur structure moléculaire secondaire qui sépare les blocs liants et non liants pour leur permettre de se fixer plus rapidement à la glace pour arrêter sa croissance.
"A notre connaissance, ce travail consiste d'abord à identifier le temps de propagation de la liaison comme variable clé dans la conception de polymères flexibles efficaces pour la liaison à la glace, ", dit Naullage. "Notre étude ouvre la voie à la conception de novo de polymères flexibles qui peuvent atteindre ou même surpasser l'efficacité des glycoprotéines antigel et avoir un impact dans la recherche biomédicale."