
Hydrate de méthane récupéré du fond de l'océan au large des côtes de l'Oregon, ETATS-UNIS. Crédit :Wikimedia Commons
Dans un article publié cette semaine dans PNAS , des chercheurs de l'Institut Van 't Hoff des sciences moléculaires de l'Université d'Amsterdam et du Centre de modélisation multi-échelle d'Amsterdam fournissent un aperçu atomistique de la formation des hydrates de méthane. Sur la base de simulations de dynamique moléculaire, ils expliquent comment se produit la sélection entre les polymorphes d'hydrates de méthane concurrents, et comment cela pourrait être généralisé à d'autres hydrates et à la formation de cristaux moléculaires.
Les hydrates de méthane sont des substances solides semblables à de la glace qui sont présentes en abondance, entre autres au fond des océans. On estime que la quantité d'énergie stockée dans les hydrates de méthane est le double de la quantité d'énergie stockée dans les ressources conventionnelles de combustibles fossiles. À la fois, la formation d'hydrates est préoccupante pour l'industrie pétrolière car ils peuvent obstruer les oléoducs, provoquant des problèmes de débit. Des hydrates de méthane sont également présents dans le pergélisol des régions arctiques. Le dégel du pergélisol en raison de l'augmentation des températures mondiales peut entraîner la libération de grandes quantités de méthane, qui est un puissant gaz à effet de serre.
Molécules de méthane encagées
Dans un hydrate de méthane, au niveau moléculaire, le méthane est enfermé dans un réseau d'eau lié à l'hydrogène. Alors que le gaz méthane est hydrophobe dans les conditions ambiantes, à basse température et à haute pression, un mélange d'eau et de méthane gazeux peut se former spontanément en hydrates.
Au cours des années, l'intérêt pour la compréhension du mécanisme de formation des hydrates s'est considérablement accru. En particulier, leur formation dans des conditions naturelles est mal connue. Comprendre le processus de nucléation homogène, et comment cela conduit à différents polymorphes d'hydrate de méthane, peut conduire à un meilleur contrôle de la cristallisation, ainsi qu'un aperçu de la sélection polymorphe en général.
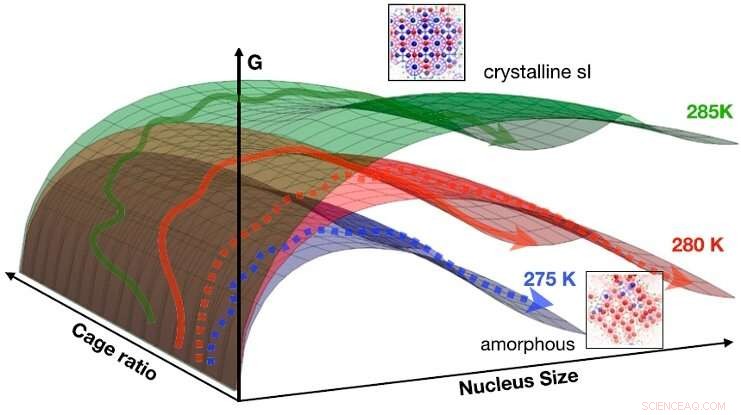
Les résultats peuvent être résumés dans une surface d'énergie libre de CNT idéalisée en fonction de la taille et du rapport de cage pour 275 K (bleu), 280 K (rouge), et 285 K (vert). Les flèches indiquent schématiquement les chemins passant du liquide au solide (flèches en pointillés :vers la phase amorphe; flèches pleines :vers la phase cristalline). À basse température (par exemple, 275 Ko), la barrière d'énergie libre pour nucléer le solide amorphe est la plus faible, la tendance est inversée à une température plus élevée (par exemple, 285 Ko), où les voies échantillonnées finissent pour la plupart dans la phase cristalline. A 280 K les deux mécanismes sont accessibles. Crédit :HIMS/PNAS
Nouvelle approche de simulation
Étant donné que la recherche expérimentale sur la formation des différents polymorphes d'hydrate de méthane souffre d'une résolution limitée, les chercheurs d'Amsterdam dirigés par le professeur Peter Bolhuis ont utilisé des simulations de dynamique moléculaire pour fournir un tel aperçu.
Appliquer une simulation de dynamique moléculaire directe n'est pas très efficace, car à surfusion modérée, la nucléation est un événement très rare, en raison de la présence d'une barrière énergétique très élevée. Une telle simulation nécessiterait des temps de calcul dépassant l'âge de l'Univers. Cependant, parce que l'événement de nucléation en lui-même, bien que rare, se produit très rapidement (sur une échelle de temps de la microseconde), les chercheurs pourraient créer une grande collection de trajectoires de dynamique moléculaire qui présentent ces événements rapides. Une analyse détaillée ultérieure de ces trajectoires a montré comment se déroule la sélection entre les mécanismes concurrents de formation de polymorphes amorphes et cristallins. Leur article PNAS met non seulement en lumière la formation d'hydrates de méthane, mais aussi sur d'autres composés clathrates et la formation de cristaux moléculaires en général.