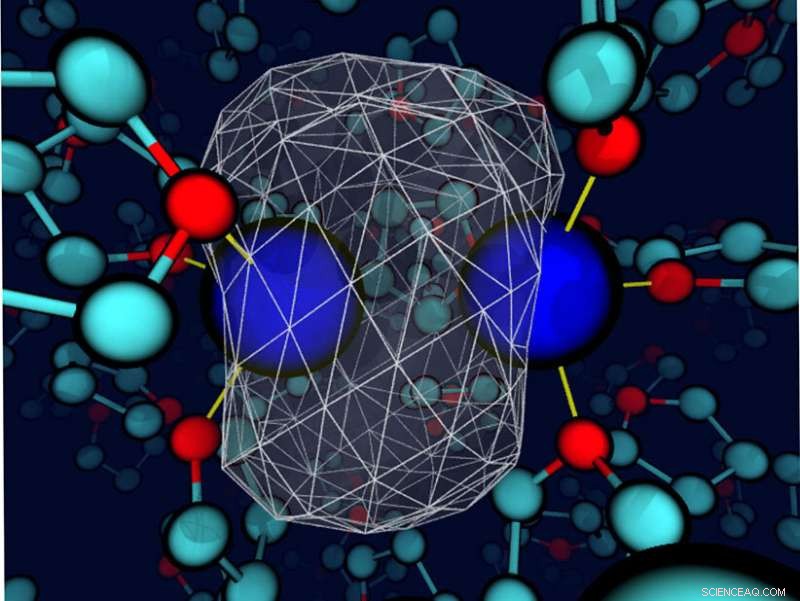
Un « instantané » révèle que le solvant tétrahydrofurane environnant déforme la densité électronique de liaison autour d'un soluté de sodium. Les noyaux de sodium sont des sphères bleues; la densité d'électrons de valence est représentée par une surface blanche transparente avec un treillis métallique blanc enfermant la majeure partie de la densité de charge. Les liaisons entre le sodium et les sites d'oxygène du solvant à proximité sont de fines lignes jaunes. Crédit :Devon Widmer, Université de Californie, Los Angeles
Mélangez quelques amandes entières dans un bocal rempli de noisettes. Secouer. Les noix rebondissent les unes contre les autres, mais ils ne réagissent pas. C'est ainsi que certaines personnes pensent des réactions qui se produisent à l'intérieur des liquides. Les solutés (amandes) réagissent entre eux dans une mer de solvant (noisettes). Mais une nouvelle étude montre que ce n'est pas toujours le cas pour de vraies réactions chimiques. Dans les bonnes conditions, le solvant peut changer l'identité chimique du soluté.
De nombreuses réactions chimiques, en particulier ceux qui concernent le maintien en vie des personnes et des plantes, arriver en solution. Cette recherche montre que dans de nombreuses réactions de ce type, le solvant n'est pas un simple spectateur. Cela signifie réoutiller les attentes et les modèles de calcul. Parce que les mêmes règles pourraient s'appliquer dans les laboratoires de chimie, les chercheurs devront peut-être sélectionner leurs solvants avec plus de soin. Les solvants pourraient contrôler ou modifier l'identité chimique du soluté.
Bien que les solvants soient soigneusement sélectionnés dans certains cas, les liquides sont souvent simplement considérés comme un moyen permettant aux réactifs de se rencontrer. Cependant, le solvant peut jouer un rôle plus important. Ici, les chercheurs ont découvert que lorsque le solvant et le soluté interagissent (énergétiquement dans le même ordre qu'une liaison hydrogène), le solvant peut contrôler la dynamique de liaison et l'identité chimique des solutés simples. Les chercheurs sont arrivés à cette conclusion en étudiant un dimère de sodium dans le solvant faiblement polaire tétrahydrofurane. Les interactions de liaison entre les atomes de solvant et de sodium ont conduit à des états de coordination uniques. Ces états devaient franchir une barrière énergétique libre, subissant essentiellement une réaction chimique, à interconvertir. Plus loin, chaque état de coordination avait sa propre dynamique et ses propres signatures spectroscopiques. Bien que les chimistes connaissent depuis longtemps l'influence des solvants dans certains cas, cette recherche met en évidence l'intérêt de sélectionner soigneusement le solvant pour créer un environnement spécifique dans certains systèmes chimiques en phase condensée.