
Échafaudages hybrides de biotraçage - Impression 3D de structures intelligentes. Crédit image :EnvisionTEC https://www.flickr.com/photos/envisiontec/ Crédit :Mary Ann Liebert, Inc. doi :https://doi.org/10.1089/ten.TEA.2018.0201
En ingénierie tissulaire osseuse (BTE), L'impression 3D est une méthode fiable et personnalisable utilisée pour réparer les défauts osseux en produisant des échafaudages tissulaires biomimétiques. Dans une étude récente publiée en ligne sur Ingénierie tissulaire Partie A (Mary Ann Liebert, Inc), Qing Li et une équipe de scientifiques ont conçu un substitut biomimétique le plus proche de la structure et de la composition osseuses naturelles pour la greffe osseuse. Pour ce travail, ils ont utilisé deux types différents de matériaux à base d'hydroxyapatite (HA) :la nanohydroxyapatite (nHA) et l'os bovin déprotéiné (DBB) dispersé dans du collagène (CoL) pour préparer une bio-encre et concevoir des composites de nHA/CoL et DBB/CoL en 3-D échafaudages imprimés.
La reconstruction esthétique de l'os alvéolaire fonctionnel est difficile après une perte osseuse due à un traumatisme, inflammation et chirurgie. Les scientifiques des matériaux peuvent combiner l'ingénierie tissulaire et les biomatériaux pour favoriser la régénération osseuse alvéolaire; un thème de plus en plus populaire en médecine régénérative. La dernière décennie a vu des avancées significatives dans la technologie d'impression 3D pour la réparation personnalisée des défauts osseux avec une traduction clinique réussie à l'aide d'imprimantes laser à métal. Les avantages de l'impression 3D incluent en grande partie un faible risque de complication, temps opératoire court et bon moulage pendant la chirurgie. Les propriétés biodégradables des matériaux peuvent guider la régénération osseuse in situ. Parmi les techniques disponibles, la bio-impression 3D à basse température (LT-3DP) est optimale pour la reconstruction de l'os alvéolaire, car il peut générer un plan 3D spécifique des défauts osseux du patient pour la reconstruction.

Fonction du système 3D-Bioplotter® telle que démontrée à Rapid 2015, Crédit vidéo :https://www.youtube.com/watch?v=Snqqo5WgZHw Crédit :Mary Ann Liebert, Inc. doi :https://doi.org/10.1089/ten.TEA.2018.0201
Le système LT-3DP peut concevoir plusieurs composites polymères-minéraux avec des propriétés de matériau améliorées. Les échafaudages poreux 3D résultants peuvent imiter l'architecture osseuse pour les interactions cellule-matrice conductrices et permettre une croissance efficace des vaisseaux sanguins pour une BTE avancée. Le matériau polymère nHA sélectionné dans l'étude est un bon candidat pour se substituer à l'os naturel, en raison de sa forte activité ostéoconductrice. Le DBB naturel est un matériau osseux xénogène alternatif, morphologiquement et structurellement similaire à l'os spongieux humain. Dans la présente étude, Li et al. répliqué avec succès un protocole précédemment établi pour la préparation du DBB. Le collagène de type I (CoL-1) est la protéine structurelle la plus abondante dans le corps humain et était donc le mieux adapté pour générer des polymères composites dans la configuration expérimentale proposée pour les constructions aux propriétés biomécaniques améliorées.
Li et al. préparé et classé les bio-encres en trois groupes en tant que CoL, nHA/CoL et DBB/CoL dans l'étude. Pour concevoir les échafaudages composites, les scientifiques ont utilisé le biotraceur 3D (EnvisionTEC, Allemagne). Après avoir imprimé l'échafaudage 3D, ils ont construit une microarchitecture en forme de grille avec des largeurs de pores de 600 µm. La microstructure interne en nid d'abeilles représentait les caractéristiques typiques de l'os spongieux. Les scientifiques des matériaux ont d'abord testé les propriétés physiques et chimiques des échafaudages composites à deux matériaux (nHA/CoL et DBB/CoL), suivi de leur biocompatibilité et de leur impact ostéogénique sur la différenciation des cellules souches de la moelle osseuse (BMSC humaine) lors des interactions cellule-matériau.
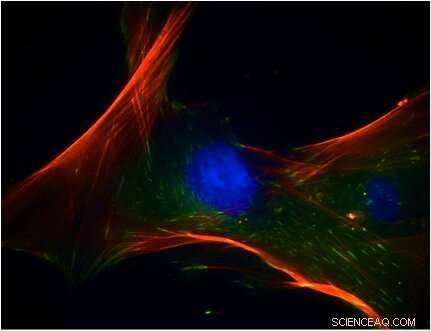
Caractérisation des cellules souches mésenchymateuses humaines avec des marqueurs d'anticorps dirigés vers les régions d'intérêt. Li et al. DAPI d'occasion (bleu, noyaux) FITC-phalloidine (rouge, F-actine ou cytosquelette) et la vinculine (verte, protéine membranaire du cytosquelette). Crédit image :Euro Stem cell https://www.eurostemcell.org/mesenchymal-stem-cells-other-bone-marrow-stem-cells Crédit :Mary Ann Liebert, Inc. doi :https://doi.org/10.1089/ten.TEA.2018.0201
Les scientifiques ont utilisé des méthodes standard de caractérisation des matériaux telles que la spectroscopie photoélectronique à rayons X (XPS), Diffraction des rayons X sur poudre (XRD) et spectroscopie infrarouge à transformée de Fourier (FTIR) pour comprendre la cohérence des deux composites, ainsi que leur diversité par rapport aux liaisons chimiques et aux phases cristallines. Ils ont utilisé la microscopie électronique à balayage (MEB) pour obtenir des résultats d'imagerie, qui a montré différentes morphologies de surface des cristaux et des échafaudages de HA en tant que facteurs affectant la structure poreuse interne du produit. Spécifiquement, le module de Young du groupe nHA/CoL (7,9 ± 0,3 MPa) était supérieur à la fois au groupe CoL (3,5 ± 0,4 MPa) et au groupe DBB/CoL (4,5 ± 0,7 MPa), indiquant une rigidité plus élevée des échafaudages composites nHA/CoL.

Le système 3D-Bioplotter® :un outil de prototypage rapide polyvalent pour traiter les biomatériaux pour l'ingénierie tissulaire assistée par ordinateur basé sur la conception assistée par ordinateur (CAO) 3D des données de tomographie par ordinateur (CT) du patient pour former un échafaudage 3D physique avec une forme extérieure conçue et une structure interne ouverte. Crédit image :EnvisionTEC https://envisiontec.com/3d-printers/3d-bioplotter/starter-series/ Crédit :Mary Ann Liebert, Inc. doi :https://doi.org/10.1089/ten.TEA.2018.0201
Pour les études de biofonctionnalisation, Li et al. ont montré que les deux échafaudages composites soutenaient également la prolifération cellulaire via une coloration par immunofluorescence. Pour ça, ils ont utilisé des anticorps marqués par fluorescence pour colorer et identifier au microscope la croissance des hBMSC sur des structures de surface imprimées en 3D. Au cours de la culture cellulaire, les scientifiques ont utilisé un milieu d'induction ostéogénique (MO) et un milieu de prolifération (PM). La méthode de coloration à la phosphatase alcaline (ALP) utilisée pour déterminer la différenciation des cellules souches, a indiqué l'expression d'ALP dans le groupe OM, mais pas dans le groupe PM.
Les scientifiques ont mené une réaction en chaîne par polymérase en temps réel (RT-PCR) après avoir extrait l'ARN total des cellules souches (hBMSC). Les résultats ont montré les niveaux d'expression des gènes d'intérêt liés à l'ostéogenèse examinés dans l'étude. En comparaison avec les groupes PM, les gènes liés à la différenciation ostéogénique précoce et tardive; Facteur de transcription lié à Runt RUNX2 , Gène de boîte HMG 9 lié au SRY SOX9 , ostéocalcine ROC et CoL1A1 dans le groupe OM a augmenté de manière significative après 7 jours. De cette façon, les chercheurs ont démontré l'ostéogenèse et les effets accrus de la formation de matrice extracellulaire pour les hBMSC cultivés sur les échafaudages 3-D biotracés pour confirmer la biocompatibilité de surface.
Li et al. ont montré que les propriétés physico-chimiques et biologiques des échafaudages bio-imprimés en 3D contenant nHA/CoL ou DBB/CoL étaient bien adaptées comme matériaux de substitution osseuse (BSM) dans l'ingénierie tissulaire osseuse (BTE). La possibilité d'imprimer facilement des échafaudages personnalisables en 3D peut avoir un potentiel pour la recherche translationnelle de la paillasse aux études précliniques et à la clinique à l'avenir.
© 2019 Réseau Science X