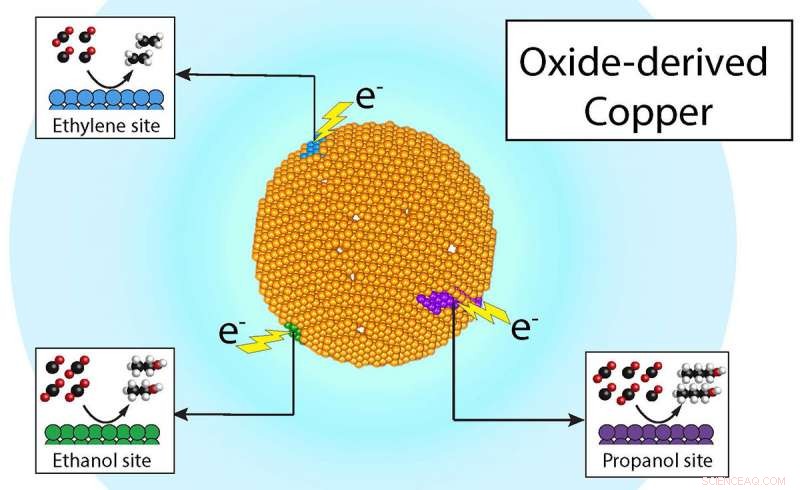
Des chercheurs du Berkeley Lab et du Centre commun pour la photosynthèse artificielle ont démontré que le recyclage du dioxyde de carbone en produits chimiques précieux tels que l'éthylène et le propanol, et des carburants tels que l'éthanol, peut être économique et efficace – tout au long de « sites actifs » spécifiques au produit sur un seul catalyseur au cuivre. Crédit :Ager et Lum/Berkeley Lab
Depuis des décennies, les scientifiques ont cherché des moyens efficaces d'éliminer les émissions excessives de dioxyde de carbone de l'air, et les recycler en produits tels que les carburants renouvelables. Mais le processus de conversion du dioxyde de carbone en produits chimiques utiles est fastidieux, cher, et inutiles et donc non viables sur le plan économique ou environnemental.
Aujourd'hui, une découverte par des chercheurs du Lawrence Berkeley National Laboratory (Berkeley Lab) et du Joint Center for Artificial Photosynthèse (JCAP) du département américain de l'Énergie montre que le recyclage du dioxyde de carbone en produits chimiques et carburants de valeur peut être économique et efficace, le tout grâce à un seul catalyseur au cuivre. .
L'ouvrage paraît dans l'édition du 17 décembre de la revue Catalyse naturelle .
Aller là où se trouve l'action :sites actifs spécifiques aux produits
Quand tu prends un morceau de cuivre, il peut être doux au toucher, mais au niveau microscopique, la surface est en fait bosselée - et ces bosses sont ce que les scientifiques appellent « sites actifs, " a déclaré Joël Ager, un chercheur du JCAP qui a dirigé l'étude. Ager est membre du personnel scientifique de la division des sciences des matériaux du Berkeley Lab et professeur adjoint au département des sciences et de l'ingénierie des matériaux de l'UC Berkeley.
C'est sur ces sites actifs que s'opère la magie de l'électrocatalyse :les électrons de la surface du cuivre interagissent avec le dioxyde de carbone et l'eau dans une séquence d'étapes qui les transforment en produits comme l'éthanol; éthylène, le précurseur des sacs en plastique; et propanol, un alcool couramment utilisé dans l'industrie pharmaceutique.

Les chercheurs du Berkeley Lab et du Centre commun pour la photosynthèse artificielle Yanwei Lum (à gauche) et Joel Ager ont découvert que le cuivre a le potentiel en tant que catalyseur pour transformer le dioxyde de carbone en produits chimiques et carburants durables sans aucun sous-produit inutile, créer une alternative verte à la fabrication chimique actuelle. Crédit :Marilyn Chung/Berkeley Lab
Depuis les années 1980, quand le talent du cuivre pour convertir le carbone en divers produits utiles a été découvert, il a toujours été supposé que ses sites actifs n'étaient pas spécifiques à un produit - en d'autres termes, vous pourriez utiliser du cuivre comme catalyseur pour fabriquer de l'éthanol, éthylène, propanol, ou un autre produit chimique à base de carbone, mais il faudrait passer par beaucoup d'étapes pour séparer les indésirables, produits chimiques résiduels formés au cours des étapes intermédiaires d'une réaction chimique avant d'arriver à votre destination finale - le produit chimique final.
"L'objectif de la chimie 'verte' ou durable est d'obtenir le produit que vous souhaitez lors de la synthèse chimique, " a déclaré Ager. " Vous ne voulez pas séparer les choses que vous ne voulez pas des produits désirables, parce que c'est cher et indésirable pour l'environnement. Et ces dépenses et ces déchets réduisent la viabilité économique des combustibles solaires à base de carbone. »
Alors, quand Ager et le co-auteur Yanwei Lum, qui était un doctorat de l'UC Berkeley. étudiant au laboratoire d'Ager au moment de l'étude, étudiaient les propriétés catalytiques du cuivre pour un projet de combustibles solaires, se demandaient-ils, "Et qu'est-ce qui se passerait si, comme la photosynthèse dans la nature, nous pourrions utiliser les électrons des cellules solaires pour piloter des sites actifs spécifiques d'un catalyseur au cuivre afin de produire un flux de produit pur d'un carburant ou d'un produit chimique à base de carbone ?", a déclaré Ager.
Retracer l'origine d'un produit chimique grâce à son « passeport »
Des études antérieures avaient montré que le cuivre « oxydé » ou rouillé est un excellent catalyseur pour la fabrication d'éthanol, éthylène, et propanol. Les chercheurs ont émis l'hypothèse que si les sites actifs dans le cuivre étaient en fait spécifiques au produit, ils pourraient retracer l'origine des produits chimiques grâce aux isotopes du carbone, "un peu comme un passeport avec des tampons nous indiquant quels pays ils ont visités, " a dit Ager.
"Quand nous avons pensé à l'expérience, nous avons pensé que c'était une idée si peu évidente, que ce serait fou d'essayer, " Ager a dit. "Mais nous ne pouvions pas le laisser aller, parce que nous pensions aussi que cela fonctionnerait, car nos précédentes recherches sur les isotopes nous avaient permis de découvrir de nouvelles voies réactionnelles. »

Images de microscopie électronique à balayage (MEB) de cuivre dérivé d'oxyde montrées à différents grossissements. Une découverte par des chercheurs du Berkeley Lab et du Centre commun pour la photosynthèse artificielle a révélé qu'à l'intérieur de ce matériau poreux se trouvent des « sites actifs » spécifiques au produit. « où les électrons de la surface du cuivre interagissent avec le dioxyde de carbone et l'eau dans une séquence d'étapes qui les transforment en produits précieux tels que le carburant à l'éthanol, éthylène, et propanol. Crédit :Ager et Lum/Berkeley Lab
Alors pour les prochains mois, Lum et Ager ont mené une série d'expériences en utilisant deux isotopes du carbone – le carbone 12 et le carbone 13 – comme « timbres de passeport ». Le dioxyde de carbone a été étiqueté avec du carbone-12, et le monoxyde de carbone – un intermédiaire clé dans la formation de liaisons carbone-carbone – a été marqué au carbone-13. Selon leur méthodologie, les chercheurs ont estimé que le rapport carbone-13 contre carbone-12 - la "signature isotopique" - trouvé dans un produit déterminerait de quels sites actifs le produit chimique est originaire.
Après que Lum ait mené des dizaines d'expériences et utilisé la spectrométrie de masse de pointe et la spectroscopie RMN (résonance magnétique nucléaire) au JCAP pour analyser les résultats, ils ont découvert que trois des produits – l'éthylène, éthanol, et le propanol - avaient des signatures isotopiques différentes montrant qu'ils provenaient de différents sites sur le catalyseur. « Cette découverte motive de futurs travaux pour isoler et identifier ces différents sites, " a déclaré Lum. " Mettre ces sites spécifiques à un produit dans un seul catalyseur pourrait un jour aboutir à une génération très efficace et sélective de produits chimiques, " dit Lum.
Des jours verts à venir pour la fabrication de produits chimiques
La nouvelle méthodologie des chercheurs - ce qu'Ager décrit comme " une chimie simple avec une touche environnementale et économique " - est ce qu'ils espèrent être un nouveau départ pour la fabrication de produits chimiques verts où une cellule solaire pourrait alimenter en électrons des sites actifs spécifiques dans un catalyseur en cuivre pour optimiser la production de carburants à l'éthanol.
"Peut-être qu'un jour cette technologie pourrait permettre d'avoir quelque chose comme une raffinerie de pétrole, mais alimenté par le soleil, extraire le dioxyde de carbone de l'atmosphère et créer un flux de produits utiles, " il a dit.