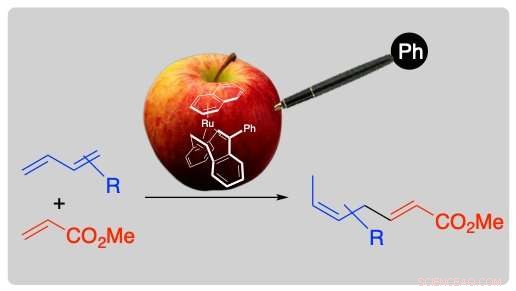
Prenez par exemple une pomme empoisonnée, il peut émettre un arôme doux et enivrant juste en collant un stylo et changer pour être délicieux. Crédit :Figure adaptée avec la permission de Organometallics, 2018, 10.1021/acs.organomet.8b00645. © 2018 Société chimique américaine
Des scientifiques de l'Université d'agriculture et de technologie de Tokyo (TUAT), Japon, ont découvert qu'un poison catalytique, qui désactive les catalyseurs homogènes, peut « renaître » en tant que ligand efficace par introduction d'un substituant, dans les réactions chimiques. Cette découverte est utile pour étendre la conception du ligand dans des catalyseurs homogènes. Cette recherche a été publiée en ligne dans la revue Organométalliques .
Un groupe de substances qui arrêtent complètement ou partiellement une catalyse par contamination est largement connu sous le nom de poison de catalyseur. Des exemples typiques de poison de catalyseur sont le mercure et les composés sulfurés pour la catalyse hétérogène et une substance chimique appelée dibenzocyclooctatetraène pour la catalyse homogène. Ces substances désactivent le catalyseur en se liant très étroitement au site actif. Le poison homogène du catalyseur, cependant, peut être modifié en tant que ligand efficace par introduction d'un substituant.
Une équipe de recherche de la TUAT recherchait des ligands diènes cycliques pour un catalyseur au ruthénium (Ru) afin de synthétiser des diènes sautés, qui sont connus pour être des sous-structures de nombreux produits naturels et molécules pharmaceutiques. Par accident, ils sont tombés sur du dibenzocyclooctatetraène, un poison catalytique homogène, travailler comme un ligand. Après le dépistage, ils ont finalement découvert que la fixation du phényle au poison du catalyseur était un ligand très efficace. Techniquement, réaction du b-myrcène (l'un des groupes de produits naturels les plus répandus) avec l'acrylate de méthyle catalysée par un complexe Ru avec 1, Le 5-cyclooctadiène (1 pour cent en moles; un ligand diène cyclique typique) n'a produit le produit de couplage linéaire qu'avec un rendement de 23 pour cent à 30 degrés C pendant 7 heures. Cependant, le complexe 5-phényldibenzocyclooctatetraène (le dibenzocyclooctatetraène était attaché à un groupe phényle) de Ru a catalysé la réaction pour donner le produit avec un rendement de 97 % en 1 heure dans les mêmes conditions.
Le dibenzocyclooctatetraene se lie étroitement au centre Ru de par sa nature. L'une des clés de cette forte activité catalytique provient probablement de l'effet stérique du groupement phényle. En présence de catalyse donnant des diènes sautés, les molécules de diène sauté formées ont tendance à rester sur le catalyseur en tant qu'intermédiaire stable, mais le groupe phényle balaie la molécule de produit loin du catalyseur. Comme résultat, le catalyseur peut prendre des mesures pour une catalyse supplémentaire.
"Avant un processus catalytique, il faut normalement éliminer les substances qui agissent comme des poisons du catalyseur pour ne pas désactiver le catalyseur. Ils sont gênants dans les catalyses car ils sont étroitement liés au site actif des catalyseurs. Cependant, la nature fortement liée au catalyseur est un avantage en tant que ligand dans les catalyseurs homogènes. Notre découverte nous a fait connaître une petite altération d'un poison de catalyseur, non seulement ne gêne pas la catalyse, mais apporte une accélération de la catalyse en tant que ligand de catalyseur. Nos résultats sont certainement utiles au développement ultérieur de la conception de ligands résistants pour les catalyseurs. En d'autres termes, un poison catalyseur n'est pas né de cette façon, mais peut renaître en tant que ligand efficace, " dit Masafumi Hirano, un professeur de chimie de la TUAT et un directeur de l'étude.