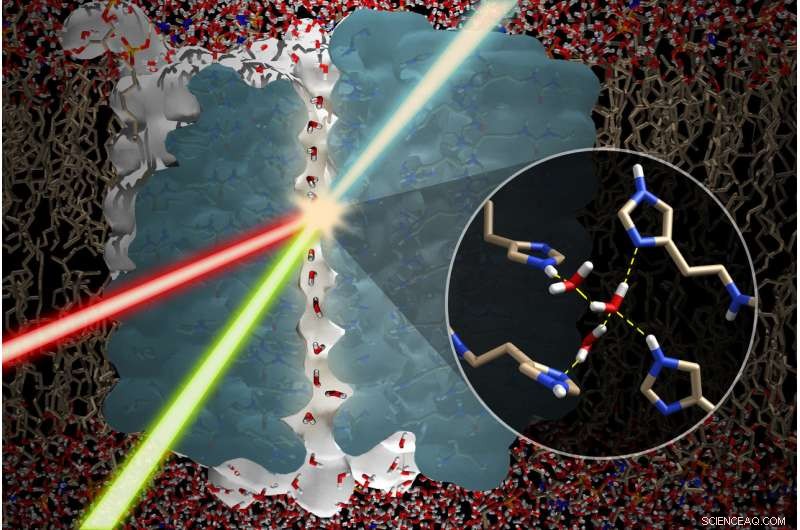
Détails d'un fil d'eau (canal central) noyé dans un canal d'immidazole auto-assemblé (bleu) dans une bicouche lipidique. La sommation des faisceaux incidents visibles (vert) et IR (rouge) produit un faisceau SFG (génération de fréquence de somme) résultant qui caractérise la liaison hydrogène du fil d'eau au niveau moléculaire (avec l'aimable autorisation de Poul Petersen, L'Université de Cornell). Crédit :Institut polytechnique Rensselaer
Les aquaporines sont des protéines qui servent de canaux d'eau pour réguler le flux d'eau à travers les membranes cellulaires biologiques. Ils éliminent également l'excès de sel et les impuretés dans le corps, et c'est cet aspect qui a suscité beaucoup d'intérêt ces dernières années sur la façon d'imiter les processus biochimiques des aquaporines potentiellement pour les systèmes de dessalement de l'eau.
Une équipe internationale de chercheurs co-dirigée par Georges Belfort a découvert l'eau, sous forme de "fils d'eau, " contenu dans une autre molécule, l'imidazole, un composé organique à base d'azote qui pourrait être utilisé comme élément de base potentiel pour les aquaporines artificielles. Les résultats ont été récemment publiés dans Avancées scientifiques . Belfort est professeur de l'Institut et professeur de génie chimique et biologique à l'Institut polytechnique Rensselaer.
collègue de Belfort, Mihail Barboiu, un responsable de recherche à l'Institut Européen des Membranes (EMI) en France, a synthétisé et étudié la dynamique d'une structure en anneau de l'imidazole intégré dans une bicouche lipidique supportée (c'est-à-dire, dans un modèle synthétique d'une membrane biologique entourant une cellule). EMI opère sous les auspices de plusieurs organisations, dont le Centre National de la Recherche Scientifique de France (en abrégé CNRS).
Les études aux rayons X de Barboiu et les simulations informatiques dynamiques du chercheur CNRS Marc Baaden montrent que la structure cyclique de l'imidazole fait de la molécule un candidat idéal pour découvrir comment les aquaporines artificielles pourraient être développées. En théorie, les molécules d'imidazole assemblées agissent comme une aquaporine en permettant aux molécules d'eau d'entrer et éventuellement de circuler à travers le centre de la structure annulaire tout en empêchant les autres molécules d'entrer.
Toujours, il n'y avait aucune preuve directe que l'eau existait à l'intérieur du canal d'eau imidazole. Découvrir, Barboiu fait appel à Belfort et Poul Petersen, professeur adjoint de chimie à l'Université Cornell.
Grâce à leurs études expérimentales, Belfort et Petersen ont découvert que non seulement l'eau existe dans le canal d'eau imidazole, mais aussi que la construction d'anneau imidazole induit les molécules d'eau à s'auto-assembler en une structure de chaîne linéaire hautement orientée – ou ce que les chercheurs ont surnommé « fils d'eau ».
"Pour la première fois, nous avons fait une observation directe de cette structure d'eau unique à l'intérieur d'un canal d'eau synthétique qui imite une aquaporine, ", a déclaré Belfort.
Belfort et ses collègues ont également découvert que la chiralité des molécules d'imidazole oriente les molécules d'eau et pourrait augmenter la perméabilité de l'eau à travers le canal d'eau par rapport à achiral (c'est-à-dire, non chirales) molécules d'imidazole qu'elles ont également assemblées. La chiralité se produit lorsqu'une image miroir d'un objet n'est pas superposable, par exemple, votre main gauche et votre main droite.
Dans le cas de la molécule d'imidazole, sa chiralité dépend de la manière dont les groupes d'atomes d'une molécule sont organisés. Comme Belfort l'a expliqué, les atomes d'imidazole chiraux peuvent être vus comme des rayons sur une roue de bicyclette qui ne peuvent pas être superposés aux « rayons » d'un imidazole achiral.
"Si vous placez plusieurs de ces anneaux les uns sur les autres comme un tas de crêpes, le centre (l'"axe") des rayons contient les molécules d'eau et leur permet de se connecter les unes aux autres de manière ordonnée pour former un fil d'eau, ", a-t-il déclaré. "Nos résultats ont également montré que le fil d'eau changeait d'orientation lorsque la chiralité de l'imidazole changeait, confirmant en outre que la forme chirale de l'imidazole contrôle le comportement de l'eau."
Dans leur étude, les chercheurs ont utilisé des canaux d'eau artificiels qu'ils ont créés à partir de structures auto-assemblées d'imidazole à l'intérieur de bicouches lipidiques, membranes minces qui forment une barrière continue autour des cellules. Les éléments constitutifs de l'imidazole ont été synthétisés par Barboiu et son groupe en France. Le groupe de recherche de Belfort a ensuite assemblé les bicouches lipidiques pour contenir les structures imidazole.
L'équipe de Belfort a utilisé une microbalance à cristal de quartz (QCM) pour mesurer l'assemblage et la teneur en eau. Les chercheurs utilisent QCM pour mesurer de petits changements de masse sur un cristal de quartz vibrant. Les lipides contenant les structures de fil d'eau ont ensuite été transportés à Cornell par Mirco Sorci, chercheur associé au laboratoire de Belfort, d'analyser plus avant la présence du fil d'eau et son orientation, à l'aide d'un instrument spécial qui mesure les liaisons hydrogène entre les molécules d'eau appelé spectromètre à génération de fréquence somme.