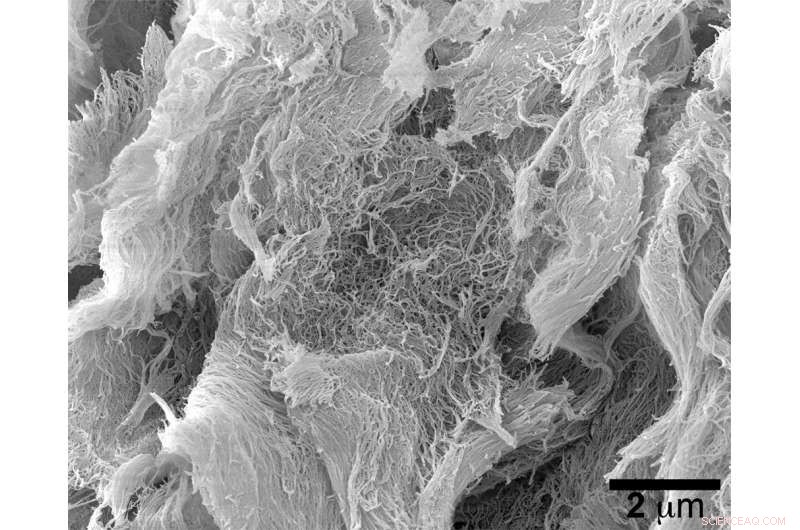
Un synthétique, L'hydrogel injectable développé à l'Université Rice a augmenté la toxicité d'une nouvelle classe de médicaments d'immunothérapie anticancéreuse. Cette image de microscopie électronique à balayage montre les nanofibres auto-assemblées qui composent l'hydrogel. Crédit :Hartgerink Research Group/Rice University
Un médicament d'immunothérapie intégré dans un hydrogel à libération lente inventé à l'Université Rice en collaboration avec le Centre des sciences de la santé de l'Université du Texas à Houston (UTHealth) semble être très efficace pour tuer les cellules cancéreuses.
STINGel combine une nouvelle classe de médicaments d'immunothérapie appelés stimulateurs des agonistes du gène de l'interféron (STING) avec un hydrogel injectable qui libère le médicament à dose constante pour activer le système immunitaire afin de tuer les cellules cancéreuses. Il a été développé par le laboratoire Rice du chimiste et bio-ingénieur Jeffrey Hartgerink et l'alun de Rice Simon Young, professeur adjoint de chirurgie buccale et maxillo-faciale à UTHealth.
Dans les essais cliniques, les médicaments d'immunothérapie ont démontré de fortes capacités de lutte contre le cancer. La recherche a également montré que les médicaments sont rapidement évacués du corps, et les essais actuels nécessitent des injections multiples.
La nouvelle recherche, qui est détaillé dans Biomatériaux , ont montré que les gels peptidiques à libération lente pouvaient administrer en continu des médicaments d'immunothérapie aux sites tumoraux pendant de longues périodes.
Hartgerink est un pionnier dans le développement d'hydrogels de peptides multidomaines (MDP) auto-assemblés, qui imitent la matrice extracellulaire du corps pour encourager la croissance des cellules et des systèmes vasculaires pour la réparation des tissus. L'hydrogel est injecté sous forme liquide, devient semi-solide à l'intérieur du corps et se dégrade lentement avec le temps.
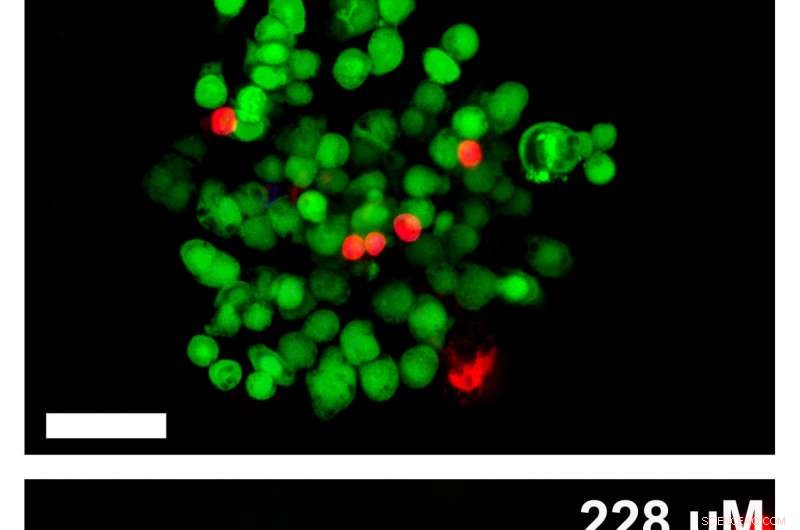
Ces images montrent comment les cellules cancéreuses ont réagi trois jours après la libération programmée des médicaments d'immunothérapie du STINGel de l'Université Rice. Les doses du médicament d'immunothérapie CDN augmentent de haut en bas ; les cellules vertes vivantes cèdent la place aux globules rouges morts à mesure que la dose augmente. Les barres d'échelle sont de 50 microns. Crédit :Hartgerink Research Group/Rice University
L'hydrogel de la nouvelle étude est également accueillant pour les cellules, mais quand les envahisseurs sont des cellules cancéreuses, ils ont des ennuis. Les médicaments d'immunothérapie appelés dinucléotides cycliques (CDN) les attendent à l'intérieur du gel.
Hartgerink, professeur de chimie et de bio-ingénierie, a déclaré que la concentration de CDN dans l'hydrogel est importante.
« L'approche normale de la livraison de CDN est une simple injection, mais cela conduit à une diffusion très rapide du médicament dans tout le corps et réduit sa concentration au site de la tumeur à des niveaux très faibles, " a-t-il dit. " En utilisant la même quantité de CDN, l'approche STINGel permet à la concentration de CDN près de la tumeur de rester beaucoup plus élevée pendant de longues périodes de temps."
STINGel a été étudié à la fois en cultures de laboratoire et in vivo. Pour la partie in vivo, six groupes de 10 rongeurs chacun ont été traités avec du CDN seul, collagènes de contrôle seuls ou avec CDN, MDP seul ou STINGel (CDN plus MDP). Seul un animal CDN ou collagène plus CDN sur 10 a survécu 105 jours, mais six des 10 animaux traités avec STINGel ont survécu. Ceux-ci se sont également avérés résistants à l'implantation ultérieure de cellules cancéreuses, ce qui signifie que leur système immunitaire a été formé pour identifier et détruire avec succès à la fois le cancer existant et l'apparition future de ce cancer, dit Hartgerink.
Le laboratoire a testé des hydrogels plus courants, mais a constaté qu'ils n'étaient pas en mesure de fournir la même libération contrôlée et n'ont également pas fourni d'avantage supplémentaire par rapport au traitement CDN observé dans les essais cliniques. "L'hydrogel MDP fournit un environnement unique pour la libération de CDN que d'autres gels ne peuvent tout simplement pas égaler, " a déclaré Hartgerink.
"Le CDN que nous avons utilisé dans cette étude est actuellement en essais cliniques, ", a-t-il déclaré. "Nous pensons que notre approche STINGel a le potentiel d'élargir considérablement le champ d'application de ce puissant médicament d'immunothérapie à un plus grand nombre de cancers résistants."