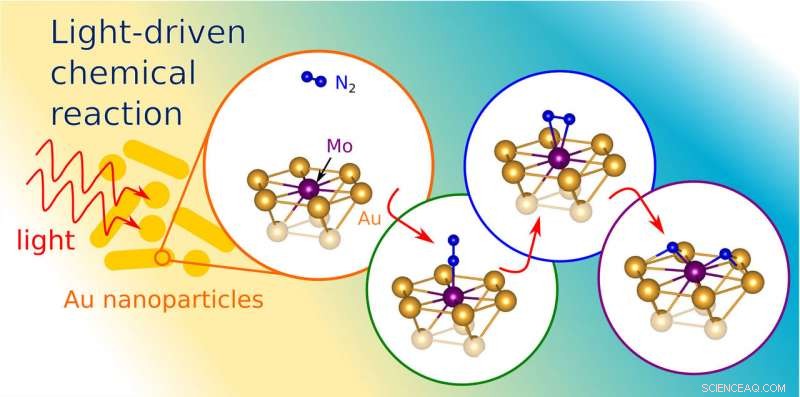
Les nanostructures en or concentrent l'énergie lumineuse et renforcent la capacité du molybdène à séparer les deux atomes d'azote d'une molécule de N2 (illustration des chercheurs). Crédit :Université de Princeton
Les engrais synthétiques à base d'azote constituent l'épine dorsale de l'approvisionnement alimentaire mondial, mais sa fabrication nécessite une énorme quantité d'énergie. Maintenant, la modélisation informatique à l'Université de Princeton indique une méthode qui pourrait réduire considérablement l'énergie nécessaire en utilisant la lumière du soleil dans le processus de fabrication.
Les fabricants fabriquent actuellement des engrais, pharmaceutiques et autres produits chimiques industriels en extrayant l'azote de l'air et en le combinant avec de l'hydrogène. L'azote gazeux est abondant, constituant environ 78 pour cent de l'air. Mais l'azote atmosphérique est difficile à utiliser car il est enfermé dans des paires d'atomes, appelé N
Une équipe de recherche dirigée par Emily Carter, le doyen de l'ingénierie de Princeton et le professeur Gerhard R. Andlinger en énergie et environnement, voulait savoir s'il serait possible d'utiliser la lumière pour affaiblir la liaison dans la molécule d'azote atmosphérique. Si c'est le cas, cela permettrait aux fabricants de réduire radicalement l'énergie nécessaire pour diviser l'azote pour l'utiliser dans les engrais et un large éventail d'autres produits.
« Exploiter l'énergie de la lumière du soleil pour activer des molécules inertes telles que l'azote, et les gaz à effet de serre méthane et dioxyde de carbone d'ailleurs, est un grand défi pour une production chimique durable, " dit Carter, qui est professeur de génie mécanique et aérospatial et de mathématiques appliquées et computationnelles. "Remplacer la haute température traditionnelle énergivore, fabrication chimique à haute pression avec la lumière du soleil, processus à température ambiante est un autre moyen de réduire notre dépendance aux combustibles fossiles. »
Les chercheurs souhaitaient tirer parti du comportement unique de la lumière lorsqu'elle interagit avec des nanostructures métalliques plus petites qu'une seule longueur d'onde de lumière. Entre autres effets, le phénomène, appelée résonance plasmonique de surface, peut concentrer la lumière et améliorer les champs électriques. Dr John Mark Martirez, chercheur post-doctoral et membre de l'équipe de recherche de Princeton, a déclaré que les chercheurs pensaient qu'il serait possible d'utiliser les résonances plasmoniques pour augmenter le pouvoir d'un catalyseur de séparer les molécules d'azote.
"C'est une méthode différente de fournir de l'énergie pour briser le lien, " dit-il. " Au lieu d'utiliser la chaleur, nous utilisons la lumière."
Dans un article du 5 janvier dans la revue Avancées scientifiques , les chercheurs décrivent comment ils ont utilisé des simulations informatiques pour modéliser le comportement de la lumière dans de minuscules structures faites d'or et de molybdène. L'or fait partie d'une classe de métaux, y compris le cuivre et l'aluminium, qui peut être façonné pour produire des résonances plasmoniques de surface. Les chercheurs ont utilisé un ensemble d'outils de modélisation informatique pour simuler des nanostructures en or, et ajouté du molybdène à sa surface, qui est un métal qui peut diviser les molécules d'azote.
"Le métal plasmonique agit comme un paratonnerre, " a déclaré Martirez. " Il concentre une grande quantité d'énergie lumineuse dans une très petite zone. "
L'énergie lumineuse concentrée augmente efficacement la capacité du molybdène à séparer les deux atomes d'azote.
"L'interaction de la lumière amplifie le champ électrique près de la surface du catalyseur, qui aide à briser le lien, ", a déclaré Martirez.
Les calculs des chercheurs indiquent que la technique de résonance plasmonique devrait être capable de réduire considérablement l'énergie nécessaire pour craquer les molécules d'azote atmosphérique. Carter a déclaré que la modélisation indique qu'il devrait être possible de dissocier la molécule d'azote à température ambiante et à des pressions inférieures à celles requises par le processus Haber-Bosch.
Simuler le processus tout en tenant compte de l'effet de la lumière était un défi. La plupart des modèles informatiques capables d'évaluer avec précision les réactions chimiques au niveau moléculaire, et tenir compte des changements induits par la lumière, ne peut simuler que quelques atomes à la fois. Bien que cela soit scientifiquement valable, il ne suffit généralement pas à évaluer les procédés industriels.
Les chercheurs se sont donc tournés vers une technique développée à l'origine par Carter qui permet aux scientifiques d'utiliser des méthodes très précises pour modéliser un petit fragment de la surface, puis d'étendre ces résultats pour comprendre un système plus large. La technique, appelée théorie de la fonction d'onde corrélée intégrée, a été vérifié à plusieurs reprises et largement utilisé au sein du groupe Carter, et les chercheurs sont confiants dans son application au problème de fractionnement de l'azote.
Carter a déclaré que son équipe collaborait avec Naomi Hallas et Peter Nordlander de l'Université Rice pour tester la technique de résonance plasmonique en laboratoire. Les chercheurs ont travaillé ensemble sur des projets similaires dans le passé, notamment en démontrant la dissociation de molécules d'hydrogène sur des nanoparticules d'or pur.
Comme prochaine étape, Carter a déclaré qu'elle aimerait étendre la technique de résonance plasmonique à d'autres liaisons chimiques fortes. Un candidat est la liaison carbone-hydrogène dans le méthane. Les fabricants utilisent du gaz naturel pour fournir de l'hydrogène dans les engrais ainsi que d'autres produits chimiques industriels importants. Donc, trouver une méthode à faible énergie pour rompre ce lien pourrait également être une aubaine pour la fabrication.