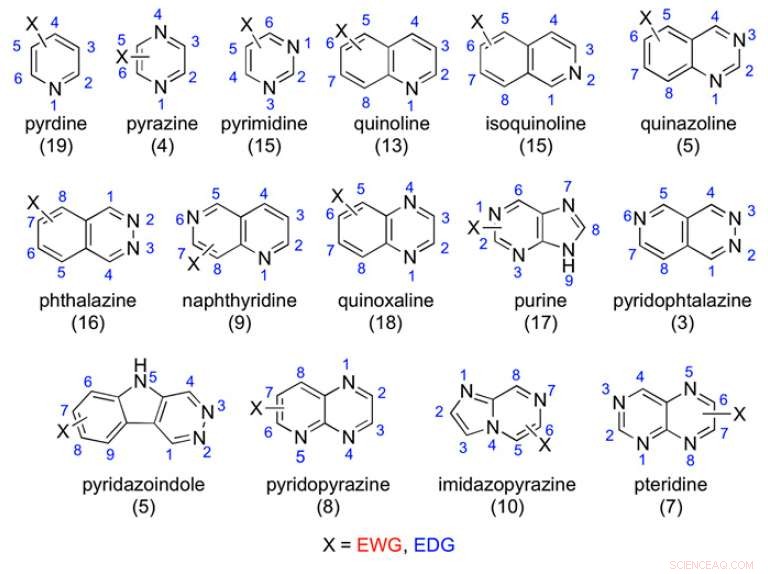
Exemples d'échafaudages aza-aromatiques étudiés :le nombre de composés testés est indiqué entre parenthèses. Crédit :(c) Actes de l'Académie nationale des sciences (2017). DOI :10.1073/pnas.1618881114
(Phys.org) - La conception de médicaments implique des essais et des erreurs guidés. La façon dont le corps métabolise un médicament particulier est importante pour déterminer l'efficacité du médicament. De nombreuses études ont été menées pour comprendre comment les xénobiotiques interagissent avec les cytochromes P450, une classe importante d'enzymes dans le métabolisme des médicaments, mais peu de recherches ont été menées pour comprendre le métabolisme de l'aldéhyde oxydase (AOX). AOX, situé dans le foie, joue un rôle important dans le métabolisme des médicaments; cependant, de nombreux médicaments potentiels échouent lors des essais de stade avancé en raison de leur interaction avec l'AOX.
Pour mieux comprendre la relation structure-métabolisme entre les groupes fonctionnels et les AOX ainsi que pour établir des directives générales pour le métabolisme des médicaments non cytochromes P450, des chercheurs de l'Université de Perguia en Italie ont mené des tests sur 198 composés avec des échafaudages aza-aromatiques pour voir lesquels étaient oxydés par l'AOX. Par ailleurs, ils ont testé 75 échafaudages en amide pour déterminer lesquels étaient hydrolysés. Ils ont découvert que des facteurs électroniques ainsi que l'encombrement stérique affectaient l'orientation de la molécule dans le site actif du MoCo, qui a déterminé si le composé était métabolisé par l'AOX. Leur travail apparaît dans le Actes de l'Académie nationale des sciences .
L'AOX est une enzyme située dans le foie qui a tendance à oxyder les composés aza-aromatiques en tant que métabolite de phase I. Des études ont montré que l'AOX active le carbone non substitué ortho à l'azote sur l'hétérocycle aza. Parce que c'est le carbone le plus électropositif du cycle aromatique, la densité électronique joue probablement un rôle dans l'activation de l'AOX. Mais ces études, ainsi que d'autres qui examinent le métabolisme des AOX, étaient basées sur un petit nombre de molécules qui ne permet pas de déduire un schéma général pour la relation structure-métabolisme.
Dans l'étude actuelle, Lepri et al. testé 198 composés aza-aromatiques pour voir s'ils étaient oxydés par l'AOX. Chacun de ceux-ci avait des échafaudages aza-aromatiques typiques avec des variations sur les substituants attracteurs d'électrons et donneurs d'électrons. Ils ont soit acquis, soit réalisé ce catalogue de composés, puis mené des études de métabolisme in vitro à l'aide de cytosol hépatique humain.
Les calculs DFT ont été utilisés pour élucider les effets de la densité électronique sur l'activité AOX. Le site de métabolisme sur le composé aromatique avait tendance à correspondre au carbone non substitué le plus électro-positif, comme prévu. En outre, Des études de calculs ont été utilisées pour effectuer une analyse d'amarrage des composés dans le site actif d'AOX.
Les auteurs ont trouvé certaines tendances pour le site du métabolisme; cependant, ces tendances sont compliquées par plusieurs facteurs. L'échafaudage de pyridine était le seul qui, comme classe d'échafaudage, n'était pas sensible au métabolisme des AOX. Les autres groupes dépendaient fortement de la densité électronique sur des carbones particuliers ou, comme les auteurs l'ont trouvé avec des composés tels que les quinoxalines et certains composés bicycliques, l'encombrement stérique dans le site actif a empêché le métabolisme des AOX.
Lepri et al. également testé 73 composés amides pour voir si AOX hydrolysait la liaison amide. En général, s'il y avait un groupe électroattracteur en position ortho sur l'analine, alors AOX ne l'a pas oxydé. S'il y avait un groupe donneur d'électrons, alors il l'a fait. Les versions méta et para des groupes donneurs d'électrons et attracteurs d'électrons n'étaient pas sensibles au métabolisme de l'AOX.
Les effets de l'exposition étaient un élément important pour déterminer si un composé était métabolisé par l'AOX. Ceci est lié à l'orientation de la molécule vers le centre MoCo dans le site actif de l'AOX. Certains groupes volumineux n'ont entraîné aucune activité là où on s'y attendait sur la base d'études informatiques. En outre, l'hydrophobie a également affecté la façon dont le composé interagissait avec le site actif. Lorsque le charbon réactif est exposé au centre MoCo, alors le composé est facilement métabolisé. Mais, lorsque la partie non réactive du composé est orientée vers le centre MoCo, alors le composé est moins susceptible d'être oxydé ou hydrolysé.
Les auteurs soulignent que de ces expériences "il ressort qu'il n'est pas du tout simple de prédire si un composé est un substrat d'AOX ou non". La difficulté réside dans la compréhension de la réactivité du carbone électrophile sur le composé ainsi que de la façon dont ce composé particulier s'orientera dans le site actif de l'enzyme. Cependant, cette étude fournit un point de départ pour des études complémentaires et des techniques de modélisation plus sophistiquées.
© 2017 Phys.org