Crédit :Wiley
La membrane plasmique sert de plaque tournante majeure pour les cascades de signaux afin de contrôler les processus cellulaires cruciaux. Mais c'est un milieu fluide, ce qui rend les processus de signalisation difficiles à surveiller. Maintenant, Des scientifiques allemands ont conçu une technique moléculaire de « pinceau » pour déclencher, contrôler, et également surveiller les processus de signalisation. Comme ils l'écrivent dans le journal Angewandte Chemie , leur système modulaire composé de blocs de construction moléculaires activables par la lumière peut, par exemple, induire une contraction structurée à l'intérieur des cellules vivantes.
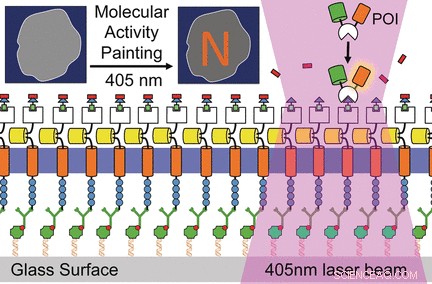
La membrane plasmique est une barrière lipidique étanche entourant la cellule. Les protéines membranaires contrôlent les entrées et sorties d'eau, ions, protéines, et d'autres composés. Les signaux extracellulaires sont transduits par des récepteurs à travers la membrane pour déclencher des processus intracellulaires tels que le mouvement ou la différenciation cellulaire. La visualisation de tels événements au niveau moléculaire reste un défi majeur, principalement en raison de la diffusion rapide des récepteurs protéiques dans la membrane plasmique. Par conséquent, les groupes de Leif Dehmelt au Max Planck Institute of Molecular Physiology et Yaowen Wu au Chemicals Genomics Center de la Max Planck Society, Allemagne, ont développé une nouvelle technologie appelée "Peinture d'Activité Moléculaire" (MAP), qui combine l'immobilisation et l'activation contrôlée par la lumière :les récepteurs artificiels solidement ancrés sur le substrat cellulaire sont équipés d'un système moléculaire modulaire conçu. Une impulsion lumineuse active les blocs de construction modulaires, ce qui peut déclencher des cascades de signaux localisées conduisant éventuellement à des mouvements du cytosquelette. Cette technologie rend la réponse cellulaire visible comme un coup de pinceau sur la membrane.
Le cœur de la technologie MAP est une molécule soluble à plusieurs composants assemblée à partir de quatre parties fonctionnelles :une fraction chloroalkyle, un lieur polymère (PEG), un groupe moléculaire appelé triméthroprime ou TMP, et un groupe sensible à la lumière appelé Nvoc. Ce « dimériseur chimique en cage », comme on l'appelle, peut remplir plusieurs tâches :Par sa partie chloroalkyle, il se lie à un récepteur artificiel, qui est solidement ancré et immobilisé sur le substrat cellulaire. Le groupe Nvoc peut être retiré ("uncaged") par une seule impulsion lumineuse. Le fragment TMP non mis en cage est ensuite ciblé par un facteur conçu pour induire une cascade de signaux dans la cellule. L'ensemble du système vise un seul objectif :le contrôle et la visualisation de la fonction moléculaire dans les cellules vivantes.
Grâce à cette technologie, les scientifiques ont induit une contraction modelée de l'actomyosine à l'intérieur d'une cellule de mammifère vivante. Ou, plus exactement, ils ont "peint" la lettre "N" sur la membrane plasmique d'une cellule vivante. "'Molecular Activity Painting' [...] permet un interrupteur, perturbations modelées des réseaux de régulation avec une précision micrométrique, " proposent les scientifiques.