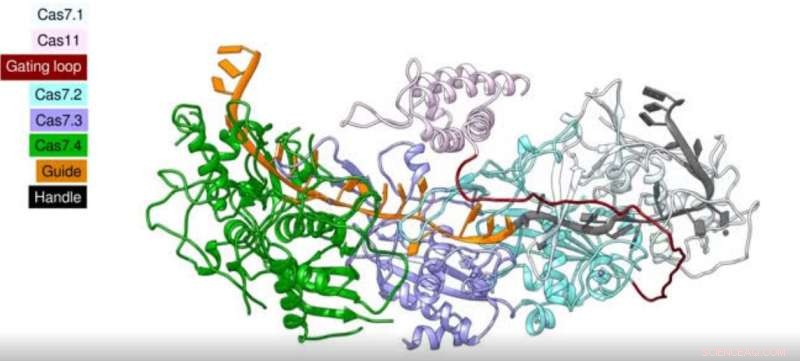
Crédit :Sciences (2022). DOI :10.1126/science.add5064
Une nouvelle recherche de Cornell offre un aperçu d'une gamme de systèmes CRISPR, qui pourraient conduire à des outils antiviraux et d'ingénierie tissulaire prometteurs chez les animaux et les plantes.
Les recherches d'Ailong Ke, professeur Robert J. Appel de biologie moléculaire et de génétique au Collège des arts et des sciences, et de Stan J.J. Brouns de l'Université de technologie de Delft aux Pays-Bas, se concentre sur un système Caspase guidé par l'ARN CRISPR récemment découvert, autrement connu sous le nom de Craspase.
Les systèmes CRISPR-Cas sont des nucléases guidées par l'ARN dans des bactéries qui clivent des cibles d'ADN ou d'ARN viral à des emplacements précis pour permettre de puissantes applications d'édition du génome. Les caspases sont une famille de protéases qui contrôlent la mort cellulaire programmée chez les animaux, y compris les humains. Une découverte récente selon laquelle des protéines de type caspase pourraient s'associer à CRISPR-Cas a électrisé la communauté scientifique. Ces caspases guidées par CRISPR ont reçu un nouveau nom, Craspase.
"D'une part, cette association était totalement inattendue et indique de nouveaux modes d'action antivirale chez les bactéries", a déclaré Ke. "D'un autre côté, nous pourrions utiliser un système comme celui-ci pour développer de nombreuses applications biotechnologiques et thérapeutiques, si nous comprenons tous les gadgets à l'intérieur de cette machinerie."
L'article des chercheurs sur le sujet, "Craspase est une protéase activée par l'ARN et guidée par l'ARN CRISPR", a été publié le 24 août dans Science . Pour cet article, les chercheurs ont utilisé des instantanés de cryo-microscopie électronique des systèmes Craspase pour expliquer comment ils se clivent pour cibler l'ARN et activer les enzymes protéases, qui peuvent décomposer les protéines.
"Ces instantanés conduisent à un film moléculaire haute définition", a déclaré Ke. "En le regardant dans les deux sens, nous savons précisément comment Craspase identifie une cible d'ARN, comment cela active à son tour la protéase, combien de temps l'activité persiste et ce qui finit par arrêter l'activité de la protéase. Les idées commencent à affluer, sur la façon de tirer le pouvoir de cette plate-forme."
Le co-premier auteur Chunyi Hu, associé postdoctoral dans le laboratoire de Ke, a déclaré que le système Craspase suscitait un énorme intérêt. "Beaucoup de concurrence. Nous et nos collaborateurs néerlandais avons uni nos forces et travaillé jour et nuit pour résoudre le puzzle", a déclaré Hu. "Le processus a un potentiel passionnant car le résultat de Craspase est une protéine plutôt qu'une dégradation de l'ADN."
"Avec d'autres technologies CRISPR, on se demande si les enzymes que nous utilisons pour modifier notre ADN sont suffisamment sûres, s'il pourrait y avoir des dommages collatéraux ou un ciblage", a déclaré Ke. "Avec Craspase, nous pouvons obtenir bon nombre des mêmes résultats thérapeutiques bénéfiques sans nous soucier de la sécurité de notre génome."
Les travaux rapportés dans l'article aident également les chercheurs à comprendre ce que Craspase fait à l'intérieur des cellules bactériennes, a déclaré Ke. "Les travaux de nos collaborateurs ont montré que c'est comme un interrupteur principal - le clivage protéolytique déclenche une cascade d'événements dans les cellules bactériennes qui finissent probablement par les tuer", a déclaré Ke. "Nous avons une réponse partielle dans cette étude. Nous enquêtons toujours."
Cette recherche récente aidera également les scientifiques à comprendre les similitudes entre la mort cellulaire programmée dans les voies cellulaires humaines et le même processus dans les voies cellulaires bactériennes.
"Nous réalisons que le même ensemble de protéases (caspases) contrôle les voies de mort cellulaire programmées dans les deux règnes de la vie", a déclaré Ke. "Cette observation a révélé à quel point cette voie est profondément enracinée."
En plus de sonder plus profondément le côté fonctionnel de ce processus, a déclaré Ke, l'équipe passera au côté application, qui pourrait inclure l'ingénierie tissulaire chez les animaux et le génie agricole. "J'espère que davantage d'enquêteurs apprécieront le potentiel de ce système et se joindront à nous", a déclaré Ke. "Nous pensons tous à la nucléase guidée par CRISPR comme un outil pour guérir les maladies génétiques, mais les protéases guidées par CRISPR pourraient avoir des impacts pour la biologie d'une manière beaucoup plus large." Discovery offre un point de départ pour de meilleurs outils d'édition de gènes