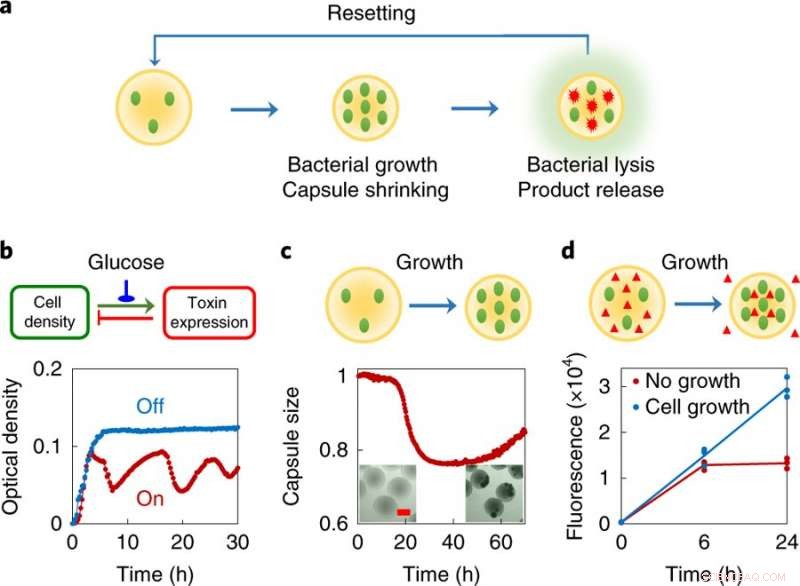
une, Concept design, chaque essaimbot se compose d'une petite population de bactéries modifiées encapsulées dans des microcapsules polymères. Ces bactéries sont conçues pour subir une lyse partielle à une densité locale suffisamment élevée. Inversement, le matériau d'encapsulation rétrécira en réponse à l'environnement chimique changeant provoqué par la croissance cellulaire. Comme les bactéries subissent une autolyse programmée, ils libèrent des protéines intracellulaires. Les capsules polymères réticulées piègent les cellules vivantes et les gros débris à l'intérieur, et le rétrécissement correspondant facilite l'exportation de produits protéiques à partir des capsules. Le système est réinitialisé en le remplissant de milieu frais. b, Lyse autonome programmée par le circuit ePop (en haut, logique de circuit ; bas, données expérimentales). Une augmentation dépendante de la densité du nombre de copies de plasmide conduit à une augmentation de l'expression d'une toxine (la protéine E du phage X174). A une concentration suffisamment élevée, la protéine E provoque la lyse cellulaire, entraînant une diminution de la densité cellulaire. Lorsqu'il est allumé (courbe rouge), le circuit a conduit à une densité de culture réduite de MC4100Z1 (ePop) équilibrée par la croissance et l'abattage régulé. Aux fins de la conception globale du système, la génération d'oscillations n'est pas indispensable. Le circuit peut être désactivé (courbe bleue) en ajoutant 1% de glucose. L'expérience a été répétée plus de trois fois indépendamment avec des résultats similaires. c, Rétrécissement des capsules en réponse à la croissance de bactéries encapsulées (en haut, schématique; bas, données expérimentales). Les cellules MC4100Z1 (ePop/GFP) ont été encapsulées dans des capsules de chitosane et cultivées dans M9. Toutes les données ont été normalisées à la valeur au temps zéro. Encart, images microscopiques de MSB après 0 h (à gauche) et 48 h (à droite). Barre d'échelle, 200 μm. L'expérience a été répétée plus de trois fois indépendamment avec des résultats similaires. ré, Le rétrécissement des capsules induit par la croissance facilite l'exportation des macromolécules des capsules (en haut, schématique; bas, données expérimentales). Cellules MG1655 et dextran–rhodamine (poids moléculaire ≈ 70, 000 g mol-1) ont été encapsulés dans les capsules de chitosane et cultivés en M9. Les gélules ont été traitées avec ou sans ampicilline (100 μg ml−1). Gélules rétractables, causée par la croissance bactérienne en l'absence d'antibiotiques, a conduit à une augmentation d'environ 2,25 fois de la fluorescence de la rhodamine par rapport aux capsules non rétractables après 24 h, qui contenait des bactéries non en croissance (supprimées par un antibiotique). L'expérience a été réalisée en triple sous forme de répliques biologiques indépendantes et les données sont présentées sous forme de points individuels, la ligne indique la moyenne. Crédit: Nature Chimie Biologie (2019). DOI :10.1038/s41589-019-0357-8
Les ingénieurs biomédicaux de l'Université Duke ont développé une nouvelle plate-forme pour créer des médicaments biologiques à l'aide de bactéries spécialement conçues qui éclatent et libèrent des protéines utiles lorsqu'ils sentent que leur capsule devient trop encombrée.
La plate-forme repose sur deux composants principaux :les bactéries modifiées, appelés "swarmbots, " qui sont programmés pour sentir la densité de leurs pairs dans leur conteneur, et le biomatériau qui confine les swarmbots, une capsule poreuse qui peut rétrécir en réponse aux changements de la population bactérienne. Quand il rétrécit, la capsule extrait les protéines ciblées créées par les bactéries captives.
Cette plateforme autonome pourrait permettre aux chercheurs de créer plus facilement, analyser et purifier divers produits biologiques à utiliser dans la bioproduction à petite échelle.
La recherche est apparue en ligne le 16 septembre dans le journal Nature Chimie Biologie .
Les bactéries sont couramment utilisées pour produire des produits biologiques, qui sont des produits comme les vaccins, thérapies géniques et protéines créées ou synthétisées à partir de sources biologiques. Actuellement, ce processus implique une série d'étapes sophistiquées comprenant la culture cellulaire, isolement de protéines et purification de protéines, dont chacun nécessite une infrastructure délicate pour assurer l'efficacité et la qualité. Pour les opérations industrielles, ces étapes sont réalisées à grande échelle. Bien que cela aide à produire de grandes quantités de certaines molécules, cette configuration n'est pas flexible ou financièrement viable lorsque les chercheurs doivent produire de petites quantités de produits biologiques divers ou travailler dans des environnements aux ressources limitées.
La nouvelle technologie a été développée par Lingchong You, professeur de génie biomédical à l'Université Duke, et un ancien chercheur postdoctoral Duke, Zhuojun Dai, maintenant professeur agrégé à l'Institut des technologies avancées de Shenzhen. Dans la nouvelle étude, ils montrent comment leur nouvelle plateforme utilise la communication entre les swarmbots et leur capsule pour réaliser une production polyvalente, analyse et purification de diverses protéines et complexes protéiques.
Dans une preuve de concept antérieure, Vous et son équipe avez conçu une souche non pathogène de la bactérie E. coli pour produire un antidote aux antibiotiques lorsque la bactérie a atteint une certaine densité. Ces essaimbots ont ensuite été confinés dans une capsule, qui a été baigné d'antibiotiques. Si une bactérie quittait la capsule, elle était détruite, mais s'il restait à l'intérieur du conteneur où la densité de population était élevée, il a survécu.
"Notre première étude a essentiellement montré une communication à sens unique, où les cellules pouvaient sentir l'environnement à l'intérieur de la capsule mais l'environnement ne réagissait pas aux cellules, " Tu as dit. " Maintenant, nous avons une communication bidirectionnelle - les essaimbots conçus peuvent toujours sentir leur densité et leur confinement, mais nous avons introduit un matériau qui peut réagir lorsque la population bactérienne à l'intérieur change. C'est comme si les deux composants se parlaient, et collectivement, ils vous donnent un comportement très dynamique."
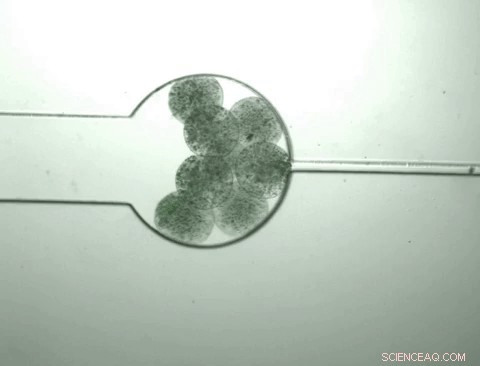
Des capsules contenant des bactéries sur mesure appelées "swarmbots" se développent et se rétrécissent en réponse à l'environnement chimique qu'elles contiennent. Les essaimbots sentent que leur propre densité de population a atteint un certain niveau et se sont ouverts pour libérer leur contenu, y compris une protéine qu'ils ont été conçus pour fabriquer. La capsule se rétrécit ensuite et le processus reprend lorsque les nutriments sont introduits. Crédit :Zhuojun Dai
Une fois que la population à l'intérieur de la capsule atteint une certaine densité, les bactéries commencent à éclater, ' libérant tout leur contenu cellulaire, y compris le produit protéique d'intérêt. À la fois, cette croissance bactérienne modifie l'environnement chimique au sein de la capsule, le faisant rétrécir. Au fur et à mesure qu'il rétrécit, il expulse la protéine libérée par les cellules éclatées tandis que les bactéries et les débris cellulaires sont conservés dans la capsule.
Une fois les protéines collectées, les chercheurs peuvent ajouter un réapprovisionnement en nutriments au plat pour inciter les capsules à s'agrandir. Cela réinitialise l'environnement intérieur et permet aux bactéries de recommencer à croître, recommencer le processus. Selon toi, ce cycle peut être répété jusqu'à une semaine.
Pour rendre la démarche utile pour la bioproduction, l'équipe a ajouté les capsules à une puce microfluidique, qui comprenait une chambre pour eux de détecter et de quantifier quelles protéines ont été libérées. Cela pourrait être remplacé par une chambre de purification pour préparer les protéines à utiliser dans les produits biologiques.
"C'est un processus très compact. Vous n'avez pas besoin d'électricité, et vous n'avez pas besoin d'une centrifugeuse pour produire et isoler ces protéines, " a déclaré You. " Cela en fait une bonne plate-forme pour la bioproduction. Vous avez la possibilité de produire un certain type de médicament dans un format très compact à faible coût, et c'est facile à livrer. En plus de ça, cette plate-forme offre un moyen simple de produire plusieurs protéines simultanément."
Selon toi, cette facilité d'utilisation a permis à l'équipe de produire, quantifier et purifier plus de 50 protéines différentes en collaboration avec le laboratoire d'Ashutoshi Chilkoti, Alan L. Kaganov Professeur et président du département de génie biomédical de Duke. Ils ont également exploré comment leur plateforme peut simplifier la création de complexes protéiques, qui sont des structures constituées de plusieurs protéines.
Dans le cadre d'une expérience de validation de principe visant à produire une voie de synthèse des acides gras à partir de plusieurs enzymes, "nous avons pu utiliser sept versions de nos swarmbots microbiens, dont chacun a été programmé pour produire une enzyme différente, " Tu as dit. " D'habitude, pour produire une voie métabolique, il faudrait équilibrer la chaîne d'approvisionnement, ce qui pourrait impliquer une régulation positive de l'expression d'une enzyme et une régulation négative de l'expression d'une autre. Avec notre plate-forme, vous n'avez pas besoin de faire cela, vous avez juste besoin de définir le bon ratio de swarmbots."
"Cette technologie est incroyablement polyvalente, " a-t-il dit. " C'est une capacité dont nous voulons profiter. "