Les aptamères, les biocapteurs basés sur l'acide nucléique capables de se lier à des protéines spécifiques ou à de petites molécules, offrent un moyen d'identifier des molécules cibles sans la complexité des appareils analytiques. Bien qu'ils soient de plus en plus utilisés dans des applications de diagnostic pour diverses maladies, leur potentiel en tant que capteurs efficaces pour le cancer est particulièrement remarquable, car la détection précoce du cancer peut conduire à un taux de guérison de plus de 90 %.
Cependant, les aptamères sont confrontés à des limites critiques car ils sont susceptibles d'être dégradés ou agrégés par des nucléases ou des protéines chargées présentes dans des échantillons biologiques tels que le sang ou la salive. Cela rend difficile leur utilisation directe dans des échantillons cliniques sans éliminer au préalable ces molécules. Récemment, une équipe de chercheurs de l'Université des sciences et technologies de Pohang (POSTECH) a résolu ce problème en utilisant une microcapsule à base de protéines.
L'équipe de recherche dirigée par les professeurs Seung Soo Oh et Sungwook Woo et Ph.D. le candidat Jinmin Kim du Département de science et d'ingénierie des matériaux de POSTECH a développé un système de capteur aptamère qui permet la détection rapide de molécules cibles directement à partir d'échantillons biologiques, éliminant ainsi le besoin de processus de prétraitement. Cette recherche a été publiée dans Biosensors and Bioelectronics .
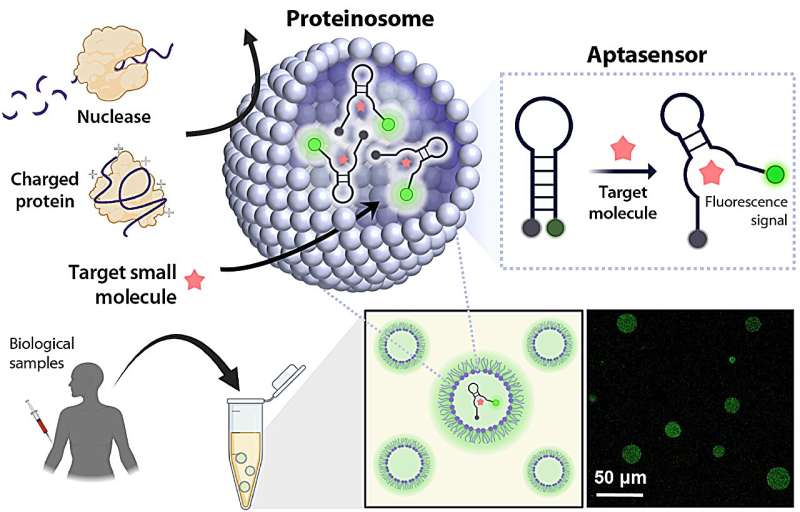
Dans cette recherche, l’équipe a créé des microcapsules sphériques appelées protéinosomes, basées sur l’auto-assemblage d’amphiphiles protéine-polymère. La microcapsule a été conçue pour contenir un aptasensor basé sur un aptamère à commutation de structure qui réagit avec les molécules cibles pour produire instantanément un signal fluorescent, et sa surface est composée d'une membrane semi-perméable sélective en taille qui ne laisse passer que les petites molécules cibles. tout en bloquant efficacement l'entrée de protéines nocives plus grosses.
Les résultats ont démontré que les performances optimales de l'aptasensor pour la détection de cibles étaient entièrement préservées même dans les biofluides non traités, permettant une détection efficace et rapide de molécules cibles telles que l'estradiol, une hormone féminine importante associée au cancer des organes reproducteurs, la dopamine, un neurotransmetteur. qui est révélateur des maladies de Parkinson ou d'Alzheimer, et de la cocaïne, une substance contrôlée qui nécessite souvent une détection rapide sur place.
Les capsules développées par les chercheurs ont démontré une protection robuste contre les protéines nocives.
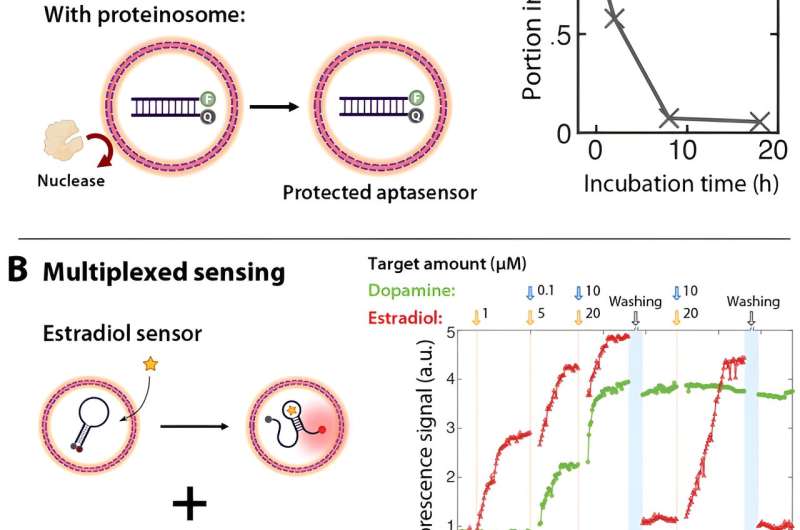
Par exemple, les aptasensors logés dans les microcapsules sont restés intacts pendant 18 heures dans des solutions de nucléases hautement concentrées, environ 300 000 fois le niveau sérique normal. De plus, en tirant parti de la propriété selon laquelle chaque capsule fonctionne comme un « récipient de réaction » indépendant, les chercheurs ont démontré le fonctionnement indépendant de plusieurs aptasenseurs dans le même mélange, permettant la détection simultanée en temps réel de plusieurs molécules cibles et la surveillance de leurs changements de concentration respectifs.
Le professeur Seung Soo Oh, qui a dirigé la recherche, a expliqué :« En intégrant la séparation des échantillons et la détection de cibles, nous avons mis au point une nouvelle technologie de biocapteur à petites molécules au point d'intervention qui est directement applicable aux échantillons biologiques tels que le sérum. révolutionner la médecine, allant de la détection précoce des maladies au traitement personnalisé."
doctorat Le candidat Jinmin Kim a déclaré :"La plate-forme de détection basée sur les protéinosomes est un système polyvalent car elle peut être étendue aux capteurs de diverses molécules cibles en changeant simplement l'aptasensor à l'intérieur."
Plus d'informations : Jinmin Kim et al, Protéinosomes semi-perméables encapsulant Aptasensor pour la détection directe de cibles dans les biofluides non traités, Biocapteurs et bioélectronique (2024). DOI :10.1016/j.bios.2024.116062
Fourni par l'Université des sciences et technologies de Pohang