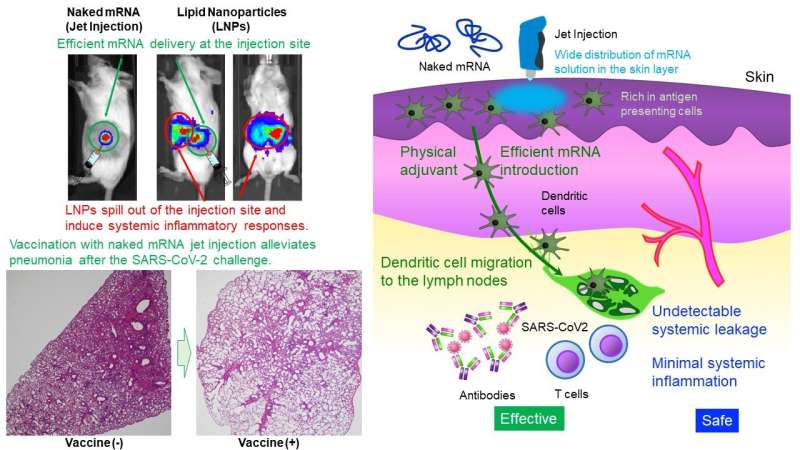
Le laboratoire Uchida du centre d'innovation de NanoMedicine a démontré que l'administration intradermique d'ARNm seul (ARNm nu) sans protection par des nanoparticules induisait une vaccination robuste contre le SRAS CoV-2, un virus provoquant le COVID-19, chez les souris et les primates. L'ARNm est très instable et nécessite généralement une minuscule capsule, telle que des nanoparticules lipidiques (LNP), pour son administration.
La méthode rapportée ici est le premier vaccin à ARNm nu démontrant une prévention contre le SRAS-CoV-2. Sans utiliser de LNP, qui sont très susceptibles de provoquer des événements indésirables systémiques, ce vaccin peut permettre des administrations répétées. Il est actuellement en cours de développement pour des essais cliniques. Les résultats détaillés de la recherche seront publiés dans Molecular Therapy .
Pendant la pandémie de COVID-19, les vaccins à ARNm ont démontré une efficacité exceptionnelle, avec des milliards de doses administrées dans le monde. Cependant, des défis sont apparus dans le cadre de leur développement rapide, notamment concernant les effets indésirables relativement forts, y compris les plus graves, qui restent des problèmes importants.
Bien que ces effets indésirables puissent être jugés acceptables pour un nombre limité de doses pendant une pandémie, une plateforme plus sûre permettant des doses multiples au cours d’une vie est souhaitable pour les rappels continus contre la COVID-19 et l’extension de l’application du vaccin à ARNm à d’autres maladies infectieuses. Les vaccins à ARNm actuels ont été associés à des effets indésirables, principalement attribués aux nanoparticules lipidiques (LNP) qui portent l'ARNm (ARNm enveloppé dans une enveloppe lipidique).
Les LNP possèdent des propriétés immunostimulatrices et peuvent déborder du site d’injection, entraînant des réponses inflammatoires systémiques. Néanmoins, les LNP jouent un rôle crucial dans l'efficacité du vaccin, comme la [Fonction I] empêchant la dégradation de l'ARNm et la délivrance efficace de l'ARNm dans les cellules, la [Fonction II] migrant vers les ganglions lymphatiques pour délivrer l'ARNm dans les cellules immunitaires et la [Fonction III] stimulant le système immunitaire. grâce aux lipides immunostimulateurs. La présente étude vise à obtenir ces fonctions sans recourir aux LNP.
Cette étude propose une conception simple et sûre, l'administration d'ARNm nu. Concernant la [Fonction II], peu de cellules immunitaires résident dans le tissu musculaire, un site d’administration actuel des vaccins à ARNm. Par conséquent, le tissu cutané, plus abondant en cellules immunitaires, a été ciblé.
De plus, pour la [Fonction I], l’équipe de recherche a utilisé un Jet Injector qui facilite l’administration d’ARNm aux cellules de la peau en utilisant le stress physique induit par le flux de jet. Dans une étude réalisée par un journaliste, Jet Injector a amélioré l'efficacité de l'administration de l'ARNm de plus de 100 fois par rapport à une injection conventionnelle avec aiguille et seringue. De plus, l'ARNm est resté au site d'injection sans fuite systémique détectable.

D’autre part, les LNP chargés d’ARNm (ARNm enveloppés dans une enveloppe lipidique) ont migré vers le foie, la rate et d’autres organes systémiques après administration intradermique, y provoquant des inflammations. De plus, l'inflammation au site d'injection était très mineure dans notre méthode, alors que l'ARNm enveloppé dans une enveloppe lipidique induisait une infiltration de cellules inflammatoires et une nécrose tissulaire.
Ensuite, l’équipe de recherche a d’abord démontré la capacité de vaccination de l’ARNm nu à l’aide d’un antigène modèle. L'injecteur à jet a considérablement amélioré l'efficacité de la production d'anticorps à un niveau comparable à celui de l'ARNm enveloppé dans une enveloppe lipidique aux doses maximales tolérables.
Ces anticorps combattent les virus présents dans l’organisme, prévenant ainsi l’infection, mais ils ne peuvent pas éliminer les cellules infectées. D’un autre côté, l’immunité cellulaire élimine ces cellules malades, jouant ainsi un rôle essentiel dans la prévention des maladies graves. Curieusement, le vaccin à ARNm nu augmente efficacement le nombre d'immunocytes, tels que les lymphocytes T CD4-positifs et les lymphocytes T CD8-positifs.
Ensuite, l’équipe de recherche a mené des expériences de provocation virale après la vaccination à ARNm nu ciblant la protéine de pointe du virus SARS-CoV-2. La vaccination a considérablement réduit la quantité de virus dans les poumons et atténué l’inflammation pulmonaire par rapport à un témoin non vacciné. Ce vaccin a fourni aux singes cynomolgus une efficacité vaccinale comparable à celle des souris sans effets indésirables significatifs.
La présente étude comprend également des analyses mécanistiques. Concernant la [Fonction II], le vaccin à ARNm nu est resté au site d’injection et n’a pas migré vers les ganglions lymphatiques. D'autre part, les cellules présentatrices d'antigène qui absorbaient l'ARNm au site d'injection ont migré vers les ganglions lymphatiques, ce qui peut contribuer à l'efficacité de la vaccination.
En effet, le vaccin a induit la maturation du ganglion lymphatique proche du site d’injection. Pour la [Fonction III], le Jet Injector a provoqué une inflammation transitoire localisée au site d'injection, recrutant des lymphocytes. L’injection d’ARNm nu à l’aiguille et à la seringue n’a pas induit une telle réponse inflammatoire. Ces résultats suggèrent que la stimulation immunitaire par Jet Injector peut fonctionner comme un adjuvant physique pour améliorer l'efficacité de la vaccination. Les réactions inflammatoires locales observées ont disparu en quelques jours.
En conclusion, le vaccin à ARNm nu réduit les effets indésirables systémiques, un problème lié à l’ARNm enveloppé dans une enveloppe lipidique, et induit une immunité suffisante pour la protection contre les maladies infectieuses. Il s’agit d’une avancée mondiale dans la prévention des maladies infectieuses grâce à l’ARNm seul. En pratique, ce vaccin pourrait devenir une plateforme permettant des administrations répétées avec des effets indésirables mineurs. D'autres études sont actuellement en cours, dans le but d'un essai clinique prévu pour 2026.
Plus d'informations : Saed Abbasi et al, Le vaccin à ARNm sans porteur induit une immunité robuste contre le SRAS CoV-2 chez les souris et les primates non humains sans réactogénicité systémique, Thérapie moléculaire (2024). DOI :10.1016/j.ymthe.2024.03.022
Informations sur le journal : Thérapie moléculaire
Fourni par le Centre d'Innovation de NanoMédecine