Les vaccins restent la référence en matière de protection contre les agents pathogènes dangereux, mais leur développement prend beaucoup de temps et de vastes ressources. Les virus à mutation rapide tels que le SRAS-CoV-2 peuvent atténuer leur efficacité et même les rendre obsolètes.
Pour combler ces lacunes, une équipe multi-universitaire dirigée par Vivek Kumar du New Jersey Institute of Technology développe une thérapie hydrogel qui agit comme une première ligne de défense contre les virus et autres menaces biologiques. Les peptides qui composent ce gel empêchent les virus tels que le SRAS-CoV-2, responsable du COVID-19, de se fixer et de pénétrer dans les cellules. Pour ce faire, ils se lient à un récepteur particulier de l'agent pathogène envahisseur tout en s'agrégeant dans un « masque moléculaire » multicouche qui atténue son action.
Au cours de leurs recherches, l’équipe a découvert que le masque moléculaire, à lui seul, prévenait les infections. L'avantage potentiel de cette nouvelle technologie, disent-ils, est sa capacité à combattre divers agents pathogènes et mutations de maladies.
"Il est important de protéger les personnes dès les premières phases d'une épidémie", a déclaré Kumar, professeur agrégé de génie biomédical. "Notre nouveau mécanisme pourrait également aider les premiers intervenants en première ligne, le personnel militaire confronté à de nouveaux agents pathogènes, les personnes vivant dans des zones reculées et sous-financées et celles qui ne peuvent pas se faire vacciner."
L'objectif à court terme est de produire un spray nasal contre les infections aéroportées.
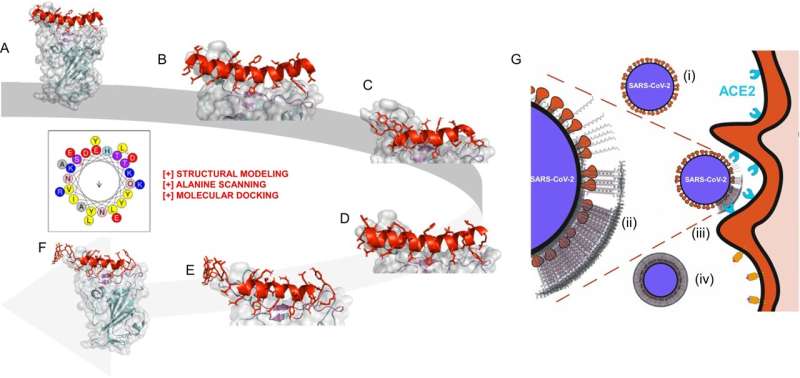
Dans une étude parue dans la revue Nature Communications , l'équipe a décrit comment le masque se lie de manière non spécifique à sa cible. Il est composé de peptides conçus par ordinateur (des chaînes d'acides aminés qui forment des protéines) qui s'auto-assemblent en hydrogels fibreux à l'échelle nanométrique. En comparaison, les anticorps produits par les vaccins ciblent des récepteurs particuliers, comme les vaccins à ARNm développés pendant la pandémie qui se lient à des protéines spécifiques sur le pic du SRAS-CoV-2.
La découverte de l'équipe est née de la recherche menée au début de la pandémie sur de nouvelles approches pour empêcher le virus d'envahir les cellules. La conception initiale, impliquant des peptides ciblant le pic du SRAS-CoV-2, a examiné des domaines hautement spécifiques. Cependant, les gels peptidiques non spécifiques qu'ils ont également conçus formaient une fibre multicouche au-dessus du virus.
Le groupe a postulé que les charges négatives dans les fibres interagissent avec des protéines chargées différemment à la surface du virus, les masquant et les empêchant ainsi d'interagir avec les cellules natives.

À propos du masque protéique non spécifique, Kumar a noté :« Il forme une structure plus grande et se lie mieux qu'une seule molécule. Bien qu'il n'ait pas une spécificité élevée, il peut s'auto-assembler et rester sur la cible plus longtemps, formant une fibre. autocollant sur la surface qui agit comme du Velcro moléculaire."
Il a ajouté :"L'objectif serait d'obtenir un agent topique qui se lie au virus. Dans le cas du SRAS-CoV-2, nous le pulvériserions dans le nez, qui est un site majeur d'infection, peut-être même à titre prophylactique."
L’équipe a d’abord testé les fibres contre un certain nombre de virus via des simulations informatiques utilisant de puissantes cartes graphiques NVIDIA, couramment utilisées dans les jeux compétitifs. Ils ont ensuite mené avec succès des tests de sécurité sur des souris et des rats, en utilisant des injections et des sprays nasaux, a déclaré Joseph Dodd-o, titulaire d'un doctorat. étudiant du laboratoire de Kumar qui a mené une grande partie des recherches sur la thérapie avec Abhishek Roy, également titulaire d'un doctorat. étudiant. La thérapie a inhibé les variantes alpha et omicrons du SRAS-CoV-2 in vitro, pendant une journée sans nuire aux animaux lors des tests in vivo.
Kumar a développé des hydrogels pour un certain nombre d'applications thérapeutiques. Son mécanisme de distribution est personnalisable et composé de brins de peptides de type Lego avec un agent bioactif attaché à une extrémité qui peut survivre dans le corps pendant des semaines, voire des mois, là où d'autres biomatériaux se dégradent rapidement. Ses liens d'auto-assemblage sont conçus pour être plus forts que les forces de dispersion du corps ; il forme des fibres stables, sans aucun signe d'induction d'inflammation.
L'hydrogel est conçu pour déclencher différentes réponses biologiques en fonction de la charge utile attachée. Le laboratoire de Kumar a publié des recherches sur des applications allant des thérapies visant à provoquer ou empêcher la création de nouveaux réseaux de vaisseaux sanguins, à réduire l'inflammation et à combattre les microbes.
"Dans ce cas, nous utilisons des charges électriques qui interagissent avec l'agent pathogène pour le perturber", a expliqué Kumar.
« Nous essayons toujours de déterminer comment les fibres interagissent :s'agit-il d'un mode d'action mécanique ? Les agents pathogènes résistants aux médicaments mutent autour de modulateurs biochimiques, mais sont-ils moins susceptibles de muter autour d'une lance mécanique ? En comprenant cette interaction fondamentale, nous voulons découvrez comment l'utiliser contre différentes maladies."
Dans le cadre de nouvelles études, le laboratoire teste la thérapie contre les bactéries et les champignons résistants aux médicaments.
Les membres de l'équipe apportent une expertise variée :conception informatique à l'Université de l'Illinois à Chicago ; capacités bioanalytiques de Georgia Tech et de la Baylor School of Medicine ; études de virologie à l'Université Rutgers ; et expérience en matière de plate-forme, d'analyse et d'essai au NJIT.
Plus d'informations : Joseph Dodd-o et al, Fibrilles antivirales de peptides auto-assemblés avec des compositions accordables, Nature Communications (2024). DOI :10.1038/s41467-024-45193-3
Informations sur le journal : Communications naturelles
Fourni par l'Institut de technologie du New Jersey