
Image des implants chirurgicaux, recouvert de nanoparticules d'or (tas de mailles à gauche) par rapport aux mailles chirurgicales d'origine antérieures au traitement (tas de mailles à droite). Crédit :ICFO
Inventé il y a environ 50 ans, les mailles médicales chirurgicales sont devenues des éléments clés dans les procédures de récupération des chirurgies des tissus endommagés, le plus fréquent étant la réparation d'une hernie. Lorsqu'il est implanté dans les tissus du patient, la conception flexible et conformable de ces mailles aide à maintenir les muscles serrés et permet aux patients de récupérer beaucoup plus rapidement qu'avec la chirurgie conventionnelle de semis et de couture.
Cependant, l'insertion d'un implant médical dans le corps d'un patient s'accompagne d'un risque de contamination bactérienne pendant la chirurgie et de formation subséquente d'un biofilm infectieux sur la surface du treillis chirurgical. De tels biofilms ont tendance à agir comme un revêtement imperméable, empêchant toute sorte d'agent antibiotique d'atteindre et d'attaquer les bactéries formées sur le film afin d'arrêter l'infection. Ainsi, antibiothérapies, qui sont limités dans le temps, pourrait échouer contre ces bactéries super résistantes et le patient pourrait se retrouver dans des chirurgies récurrentes qui pourraient même entraîner la mort. En réalité, selon le Réseau européen de surveillance de la résistance aux antimicrobiens (EARS-Net), en 2015 plus de 30, 000 décès en Europe étaient liés à des infections par des bactéries résistantes aux antibiotiques.
Autrefois, plusieurs approches ont été recherchées pour éviter la contamination des implants pendant la chirurgie. Des protocoles aseptiques post-opératoires ont été établis et mis en œuvre pour lutter contre ces bactéries résistantes aux antibiotiques, mais aucun n'a entièrement rempli le rôle de résoudre ce problème.
Dans une étude récente publiée dans Lettres nano et mis en évidence dans Photonique de la nature , Chercheurs ICFO Dr. Ignacio de Miguel, Arantxa Albornoz, dirigé par ICREA Prof. à ICFO Romain Quidant, en collaboration avec les chercheurs Irene Prieto, Dr Vanesa Sanz, Dr Christine Weis et Dr Pau Turon de la grande entreprise de dispositifs médicaux et de dispositifs pharmaceutiques B. Braun, ont mis au point une nouvelle technique qui utilise la nanotechnologie et la photonique pour améliorer considérablement les performances des treillis médicaux pour les implants chirurgicaux.
Grâce à une collaboration continue depuis 2012, l'équipe de chercheurs de l'ICFO et de B. Braun Surgical, S.A., a développé un maillage médical avec une particularité :la surface du maillage a été chimiquement modifiée pour ancrer des millions de nanoparticules d'or. Pourquoi? Parce qu'il a été prouvé que les nanoparticules d'or convertissent très efficacement la lumière en chaleur dans des régions très localisées.

Micrographies SEM de la S. aureus biofilm formé sur la surface du treillis chirurgical. Crédit :ICFO
La technique d'utilisation des nanoparticules d'or dans les processus de conversion lumière-chaleur avait déjà été testée dans des traitements anticancéreux dans des études précédentes. Encore plus, à ICFO, cette technique avait été mise en œuvre dans plusieurs études antérieures soutenues par la Fondation Cellex, étant ainsi un autre exemple frappant de la façon dont le soutien philanthropique visionnaire précoce destiné à résoudre des problèmes fondamentaux conduit finalement à d'importantes applications pratiques. Pour ce cas particulier, en sachant que plus de 20 millions d'opérations de réparation de hernies ont lieu chaque année dans le monde, ils pensaient que cette méthode pourrait réduire les coûts médicaux des opérations récurrentes tout en éliminant les traitements antibiotiques coûteux et inefficaces qui sont actuellement utilisés pour résoudre ce problème.
Ainsi, dans leur expérience in vitro et à travers un processus minutieux, l'équipe a recouvert le treillis chirurgical de millions de nanoparticules d'or, en les répartissant uniformément sur toute la structure. Ils ont testé les mailles pour s'assurer de la stabilité à long terme des particules, la non-dégradation du matériau, et le non-détachement ou libération de nanoparticules dans le milieu environnant (flacon). Ils ont pu observer une répartition homogène des nanoparticules sur la structure à l'aide d'un microscope électronique à balayage.
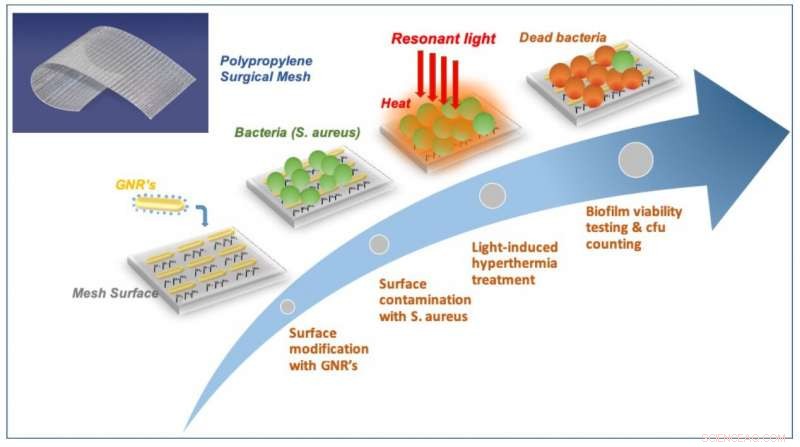
Vue schématique de la prévention des biofilms par plasmon sur les filets chirurgicaux. Crédit :ICFO
Une fois le maillage modifié prêt, l'équipe l'a exposé à des bactéries S.aureus pendant 24 heures jusqu'à ce qu'ils observent la formation d'un biofilm à la surface. Ensuite, ils ont commencé à exposer le maillage à de courtes impulsions intenses de lumière proche infrarouge (800 nm) pendant 30 secondes pour s'assurer que l'équilibre thermique était atteint, avant de répéter ce traitement 20 fois avec 4 secondes d'intervalles de repos entre chaque impulsion. Ils ont découvert ce qui suit :Premièrement, ils ont vu que l'éclairage du maillage à la fréquence spécifique induirait des résonances plasmoniques de surface localisées dans les nanoparticules - un mode qui entraîne une conversion efficace de la lumière en chaleur, brûler les bactéries à la surface. Deuxièmement, en utilisant un microscope confocal à fluorescence, ils ont vu combien de bactéries étaient mortes ou étaient encore en vie. Pour les bactéries qui sont restées vivantes, ils ont observé que les bactéries du biofilm devenaient des cellules planctoniques, récupérer leur sensibilité ou leur faiblesse à l'antibiothérapie et à la réponse du système immunitaire. Pour les bactéries mortes, ils ont observé qu'en augmentant la quantité de lumière délivrée à la surface du maillage, les bactéries perdraient leur adhérence et se décolleraient de la surface. Troisièmement, ils ont confirmé que le fonctionnement à des gammes de lumière proche infrarouge était complètement compatible avec les paramètres in-vivo, ce qui signifie qu'une telle technique n'endommagerait probablement pas les tissus sains environnants. Finalement, ils ont répété le traitement et ont confirmé que le chauffage récurrent du treillis n'avait pas affecté ses capacités d'efficacité de conversion.
Comme le commente le professeur ICREA à ICFO Romain Quidant, « les résultats de cette étude ont ouvert la voie à l'utilisation des nanotechnologies plasmoniques pour empêcher la formation de biofilm bactérien à la surface des implants chirurgicaux. Il reste encore plusieurs problèmes à résoudre mais il est important de souligner qu'une telle technique signifie un changement radical dans les procédures opératoires et un nouveau rétablissement du patient après la guérison."
Dr Pau Turon, Directeur Recherche et Développement chez B. Braun Surgical, S.A. explique, « notre engagement à aider les professionnels de la santé à éviter les infections nosocomiales nous pousse à développer de nouvelles stratégies pour lutter contre les bactéries et les biofilms. De plus, l'équipe de recherche envisage d'étendre cette technologie à d'autres secteurs où les biofilms doivent être évités."