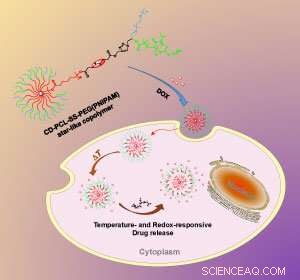
Le changement de température et d'environnement chimique à l'intérieur de la cellule déclenche la libération par la nanoparticule de sa charge utile de médicament. Crédit :La Société royale de chimie
Les chercheurs d'A*STAR ont développé des particules d'administration de médicaments à l'échelle nanométrique qui peuvent détecter leur environnement, et ne libèrent leur charge utile qu'après être entrés dans une cellule, une découverte qui pourrait rendre de nombreux médicaments existants plus efficaces.
Les nouvelles nanoparticules, développé par Zibiao Li de l'Institut de recherche et d'ingénierie des matériaux A*STAR et ses collaborateurs, sont une amélioration significative par rapport aux générations précédentes de nanoparticules d'administration de médicaments à base de polymères. Les premiers exemples consistaient généralement en de simples chaînes polymères avec une tête hydrophile et apolaire, queue hydrophobe. Dans l'eau, ces chaînes s'agrègent naturellement en sphères, avec leurs queues hydrophobes pointant toutes vers l'intérieur pour former un noyau non polaire. Le noyau a formé un bon site pour que les molécules de médicament se nichent. Dans la circulation sanguine, cependant, ces agrégats ont tendance à se déchirer.
Li et ses collègues ont utilisé les dernières techniques de synthèse de polymères pour créer des nanoparticules à molécule unique. Plutôt qu'un agrégat auto-assemblé de polymères séparés, l'équipe a synthétisé une structure plus robuste dans laquelle les chaînes polymères étaient fortement liées de manière covalente à un noyau central. La synthèse a commencé avec la bêta-cyclodextrine, une molécule de sucre circulaire avec 21 groupes hydroxyle à sa surface. Les groupes hydroxyle ont formé les ancres chimiques à partir desquelles l'équipe a construit le multiple long, en forme de Y, bras polymères multifonctionnels.
"Le plus grand défi dans la fabrication de la [nanoparticule] était d'intégrer différentes méthodologies de synthèse dans une conception macromoléculaire, " dit Li. A l'une des extrémités de chaque branche en forme de Y, l'équipe a attaché un polymère sensible à la température appelé PNIPAM. A température ambiante, le polymère PNIPAM s'étend vers l'extérieur, mais s'effondre une fois la température corporelle, 37 degrés Celsius, est atteint, permettant à la cargaison de molécules médicamenteuses de la nanoparticule de s'échapper.
A mi-chemin le long de chaque bras polymère, l'équipe a installé une liaison soufre-soufre. Lorsque les particules pénètrent dans une cellule, ils rencontrent des niveaux élevés de glutathion, une molécule qui clive les liaisons soufre-soufre. Ainsi, la couche extérieure de polymère de la nanoparticule est coupée, et le médicament est libéré encore plus rapidement.
Lorsque l'équipe a testé cet effet avec un médicament anticancéreux appelé doxorubicine, l'effet double action était clair. "Le passage de la température ambiante à la température corporelle, et l'effet du glutathion, a montré une libération synergique et rapide du médicament, " dit Li. À des températures plus basses, ou en l'absence de glutathion, la libération du médicament était significativement plus lente, il dit.
"Le prochain plan est d'intégrer de nouvelles fonctionnalités, pour la libération de précision du médicament pour le traitement ciblé du cancer, " dit Li. Une extrémité de chaque branche en forme de Y pourrait être fonctionnalisée avec une molécule qui adhère sélectivement aux cellules cancéreuses, délivrer le médicament précisément là où il est nécessaire.