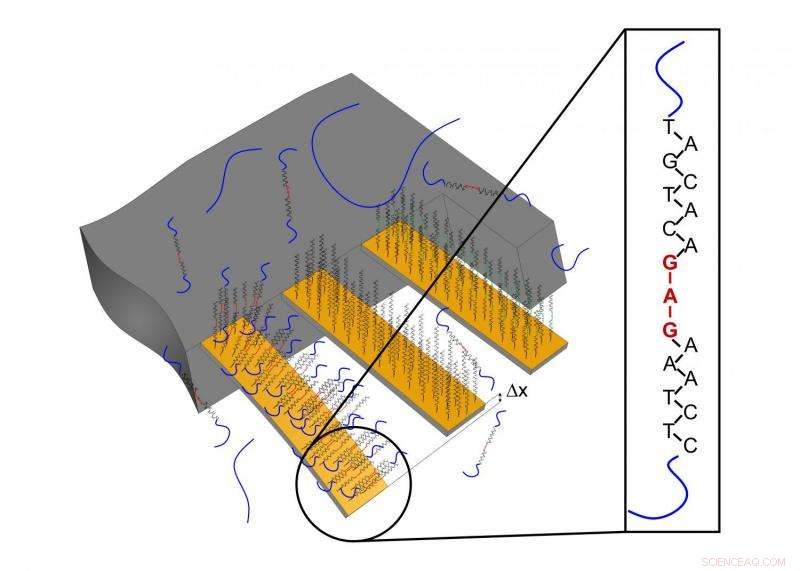
Le cantilever de gauche porte la séquence de reconnaissance de la mutation cible. S'il est présent dans l'échantillon testé, le segment d'ARN correspondant se lie au cantilever, faisant plier ce dernier. Cela peut être mesuré, fournissant des preuves claires que le changement génétique est présent. Crédit :Université de Bâle, Département de physique
Les changements dans la constitution génétique des échantillons de tissus peuvent être détectés rapidement et facilement à l'aide d'une nouvelle méthode basée sur la nanotechnologie. Ce rapport des chercheurs de l'Institut suisse des nanosciences, l'Université de Bâle et l'Hôpital universitaire de Bâle dans les premiers tests cliniques avec des mutations génétiques chez des patients atteints de mélanome malin. Le journal Lettres nano a publié l'étude.
Selon les estimations de l'American Skin Cancer Foundation, aujourd'hui, plus de personnes développent un cancer de la peau que du sein, prostate, cancer du poumon et du côlon ensemble. Bien que le mélanome malin ne représente qu'environ 5 % des cancers de la peau, ce sont les cas les plus graves et peuvent entraîner la mort. Environ la moitié de tous les patients qui développent un mélanome malin présentent un changement génétique particulier (mutation). Il s'agit d'une modification du gène BRAF (gène B pour Rapid Acceleration of Fibrosarcoma) qui conduit à une prolifération cellulaire incontrôlée.
Il existe désormais des médicaments qui exploitent ces mutations spécifiques et combattent le cancer, allongeant considérablement l'espérance de vie des patients. Cependant, ils ne fonctionnent que si la mutation génétique correspondante est effectivement présente. Là où il n'y en a pas, ils donnent lieu à des effets secondaires graves sans produire l'effet désiré. « Il est donc essentiel que nous puissions identifier les mutations de manière fiable dans les échantillons de tissus. C'est le seul moyen de garantir que les patients reçoivent le bon traitement et des résultats positifs. " explique le co-auteur de l'article, Professeur Katharina Glatz de l'Institut de pathologie de l'Hôpital universitaire de Bâle.
Micro porte-à-faux revêtus
Dans une étude clinique pilote, l'équipe dirigée par le professeur Ernst Meyer et le professeur Christoph Gerber de l'Institut suisse des nanosciences et du Département de physique de l'Université de Bâle a utilisé pour la première fois des nanocapteurs pour détecter les mutations dans des échantillons de tissus de patients atteints de mélanome malin. Faire cela, les chercheurs ont utilisé de minuscules porte-à-faux revêtus de différentes manières. Certains d'entre eux portaient une séquence de reconnaissance de la mutation que les chercheurs ciblaient.
Ensuite, le matériel génétique (ARN) des échantillons de tissus des patients a été isolé et appliqué aux cantilevers. Si le changement génétique est présent, l'ARN du patient se lie à la séquence de reconnaissance sur le cantilever. La contrainte de surface résultante entraîne une flexion du porte-à-faux, qui peut être mesuré. Si la mutation est absente de l'échantillon d'ARN, cette flexion ne se produit pas - en d'autres termes, seule une liaison spécifique produit un signal. L'avantage d'utiliser des nanocantilever est qu'aucune procédure fastidieuse n'est nécessaire. Il faut moins d'une journée pour passer de la biopsie au diagnostic.
Impensable il y a 30 ans
Dans cette étude, l'équipe de recherche de Bâle a pu démontrer que les micro-cantilevers nanomécaniques peuvent identifier des mutations dans des mélanges complexes d'ARN total isolés à partir d'échantillons de tissus. En premier, les cantilevers n'étaient utilisés que dans les microscopes à force atomique. Le professeur Christoph Gerber – qui doit recevoir le prix Kavli à Oslo le 6 septembre, avec Gerd Binnig et Cal Quate, pour le développement du microscope à force atomique – observe :« Il y a trente ans, nous n'étions pas en mesure de prévoir que notre technologie pourrait un jour être utilisée à l'hôpital pour une médecine personnalisée - "de la paillasse au chevet, ' comme c'était."