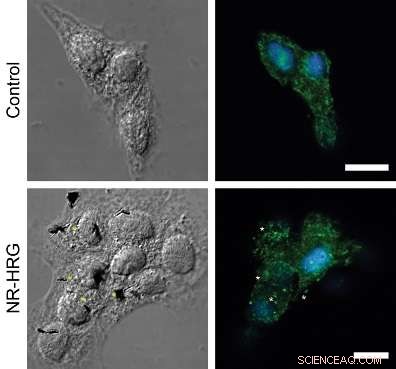
Figure :Regroupement des récepteurs ErbB2 lors de la liaison HRG-nanorod aux cellules MCF7. Micrographies confocales montrant une section dorsale de cellules MCF7 ciblées (panneau inférieur) et non ciblées (panneau supérieur). Les récepteurs ErbB2 (vert) ont été immunocolorés sans perméabiliser la membrane plasmatique. Les noyaux ont été colorés avec Hoechst 33342 (bleu). Les étoiles indiquent des exemples de clusters de récepteurs ErbB2 qui sont à proximité des nanotiges.
Des chercheurs de l'UCD ont manipulé avec succès des nanoparticules pour cibler deux lignées cellulaires de cancer du sein humain en tant qu'outil de diagnostic et de traitement du cancer.
L'enrobage des nanoparticules avec différentes substances permet d'ajuster leur interaction avec les cellules d'une manière particulière. Par exemple, l'utilisation d'une particule optiquement active comme l'or (Au) fournira un excellent contraste dans l'imagerie proche infrarouge (NIR) et, si chauffé, peut effectivement détruire les tissus environnants. C'est ce qu'on appelle la thérapie d'ablation photothermique. Les particules magnétiquement actives comme le fer (Fe) peuvent permettre des thérapies physiques en générant de la chaleur lorsqu'elles sont exposées à des champs magnétiques alternatifs provoquant la mort cellulaire (hyperthermie magnétique).
L'équipe UCD dirigée par Conway Fellows, Le professeur Gil Lee de la School of Chemistry and Chemical Biology et le professeur Walter Kolch de la Systems Biology Ireland, nanotiges synthétisées avec un long segment de fer recouvert de polyéthylène glycol et une courte pointe d'or recouverte d'une seule couche de la protéine, héréguline (HRG).
HRG est un facteur de croissance qui se lie à et active la famille ErbB de récepteurs protéiques. ErbB2 est surexprimé dans certains cancers du sein et lié à un mauvais pronostic. Cependant, La surexpression d'ErbB2 entraîne une sensibilité accrue à certains médicaments. L'équipe pense que les nanotiges fonctionnalisées Fe-Au utilisées conjointement avec ces médicaments pourraient être utiles dans le traitement du cancer.
Après avoir caractérisé et ajusté l'interaction des nanotiges avec les cellules, l'équipe de recherche a évalué comment les cellules réagissent à la stimulation mécanique. Pour faire ça, ils ont intégré une pince électromagnétique à un microscope optique et utilisé une nouvelle puce microfluidique pour surveiller l'interaction de nanotiges individuelles avec deux lignées cellulaires de cancer du sein humain qui expriment la famille de récepteurs ErbB à des vitesses différentes. Lorsque les nanotiges HRG se lient aux cellules cancéreuses exprimant ErbB, ils déclenchent une cascade d'événements de signalisation qui conduisent à la mort cellulaire.
"En utilisant des pincettes magnétiques pour étirer les cellules, nous avons pu activer davantage les voies de signalisation cellulaire pour déclencher la mort cellulaire. C'était encore plus efficace pour provoquer la mort des cellules cancéreuses que l'hyperthermie magnétique, l'autre approche thérapeutique que nous avons évaluée », a expliqué le Dr Devrim Kilinc, premier auteur et chercheur dans le groupe Lee.
"Les résultats sont une indication positive pour le ciblage à l'échelle nanométrique et la manipulation localisée des cellules cancéreuses avec un profil de récepteur spécifique."