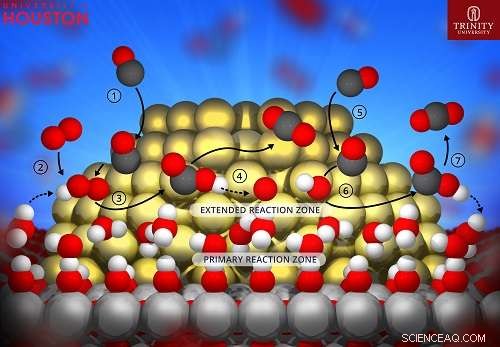
Représentation schématique de la voie d'énergie la plus basse pour l'oxydation du CO sur des catalyseurs or-oxyde de titane. La couche d'eau sur le support d'oxyde de titane étend la zone de réaction sur le nanocluster d'or et fournit des protons qui aident à l'étape de dissociation de l'oxygène. Crédit :Hieu Doan, Université de Houston
Des chercheurs de l'Université de Houston et de l'Université Trinity ont pour la première fois fourni des preuves directes d'un mécanisme de réaction à médiation par l'eau pour l'oxydation catalytique du monoxyde de carbone.
Les travaux ont utilisé des nanoparticules d'or et du dioxyde de titane comme catalyseur pour accélérer le processus et ont déterminé que l'eau sert de co-catalyseur pour la réaction qui transforme le monoxyde de carbone en dioxyde de carbone. Alors que les chercheurs travaillent depuis des années sur l'oxydation du monoxyde de carbone à l'aide de catalyseurs à l'or et se rendent compte que l'eau peut modifier la réaction, aucun n'a été en mesure d'expliquer pleinement pourquoi cela a fonctionné.
Le travail est décrit dans l'édition du 5 septembre de la revue Science .
"Nous pouvons dire avec un haut degré de certitude que nous comprenons maintenant le rôle de chacun des composants et ce qu'ils font au cours de cette réaction catalytique, " dit Lars Grabow, professeur adjoint de génie chimique et biomoléculaire à l'Université de Houston. Lui et Hieu Doan, un doctorat étudiant à l'UH Cullen College of Engineering, développé des simulations informatiques pour soutenir les expériences menées par les chimistes de l'Université Trinity Bert Chandler, Christopher Pursell et Johnny Saavedra.
Chandler, professeur de chimie à Trinity, a déclaré que le travail était une véritable collaboration.
"Il nous a fallu tous pour y arriver, " a-t-il dit. " Ce que nous avons fait, c'est combler le fossé entre la science des surfaces et les informaticiens. Nous savions que l'eau aidait à la réaction mais ne comprenions pas pleinement son rôle. Nous savons maintenant que l'eau est un co-catalyseur de cette réaction."
Lorsqu'il est utilisé en bijouterie, l'or est apprécié pour ses propriétés non réactives – il ne rouille pas et ne ternit pas lorsqu'il est exposé à l'air ou à l'eau. Et les chercheurs savent depuis longtemps que, malgré sa réputation de métal inerte, les nanoparticules d'or peuvent fonctionner comme un catalyseur pour accélérer la réaction chimique.
Mais personne ne savait exactement pourquoi cela fonctionnait. L'eau s'est avérée être la clé, même lorsqu'il n'est pas explicitement ajouté au processus, dit Grabow.
Des quantités infimes d'eau extraite de l'air ont entraîné les réactions à la surface des catalyseurs à l'or, il a dit.
Au cours des expériences et de l'étude informatique, les chercheurs ont examiné comment l'eau, les hydroxyles de surface et l'interface métal-support ont interagi pendant l'oxydation du monoxyde de carbone sur un catalyseur or-oxyde de titane.
"Dans tous les cas, un transfert de protons essentiellement sans barrière a abaissé l'énergie globale du système, générer H2O2 ou OOH. Une fois OOH formé, il a migré le long de la particule Au, permettant aux atomes de s'approcher, mais pas strictement à, l'interface métal-support pour participer à la réaction, " ils ont écrit pour décrire leurs découvertes, se référant à la génération de peroxyde d'hydrogène ou à la migration d'hydroperoxyle et d'hydroperoxyle le long des particules d'or.
Essentiellement, ils ont découvert que les protons d'une fine couche d'eau s'étendant sur la surface du catalyseur se détachent des molécules d'eau et se fixent aux molécules d'oxygène, se déplaçant brièvement sur la surface du catalyseur pour stimuler la réaction avant de retourner à la couche d'eau.
Les modèles précédents se concentraient généralement sur les composants individuels de la réaction, Grabow a dit, faisant de ce projet le premier à rassembler toutes les facettes dans un modèle unique qui prend pleinement en charge les observations expérimentales des chimistes de Trinity. Chandler a déclaré que les travaux pourraient fournir un moyen de produire de l'hydrogène propre à partir du pétrole et du gaz naturel.