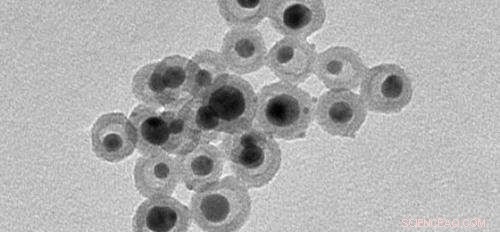
Des chimistes soutenus par le Fonds national suisse de la recherche scientifique (FNS) ont mis au point un procédé de synthèse en un seul pot pour encapsuler des nanoparticules. Ce type de particule pourrait améliorer le revêtement antimicrobien des implants.
Les populations occidentales vivent plus longtemps tout en bénéficiant d'une bonne santé. De plus en plus de monde, par exemple les jeunes retraités, se faire poser des implants pour poursuivre leurs activités. Mais une telle chirurgie n'est pas sans risques :lors d'une opération, les bactéries peuvent atteindre la surface de l'implant. Une fois qu'ils ont colonisé la surface et formé un biofilm, l'implant doit être retiré et la plaie nettoyée. Aucun nouvel implant ne peut être posé tant que l'infection n'a pas complètement disparu. Ces complications touchent 2% des articulations artificielles de la hanche, 5 à 10 % d'articulations artificielles du genou et atteindre 50 % pour les opérations de dérivation cardiaque et de stent.
Une façon de lutter contre la croissance des bactéries à la surface de l'implant est l'ajout d'un revêtement antimicrobien. Un groupe de recherche, dirigé par Katharina Fromm de l'Université de Fribourg, a développé un tel revêtement. Il fait actuellement l'objet de tests in-vivo dans le cadre d'un projet financé par la CTI. Ce revêtement émet en permanence un agent antimicrobien - des ions d'argent - pendant une durée d'environ trois mois.
Revêtement avec effet plus long
Pour prolonger l'efficacité du revêtement, les chercheurs travaillent actuellement sur un revêtement de deuxième génération dans lequel la nanoparticule d'argent serait encapsulée dans de la silice. Cela permettrait d'améliorer la stabilité de la nanoparticule en l'isolant de son environnement. Cela ralentirait également la diffusion de l'argent et prolongerait l'efficacité du revêtement. Un autre avantage de cette méthode est que les cellules peuvent tolérer un nombre beaucoup plus important de nanoparticules d'argent si elles sont encapsulées que si elles sont nues.
À cette fin, les chercheurs ont développé, dans le cadre du Programme National de Recherche "Matériaux Intelligents" (PNR 62), un procédé de synthèse en un seul pot (*) pour encapsuler les nanoparticules. Cela leur permet de déterminer la porosité et la taille du conteneur de silice par rapport à la nanoparticule qu'il contient. Sous le microscope, il ressemble à un hochet nanoscopique.
Libération ciblée
Pour améliorer encore les performances du revêtement, les chercheurs - en collaboration avec l'équipe du Pr Christian Bochet - travaillent également sur des capteurs bactériens qu'ils visent à fixer sur les nanoparticules encapsulées. Si un tel capteur était en place, l'argent ne serait libéré que si un agent pathogène se trouvait à proximité. Cette libération ciblée prolongerait encore l'efficacité de la protection et empêcherait l'argent d'être libéré inutilement dans l'organisme.
La synthèse développée par les chercheurs permet le développement de différents types de conteneurs pour diverses nanoparticules. Le potentiel applicatif de ces nano-hochets est donc considérable :en contrôlant la porosité du contenant, il est par exemple possible de contrôler quelles molécules peuvent s'approcher des nanoparticules. Cette, à son tour, permettrait de créer un nanoréacteur dans lequel une réaction chimique peut avoir lieu. La technique pourrait également permettre de nouvelles conceptions de batteries dans lesquelles chaque nanoparticule encapsulée jouerait le rôle d'une électrode.