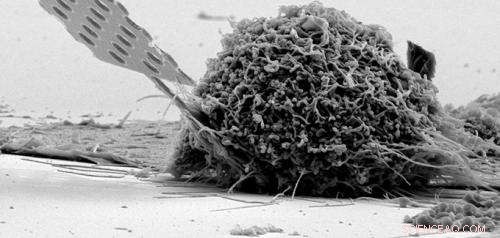
Cette image au microscope électronique à balayage (MEB) montre une sonde à nanofaisceau, comprenant une grande partie de la pointe du manche, inséré dans une cellule typique. Crédit :Gary Shambat, École d'ingénierie de l'Université de Stanford
Si les ingénieurs de Stanford réussissent, la recherche biologique pourrait bientôt être transformée par une nouvelle classe de sondes électroluminescentes suffisamment petites pour être injectées dans des cellules individuelles sans nuire à l'hôte. Bienvenue dans la biophotonique, une discipline au confluent de l'ingénierie, la biologie et la médecine dans lesquelles les dispositifs basés sur la lumière – lasers et diodes électroluminescentes (LED) – ouvrent de nouvelles voies dans l'étude et l'influence des cellules vivantes.
L'équipe a décrit leur sonde dans un article publié en ligne le 13 février par le journal Lettres nano . C'est la première étude à démontrer que des résonateurs de lumière sophistiqués peuvent être insérés à l'intérieur des cellules sans endommager la cellule. Même avec un résonateur intégré à l'intérieur, une cellule est capable de fonctionner, migrer et se reproduire normalement.
Applications et implications
Les chercheurs appellent leur appareil un « nanofaisceau, " parce qu'elle ressemble à une poutre en I en acier avec une série de trous ronds gravés au centre. Ces poutres, cependant, ne sont pas massifs, mais ne mesurent que quelques microns de longueur et quelques centaines de nanomètres de largeur et d'épaisseur. Cela ressemble un peu à une pièce d'un ancien ensemble de monteurs. Les trous à travers les faisceaux agissent comme une salle de miroirs à l'échelle nanométrique, focaliser et amplifier la lumière au centre du faisceau dans ce que l'on appelle des cavités photoniques. Ce sont les éléments constitutifs des lasers et des LED à l'échelle nanométrique.
« Des dispositifs comme les cavités photoniques que nous avons construites sont probablement les ingrédients les plus divers et les plus personnalisables de la photonique, " a déclaré l'auteur principal de l'article, Jelena Vuckovic, un professeur de génie électrique. "Les applications vont de la physique fondamentale aux nanolasers et aux biocapteurs qui pourraient avoir un impact profond sur la recherche biologique."
Au niveau cellulaire, un nanofaisceau agit comme une aiguille capable de pénétrer les parois cellulaires sans blessure. Une fois inséré, le faisceau émet de la lumière, produisant un éventail remarquable d'applications et d'implications de recherche. Alors que d'autres groupes ont montré qu'il est possible d'insérer des nanotubes simples et des nanofils électriques dans les cellules, personne n'avait encore réalisé des composants optiques aussi compliqués à l'intérieur des cellules biologiques.
"Nous pensons qu'il s'agit d'un changement assez spectaculaire par rapport aux applications existantes et qu'il permettra de multiplier les opportunités pour comprendre et influencer la biologie cellulaire, " a déclaré le premier auteur de l'article, Gary Shambat, un doctorant en génie électrique. Shambat travaille au Nanoscale and Quantum Photonics Lab dirigé par Vuckovic.
Fer à repasser à un aimant
Dans ce cas, les cellules étudiées provenaient d'une tumeur de la prostate, indiquant une application possible de la sonde dans la recherche sur le cancer. L'utilisation principale et la plus immédiate serait la détection en temps réel de protéines spécifiques dans les cellules, mais la sonde pourrait être adaptée pour détecter toute biomolécule importante telle que l'ADN ou l'ARN.

Cette image montre un nanofaisceau photonique inséré dans une cellule. Les trous gravés à travers le faisceau ainsi que la structure en couches de type sandwich du faisceau lui-même sont clairement visibles. La structure du faisceau alterne entre des couches d'arséniure de gallium et un cristal photonique contenant les points quantiques producteurs de photons. Crédit :Gary Shambat, École d'ingénierie de l'Université de Stanford
Pour détecter ces molécules clés, les chercheurs enduisent la sonde de certaines molécules organiques ou anticorps connus pour attirer les protéines cibles, tout comme le fer à un aimant. Si les protéines désirées sont présentes dans la cellule, ils commencent à s'accumuler sur la sonde et provoquent un décalage léger mais détectable de la longueur d'onde de la lumière émise par l'appareil. Ce décalage est une indication positive que la protéine est présente et en quelle quantité.
"Disons que vous avez une étude qui s'intéresse à savoir si un certain médicament produit ou inhibe une protéine spécifique. Notre biocapteur dira définitivement si le médicament fonctionne et dans quelle mesure en fonction de la couleur de la lumière de la sonde. Ce serait assez un outil puissant, " a expliqué Sanjiv Sam Gambhir, MARYLAND, co-auteur de l'article et président du département de radiologie de la Stanford School of Medicine ainsi que directeur du centre canarien de Stanford pour la détection précoce du cancer.
En tant que tel, des capteurs optiques nanométriques intégrables représenteraient un développement clé dans la quête de thérapies anticancéreuses spécifiques au patient, souvent appelées médecine personnalisée, dans lesquelles les médicaments sont ciblés sur le patient en fonction de son efficacité.
Une structure intelligente
Structurellement, le nouveau dispositif est un sandwich de couches extrêmement minces d'arséniure de gallium semi-conducteur alternant avec des couches tout aussi minces de cristal électroluminescent, une sorte de carburant photonique connu sous le nom de points quantiques. La structure est taillée dans des copeaux ou des plaquettes, un peu comme les sculptures sont ciselées dans la roche. Une fois sculpté, les dispositifs restent attachés au substrat épais.
Shambat et ses collègues ingénieurs ont travaillé sur des dispositifs optiques similaires pour une utilisation en ultrarapide, des applications informatiques ultra-efficaces où le fait d'avoir des dispositifs immobilisés sur des puces et des plaquettes n'a pas tellement d'importance puisqu'ils seront à terme intégrés à la microélectronique.
Pour les applications biologiques, cependant, l'épaisseur, substrat lourd présente un obstacle sérieux pour l'interfaçage avec des cellules individuelles. Les nanocavités sous-jacentes et très importantes sont verrouillées en position sur le matériau rigide et incapables de pénétrer les parois cellulaires.
La percée de Shambat est survenue lorsqu'il a réussi à décoller les nanofaisceaux photoniques, laissant la plaquette volumineuse derrière. Il a ensuite collé le dispositif photonique ultrafin à un câble à fibre optique avec lequel il dirige la sonde en forme d'aiguille vers et dans la cellule.
De la même manière, anticipant que l'arséniure de gallium pourrait être toxique pour les cellules, Shambat a également conçu un moyen astucieux d'encapsuler ses appareils dans un revêtement électriquement isolant d'alumine et de zircone. Le revêtement sert à deux fins :il protège à la fois la cellule de l'arséniure de gallium potentiellement toxique et protège la sonde de la dégradation dans l'environnement cellulaire.
Des résultats "éblouissants"
Une fois inséré dans la cellule, la sonde émet de la lumière, que l'on peut observer de l'extérieur. Pour les ingénieurs, cela signifie que presque toutes les applications ou utilisations actuelles de ces puissants dispositifs photoniques peuvent être transposées dans l'environnement auparavant interdit de l'intérieur de la cellule.
Dans une conclusion que les auteurs qualifient d'étonnante, ils ont chargé leurs nanofaisceaux dans les cellules et ont observé la croissance des cellules, ont migré dans l'environnement de recherche et se sont reproduits. Chaque fois qu'une cellule se divise, l'une des cellules filles a hérité du nanofaisceau du parent et le faisceau a continué à fonctionner comme prévu.
Cette héritabilité permet aux chercheurs d'étudier les cellules vivantes sur de longues périodes de temps, un avantage de recherche impossible avec les techniques de détection existantes, qui nécessitent que les cellules soient mortes ou fixées en place.
"Nos sondes nanométriques peuvent résider dans les cellules pendant de longues périodes, fournir potentiellement un retour de capteur ou donner des signaux de contrôle aux cellules en aval, " a déclaré Shambat. "Nous avons suivi une cellule pendant huit jours. C'est long pour une étude à cellule unique."