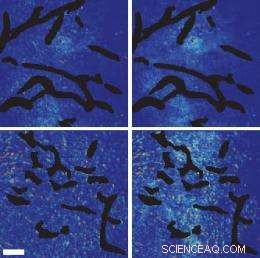
Panneaux supérieurs :configurations de contrôle. Panneaux inférieurs :Tissu tumoral mammaire après normalisation des vaisseaux sanguins. À gauche :peu de grosses nanoparticules sont visibles. À droite :les plus petites nanoparticules ont bien pénétré. Crédit :Vikash Chauhan / Nature Nanotech.
La combinaison de deux stratégies conçues pour améliorer les résultats du traitement du cancer – les médicaments antiangiogéniques et les nanomédicaments – ne peut réussir que si les plus petits nanomédicaments sont utilisés. Une nouvelle étude des chercheurs du Massachusetts General Hospital (MGH), apparaissant dans Nature Nanotechnologie , constate que la normalisation des vaisseaux sanguins dans les tumeurs, qui améliore l'administration des médicaments de chimiothérapie standard, peuvent bloquer l'administration de molécules de nanothérapie plus grosses.
"Nous avons découvert que la normalisation vasculaire ne fait qu'augmenter l'administration des plus petits nanomédicaments aux cellules cancéreuses, " dit Vikash P. Chauhan, du laboratoire Steele de biologie des tumeurs du service de radio-oncologie de l'HGM, auteur principal du rapport. "Nous avons également montré que les plus petits nanomédicaments sont intrinsèquement meilleurs que les plus grands nanomédicaments pour pénétrer les tumeurs, suggérant que des nanomédicaments plus petits pourraient être idéaux pour le traitement du cancer."
Les tumeurs doivent générer leur propre approvisionnement en sang pour continuer à croître, mais les vaisseaux alimentant les tumeurs ont tendance à être désorganisés, surdimensionné et qui fuit. Non seulement cela empêche l'administration de médicaments chimiothérapeutiques aux cellules non proches des vaisseaux tumoraux, mais la fuite de plasma hors des vaisseaux sanguins augmente la pression à l'intérieur de la tumeur, réduisant davantage la capacité des médicaments à pénétrer dans les tumeurs. Le traitement avec des médicaments qui inhibent l'angiogenèse - le processus par lequel de nouveaux vaisseaux sont générés - réduit certaines de ces anomalies, un processus appelé normalisation vasculaire qui s'est avéré améliorer le traitement de certains cancers avec des médicaments de chimiothérapie standard.
Les nanomédicaments sont en fait conçus pour exploiter les anomalies des vaisseaux tumoraux. Alors que les molécules des médicaments de chimiothérapie standard mesurent environ un nanomètre – un milliardième de mètre – les molécules de nanomédecine sont de 10 à 100 fois plus grosses, trop grand pour pénétrer les pores des vaisseaux sanguins dans les tissus normaux mais assez petit pour passer à travers les pores surdimensionnés des vaisseaux tumoraux. Étant donné que la taille des nanomédicaments devrait les maintenir hors des tissus normaux, ils sont prescrits pour réduire les effets secondaires négatifs de la chimiothérapie.
La présente étude a été conçue pour déterminer si l'utilisation de médicaments anti-angiogenèse pour normaliser la vascularisation tumorale améliorerait ou entraverait l'administration de nanomédicaments aux cellules tumorales. Dans des études utilisant un modèle murin de cancer du sein, les enquêteurs ont d'abord confirmé que le traitement avec le DC101, un anticorps contre une molécule essentielle à la croissance des vaisseaux sanguins, diminué temporairement le diamètre des vaisseaux sanguins tumoraux agrandis. Ils ont ensuite montré que cette normalisation vasculaire améliorait la pénétration dans les tumeurs des particules de 12 nanomètres mais pas des molécules de 60 ou 125 nanomètres.
Un modèle mathématique préparé par l'équipe du MGH a prédit que, tandis que les pores anormalement grands dans les parois des vaisseaux sanguins tumoraux entraînent une augmentation de la pression à l'intérieur de la tumeur qui empêche l'entrée des médicaments, la réduction de la taille des pores par un traitement anti-angiogenèse soulagerait la pression intratumorale, permettant l'entrée de ces molécules qui passent à travers les pores plus petits. Pour tester cette prédiction, ils ont traité des souris avec des tumeurs mammaires implantées soit avec DC101 et Doxil, une version 100 nanomètres du médicament chimiothérapeutique doxorubicine, ou avec DC101 et Abraxane, une version 10 nanomètres du paclitaxel. Bien que le traitement avec les deux chimiothérapies ait retardé la croissance tumorale, la normalisation vasculaire avec le DC101 n'a amélioré que l'efficacité d'Abraxane et n'a eu aucun effet sur le traitement par Doxil.
"Une variété de nanomédicaments anticancéreux sont actuellement utilisés ou en essais cliniques, " dit Chauhan, qui est un étudiant diplômé de la Harvard School of Engineering and Applied Sciences (SEAS). "Nos résultats suggèrent que la combinaison de nanomédicaments plus petits avec des thérapies antiangiogéniques peut avoir un effet synergique et que les nanomédicaments plus petits devraient intrinsèquement pénétrer les tumeurs plus rapidement que les nanomédicaments plus gros, en raison des principes physiques qui régissent la pénétration de la drogue. Bien qu'il semble que le développement futur des nanomédicaments devrait se concentrer sur leur petite taille (environ 12 nanomètres), nous devons également rechercher des moyens d'améliorer l'administration des nanomédicaments plus volumineux actuellement utilisés. »
« Les agents antiangiogéniques sont prescrits à un grand nombre de patients cancéreux en association avec les thérapeutiques conventionnelles, " explique Rakesh K. Jain, Doctorat, directeur du Steele Lab et auteur principal et correspondant du Nature Nanotechnologie rapport. "Notre étude fournit des lignes directrices sur la façon de combiner les médicaments antiangiogéniques avec les nanothérapies." Jain est professeur cuisinier de radio-oncologie (biologie des tumeurs) à la Harvard Medical School.