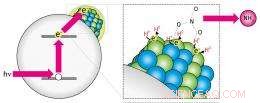
L'utilisation du rayonnement ultraviolet (hν) pour produire des électrons énergétiques (e-) permet à un catalyseur cuivre-palladium (sphères vertes et bleues) de générer de l'hydrogène (H0) sans utiliser de combustibles fossiles. Ce matériau peut alors transformer les ions nitrate (NO3-) en ammoniac (NH3). Reproduit, avec la permission, de Réf. 1 © 2011 Société chimique américaine
Nourrir les cultures avec de l'ammoniac synthétique (NH
Une équipe de recherche dirigée par Miho Yamauchi et Masaki Takata du centre RIKEN SPring-8 à Harima a maintenant découvert un moyen presque idéal de détoxifier les effets des engrais à base d'ammoniac. En synthétisant des nanocatalyseurs bimétalliques photoactifs qui génèrent de l'hydrogène gazeux à partir de l'eau en utilisant l'énergie solaire, l'équipe peut convertir catalytiquement le NO
Remplacement des atomes d'oxygène du NO
Selon Yamauchi, le défi de la synthèse d'alliages CuPd mélangés de manière homogène est de trouver le bon timing :les deux ions métalliques se transforment en états atomiques à des vitesses différentes, provoquant une séparation de phases. Yamauchi et son équipe ont utilisé les puissants rayons X du synchrotron du SPring-8 Center pour caractériser la structure atomique de la CuPd synthétisée avec des réactifs agressifs ou doux. Leurs expériences ont révélé qu'un réactif réducteur relativement puissant appelé borohydrure de sodium donnait des alliages avec un mélange presque parfait jusqu'à des dimensions nanométriques.
La plupart des synthèses d'ammoniac utilisent de l'hydrogène gazeux produit à partir de combustibles fossiles, mais l'utilisation de l'énergie solaire par les chercheurs évite cela. Ils ont découvert que le dépôt du nanoalliage sur du dioxyde de titane photosensible (TiO
Yamauchi est convaincu que cette approche peut aider à réduire l'impact écologique de nombreuses réactions d'hydrogénation chimique classiques. « Compte tenu des problèmes environnementaux auxquels nous sommes confrontés, il faut passer de la synthèse chimique à l'hydrogène fossile à d'autres procédés propres, " dit-elle.