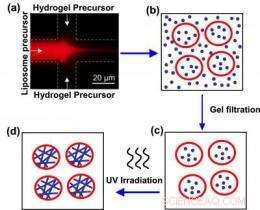
Schéma illustrant la création d'hybrides liposome-hydrogel. Une solution contenant un phospholipide ("précurseur de liposomes") se mélange avec une solution contenant un précurseur d'hydrogel (a). Se fondant à l'interface des deux canaux, le phospholipide forme des liposomes (b) qui piègent le précurseur d'hydrogel à l'intérieur. La matière à l'extérieur des vésicules est retirée (c) et les liposomes sont irradiés aux UV. Cela polymérise les chaînes protéiques dans l'hydrogel et donne un hybride liposome-hydrogel (d). Crédit :NIST
Les gens ont combiné des matériaux pour obtenir les meilleures propriétés des deux depuis que le cuivre et l'étain ont été fusionnés pour commencer l'âge du bronze. Dans la dernière fusion réussie, chercheurs de l'Institut national des normes et de la technologie, l'Université du Maryland et la Food and Drug Administration (FDA) des États-Unis ont mis au point une méthode pour combiner deux substances qui, individuellement, ont suscité un intérêt pour leurs applications biomédicales potentielles :une « bulle » de membrane phospholipidique appelée liposome et des particules d'hydrogel, un réseau rempli d'eau de chaînes polymères. La combinaison forme une particule hybride à l'échelle nanométrique (un milliardième de mètre) qui pourrait un jour se déplacer directement vers des cellules spécifiques telles que des tumeurs, passer facilement à travers la membrane cellulaire de la cible, puis libérer lentement une charge utile de médicament.
Dans un article récent de la revue Langmuir , l'équipe de recherche a examiné comment les liposomes et les nanoparticules d'hydrogel présentent des avantages et des inconvénients individuels pour l'administration de médicaments. Alors que les liposomes ont des propriétés de surface utiles qui leur permettent de cibler des cellules spécifiques et de traverser les membranes, ils peuvent se rompre si le milieu environnant change. Les nanoparticules d'hydrogel sont plus stables et possèdent des capacités de libération contrôlée pour ajuster le dosage d'un médicament au fil du temps, mais sont sujettes à la dégradation et à l'agglutination. L'objectif des chercheurs était de concevoir des nanoparticules incorporant les deux composants pour utiliser les forces de chaque matériau tout en compensant leurs faiblesses.
Pour fabriquer leurs vésicules hybrides liposome-hydrogel, les chercheurs ont adapté une technique NIST-UM connue sous le nom de COMMAND pour le mélange microfluidique contrôlé et la détermination des nanoparticules qui utilise un dispositif fluidique microscopique (microfluidique). Dans le nouveau travail, les molécules de phospholipides sont dissoutes dans de l'alcool isopropylique et alimentées via un minuscule (21 micromètres de diamètre, ou trois fois la taille d'une cellule de levure) canal d'entrée dans un canal "mélangeur", puis "focalisé" en un jet de fluide par une solution à base d'eau ajoutée par deux canaux latéraux. Des molécules précurseurs d'hydrogel sont mélangées au fluide de focalisation.
Au fur et à mesure que les composants se mélangent aux interfaces des flux de fluide, les molécules de phospholipides s'auto-assemblent en vésicules nanométriques de taille contrôlée et piègent les monomères en solution à l'intérieur. Les vésicules nouvellement formées sont ensuite irradiées avec de la lumière ultraviolette pour polymériser les précurseurs d'hydrogel qu'elles transportent en un gel solide constitué de chaînes réticulées. Ces chaînes renforcent les vésicules tout en leur permettant de conserver la forme sphérique de l'enveloppe liposomique (qui, à son tour, faciliterait le passage à travers une membrane cellulaire).
Pour transformer les vésicules hybrides liposome-hydrogel en véhicules d'administration cellulaire, un médicament ou une autre cargaison serait ajouté au fluide de focalisation pendant la production.