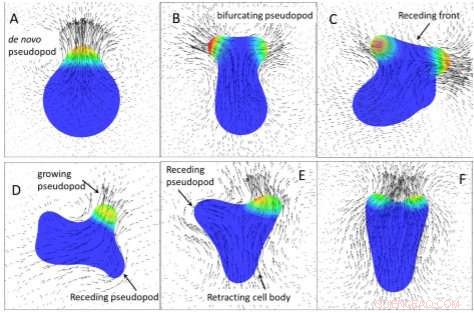
Des vecteurs de vitesse instantanée du fluide tracés dans un plan passant par le centre de gravité de la cellule, superposée à une forme de cellule 2D. Crédit :Eric J. Campbell et Prosenjit Bagchi, Université Rutgers
Des motifs rythmiques et des mouvements précis, ce sont des éléments clés d'une bonne nage. Les olympiens présentent des schémas respiratoires répétés, avec tête synchronisée, mouvements des jambes et des bras, captivant les spectateurs et provoquant des applaudissements pour des allures record. Des démonstrations comparables de cette répétition de schéma et de cette consommation d'énergie peuvent également être observées chez un nageur microscopique, la cellule amiboïde.
Les formes de nage des cellules sont désormais prévisibles à de nouveaux niveaux de précision grâce à une modélisation 3D avancée. Les chercheurs Eric J. Campbell et Prosenjit Bagchi, du Département de génie mécanique et aérospatial de l'Université Rutgers, a généré un modèle 3-D d'une amibe pratiquant la nage dirigée par des pseudopodes. La recherche apparaîtra sur la couverture du numéro de ce mois-ci de Physique des fluides .
Les cellules amiboïdes ont des cytosquelettes particulièrement flexibles, sans forme définie. Ils peuvent contracter et étendre leur système squelettique tout en modifiant simultanément la consistance de leur cytoplasme, le plasma entourant les organites de la cellule. Les cellules amiboïdes se distinguent également par leur capacité de motilité induite par les pseudopodes. Pseudopodes, signifiant faux pieds, sont des projections du corps cellulaire qui peuvent croître, diviser ou se rétracter pour assurer la locomotion. Le mouvement des pseudopodes est plus complexe que prévu. Il repose sur des réactions biomoléculaires, la déformation cellulaire et le mouvement du cytoplasme et du liquide extracellulaire.
« Dans cette recherche, nous avons combiné un modèle de pointe pour la déformation cellulaire avec le mouvement des fluides intra- et extra-cellulaires, et la biochimie des protéines à l'aide d'un modèle de formation de motifs dynamiques, ", a déclaré Campbell. "Nous avons ensuite utilisé des superordinateurs parallèles pour prédire le mouvement de la cellule, et étudié son comportement en faisant varier la déformabilité des cellules, viscosité du fluide, et la diffusivité des protéines."
Les cellules amiboïdes montrent une unidirectionnalité dans la nage avec un changement correspondant dans la dynamique des pseudopodes, causée par des projections de plus en plus répandues à l'avant de la cellule. Cette unidirectionnalité est probablement causée par une vitesse de nage accrue en raison de l'orientation focalisée. En utilisant des simulations de modèles informatiques, les chercheurs ont étudié la nage cellulaire en faisant varier la diffusivité des protéines, l'élasticité de la membrane et la viscosité cytoplasmique.
La modélisation précise de la nage des cellules amiboïdes a posé un certain nombre de défis. « Le modèle devait pouvoir résoudre les déformations en trois dimensions avec une grande précision et sans aucune instabilité numérique, " a déclaré Campbell. La biochimie des protéines, qui crée la force locomotrice, devait être couplé au modèle. Le mouvement fluide devait également être pris en compte. "Les fluides intra- et extra-cellulaires peuvent avoir des propriétés différentes, et le modèle doit tenir compte de ces différences."
Ces différents paramètres ont été intégrés pour optimiser la modélisation de la locomotion cellulaire, fournir du neuf, des informations plus précises sur les mécanismes de locomotion. Les cellules amiboïdes démontrant cette motilité entraînée par les pseudopodes peuvent offrir des informations sur de nombreux processus biologiques. Selon Campbell, la mobilité est également observée au cours du développement embryonnaire, cicatrisation des plaies, réponse immunitaire des globules blancs, et les cellules cancéreuses métastatiques.