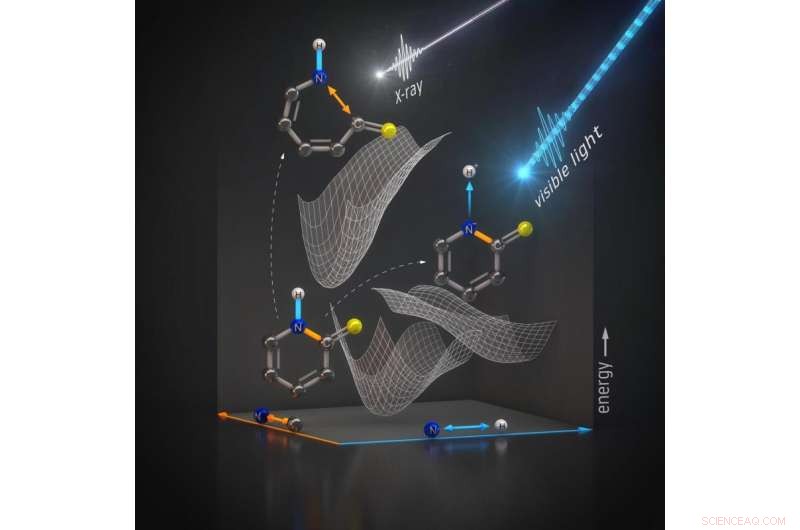
Une illustration montre comment l'énergie de la lumière modifie une molécule de 2-thiopyridone. La lumière optique frappe la molécule, et il perd un proton lié à l'hydrogène. Une sonde à rayons X permet aux scientifiques de suivre la rupture sélective des liaisons entre l'azote et ses voisins carbone et hydrogène. Crédit :Helmholtz-Zentrum Berlin
Lorsque les molécules qui portent le code génétique dans nos cellules sont exposées à des dommages, ils ont des défenses contre les ruptures et les mutations potentielles.
Par exemple, lorsque l'ADN est frappé par la lumière ultraviolette, il peut perdre l'excès d'énergie du rayonnement en éjectant le noyau d'un atome d'hydrogène (un seul proton) pour empêcher la rupture des autres liaisons chimiques du système.
Pour mieux comprendre ce processus, les chercheurs ont utilisé les impulsions laser à rayons X de la source de lumière cohérente Linac (LCLS) du laboratoire national de l'accélérateur SLAC du ministère de l'Énergie pour étudier comment l'énergie de la lumière transforme une molécule relativement simple, 2-thiopyridone. Cette molécule subit une transformation chimique qui se produit également dans les éléments constitutifs de l'ADN. Les scientifiques ont examiné ce processus en sondant l'atome d'azote dans la molécule avec des impulsions de rayons X qui n'ont duré que quelques femtosecondes, ou des quadrillions de seconde.
Les résultats, Publié dans Angewandte Chemie , sont un pas vers une meilleure compréhension de ce que l'on appelle les "transferts de protons à l'état excité" dans l'ADN et d'autres molécules.
"À l'heure actuelle, nous voulons rester simple, " dit l'auteur principal Sebastian Eckert, doctorant à l'Université de Potsdam et Helmholtz-Zentrum Berlin. « Il est plus facile de regarder les effets de la photoexcitation dans la 2-thiopyridone car cette molécule est suffisamment petite pour être comprise et ne possède qu'un seul atome d'azote. Nous sommes parmi les premiers au LCLS à examiner l'azote à cette énergie, il s'agit donc en quelque sorte d'une expérience pilote."
C'est aussi la première fois que la méthode, connu sous le nom de diffusion inélastique résonante des rayons X ou RIXS, a été utilisé pour examiner les changements moléculaires impliquant l'azote qui se produisent en femtosecondes. Ce court laps de temps est important car c'est à cette vitesse que les protons sont chassés des molécules exposées à la lumière, et il faut des rayons X brillants pour voir ces changements ultrarapides.
« LCLS est la seule source de lumière à rayons X qui peut fournir suffisamment de photons - des particules de lumière, " dit la co-auteur Munira Khalil, professeur à l'Université de Washington. "Notre mécanisme de détection est" avide de photons "et nécessite des impulsions lumineuses intenses pour capturer l'effet que nous voulons voir."
Dans l'étude, les chercheurs ont utilisé un laser optique pour initier des changements dans la molécule, suivi d'une sonde à rayons X LCLS qui leur a permis de voir les mouvements dans les liaisons.
"Nous recherchons un effet de résonance - une signature qui nous permet de savoir que nous avons réglé les rayons X sur une énergie qui garantit que nous n'examinons que les changements liés ou proches de l'atome d'azote, " dit Mike Minitti, scientifique du LCLS et co-auteur de l'article.
Ces études de « résonance » amplifient le signal de manière à ce que les scientifiques puissent clairement interpréter la façon dont les rayons X interagissent avec l'échantillon.
L'équipe de recherche s'est principalement intéressée aux liaisons entre les atomes voisins de l'azote, et a confirmé que la lumière optique brise les liaisons azote-hydrogène.
"Nous avons également pu confirmer que les rayons X utilisés pour sonder l'échantillon ne brisent pas la liaison azote-hydrogène, la sonde elle-même ne crée donc pas d'effet artificiel. L'énergie des rayons X est plutôt transférée à une liaison entre les atomes d'azote et de carbone, le rompre, " dit Jesper Norell, doctorant à l'Université de Stockholm et co-auteur de l'article.
Prochain, la collaboration utilisera la même approche pour étudier des molécules plus complexes et mieux comprendre la vaste classe de réactions photochimiques.