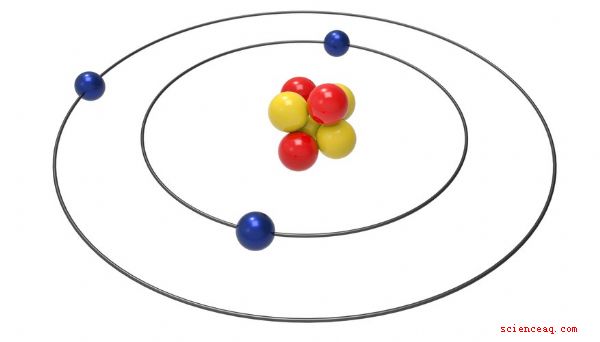
Un isotope est un élément qui a une quantité de neutrons différente de sa masse atomique standard. Certains isotopes peuvent être relativement instables et peuvent donc émettre des radiations au fur et à mesure que l'atome se désintègre. Les neutrons sont des particules avec une charge neutre qui se trouvent dans le noyau d'un atome aux côtés des protons. Les neutrons aident à donner à l'atome sa masse et sa structure; sur le tableau périodique des éléments, le nombre de masse atomique est la somme des protons et des neutrons.
Découvrez combien de neutrons possède l'atome donné de l'élément. Ces informations devront probablement être fournies; la capacité d'examiner un atome individuel est extrêmement difficile et coûteuse.
Regardez l'atome sur le tableau périodique des éléments et découvrez quelle est sa masse atomique.
Soustrayez le nombre de protons de la masse atomique. Il s'agit du nombre de neutrons que possède la version régulière de l'atome. Si le nombre de neutrons dans l'atome donné est différent, c'est un isotope.