Les scientifiques du laboratoire national d'Oak Ridge du ministère de l'Énergie ont fait un grand pas en avant vers la compréhension d'un processus viable de capture directe dans l'air, ou DAC, du dioxyde de carbone de l'atmosphère. Ce processus DAC en est à ses débuts dans le but d'obtenir des émissions négatives, où la quantité de dioxyde de carbone éliminée de l'enveloppe des gaz entourant la Terre dépasse la quantité émise.
La recherche, récemment publiée dans Cell Reports Physical Science , s'est concentré sur les étapes fondamentales de la séquestration du dioxyde de carbone à l'aide de glycine aqueuse, un acide aminé connu pour ses qualités absorbantes. En combinant une série de méthodes informatiques avancées, les scientifiques ont sondé des phénomènes dynamiques moins explorés dans les solutions liquides liés à la vitesse à laquelle le dioxyde de carbone peut être capturé.
"Les réactions chimiques dans l'eau sont compliquées, surtout lorsque le mouvement des molécules d'eau joue un rôle important", a déclaré Santanu Roy, qui a conçu l'enquête informatique avec son collègue Vyacheslav Bryantsev. "Les molécules d'eau et les produits chimiques s'engagent dans quelque chose de similaire à une danse couplée qui peut ralentir légèrement ou considérablement la réaction. Comprendre ces interactions dynamiques, connues sous le nom d'effets de solvant hors équilibre, est essentielle pour avoir une idée complète du fonctionnement des réactions et de la rapidité avec laquelle elles se produisent. "
Les chercheurs ont découvert qu’en examinant la vitesse à laquelle le dioxyde de carbone est absorbé, se concentrer uniquement sur la barrière de l’énergie libre – le seuil d’énergie qui doit être surmonté pour qu’un système passe d’un état à un autre – est une simplification excessive qui ne fournit pas l’intégralité de l’information. image. Cette approche incomplète peut conduire à une compréhension inexacte de la cinétique de réaction, les facteurs qui influencent la vitesse à laquelle une réaction se produit.
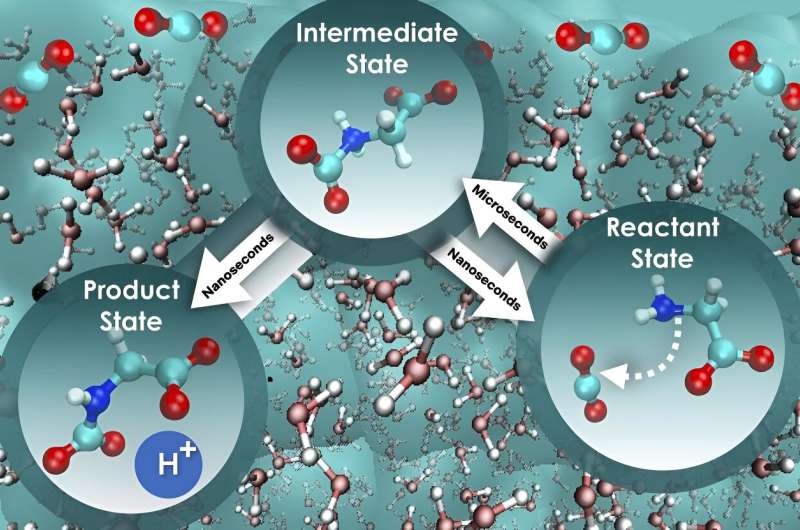
"Nous avons utilisé une approche plus complète qui prend en compte l'influence de l'eau sur le mouvement le long du chemin de réaction, et le résultat était intrigant", a déclaré Bryantsev. "L'étape initiale, où la glycine interagit avec le dioxyde de carbone, est près de 800 fois plus lente que l'étape suivante, où un proton est libéré pour finalement former un mélange d'état de produit destiné à retenir le dioxyde de carbone absorbé.
"Il est frappant de constater que la barrière d'énergie libre reste constante pour les deux étapes, et donc cette perspective différente distingue véritablement la vitesse de ces deux étapes critiques et offre une voie pour augmenter l'efficacité de l'absorption et de la séparation du dioxyde de carbone."
Les simulations approfondies de dynamique moléculaire ab initio utilisées dans cette étude étaient encore limitées par leurs courtes échelles de temps et de longueur et par les coûts de calcul élevés pour représenter les réactions chimiques.
"Pour les projets futurs, nous avons l'intention de combiner l'approche émergente d'apprentissage automatique avec des simulations très précises et de développer des potentiels d'interaction interatomique basés sur des réseaux neuronaux profonds. Cela nous permettra d'effectuer des simulations moléculaires avec une grande précision à grande échelle avec des coûts de calcul considérablement réduits", " a déclaré Xinyou Ma, qui a réalisé les simulations.
Roy a ajouté :« Bien que nous ayons dressé un tableau cinétique au niveau moléculaire de la capture du dioxyde de carbone par les acides aminés aqueux, l'accès à de grandes échelles de longueur et de temps grâce à l'utilisation de l'approche d'apprentissage automatique nous aidera à comprendre les effets de facteurs macroscopiques tels que la température. , la pression et la viscosité sur le DAC et comment ces effets sont liés à l'image moléculaire obtenue."
Dans l’ensemble, les résultats de l’étude mettent en lumière le fonctionnement complexe du DAC et soulignent le rôle essentiel de la cinétique, de la thermodynamique et des interactions moléculaires dans l’élimination du dioxyde de carbone de l’atmosphère par les acides aminés aqueux. À mesure que ces mécanismes seront mieux compris, la perspective de déployer une technologie DAC à grande échelle deviendra plus réalisable. Dans le monde entier, plusieurs projets DAC différents en sont à différents stades de recherche, de test et de développement.
Plus d'informations : Xinyou Ma et al, Une étude d'énergie libre ab initio du mécanisme de réaction et des étapes limitantes de la capture du CO2 par la glycine aqueuse, Cell Reports Physical Science (2023). DOI :10.1016/j.xcrp.2023.101642
Informations sur le journal : Rapports cellulaires sur la science physique
Fourni par le Laboratoire national d'Oak Ridge