Une équipe de recherche affiliée à l'UNIST a réalisé un exploit révolutionnaire en observant la dissolution du sel dans l'eau au niveau atomique et en découvrant expérimentalement le principe sous-jacent.
Dirigée par le professeur Hyung-Joon Shin et ses chercheurs du Département de science et d'ingénierie des matériaux de l'UNIST, l'équipe a présenté la « technologie innovante de contrôle des ions uniques ». Cette approche de pointe permet la manipulation précise de molécules d'eau individuelles pour extraire sélectivement des ions spécifiques du sel.
Les résultats de l'étude ont été publiés dans Nature Communications. le 16 mars 2024.
Sel, composé de liaisons ioniques robustes entre les cations sodium (Na + ) et les anions chlore (Cl - ), subit un processus de transformation lorsqu’il est immergé dans l’eau. L'interaction entre les polarités positives et négatives des molécules d'eau perturbe la liaison entre les ions sodium et chlore, conduisant à leur séparation et à la formation d'eau salée.
Bien que le principe de dissolution du sel dans l’eau puisse sembler simple, les études antérieures ont principalement exploré ce phénomène de manière théorique. Cependant, la capacité de confirmer expérimentalement quels ions se dissolvent en premier dans l’eau et d’élucider le mécanisme par lequel les molécules d’eau affaiblissent les liaisons ioniques du sel était restée jusqu’à présent insaisissable. Le professeur Shin a fait remarquer :"Le défi résidait dans la nature complexe de l'étude et du contrôle des ions individuels au milieu du mouvement dynamique des ions dissous dans l'eau."
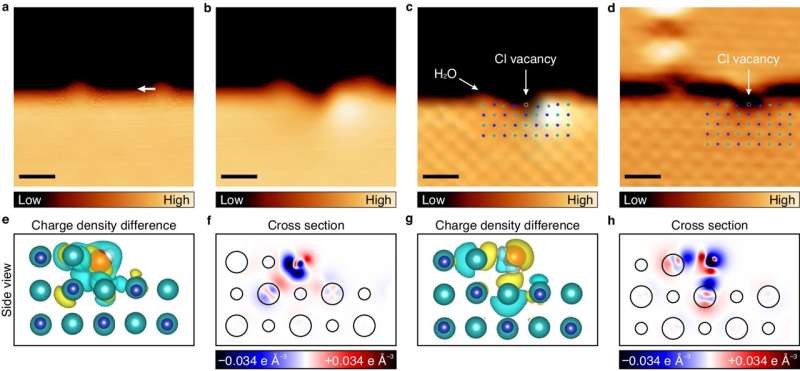
Dans une expérience méticuleusement contrôlée menée dans des conditions cryogéniques et sous vide ultra poussé à –268,8°C, l’équipe de recherche a placé une molécule d’eau sur une fine membrane de sel constituée de deux à trois couches atomiques. En utilisant un microscope à effet tunnel (STM) capable d'effectuer des mesures à l'échelle atomique, l'équipe a observé un infime changement de hauteur de 10 picomètres (pm) lorsque les molécules d'eau étaient manœuvrées horizontalement à travers la membrane de sel. Cette observation a été attribuée à la forte interaction entre les anions de chlore et les molécules d'eau.
En déplaçant stratégiquement des molécules d’eau le long du film de sel avec une épaisseur atomique variable, les chercheurs ont réussi à faire disparaître un anion chlore de son chemin. La polarité des molécules d'eau a joué un rôle central dans la rupture de la liaison ionique du sel, provoquant l'émergence de l'anion chlore avant le cation sodium.
L’équipe a en outre souligné que le taux de polarisation des anions chlore, qui est 20 fois plus prononcé que celui des cations sodium, les rend très sensibles aux changements électriques externes induits par les molécules d’eau. Cette réactivité accrue était particulièrement évidente dans les régions où les atomes manquaient de liaisons suffisantes avec l'environnement.
Huijun Han (Programme combiné MS/Ph.D. de science et d'ingénierie des matériaux, UNIST), l'auteur principal de l'article a déclaré :« Bien que la compréhension théorique de la fonte du sel dans l'eau soit établie depuis longtemps, notre succès dans l'extraction d'ions uniques à travers Le contrôle précis des molécules d'eau marque une avancée expérimentale significative."
"Les ions jouent un rôle central dans la modification des performances des batteries et des matériaux semi-conducteurs", a souligné le professeur Shin. "Nous envisageons d'exploiter la technologie de contrôle des ions uniques pour faire progresser les technologies fondamentales liées aux fonctionnalités ioniques."
Plus d'informations : Huijun Han et al, Dissolution contrôlée d'un seul ion à partir d'une interface saline, Nature Communications (2024). DOI :10.1038/s41467-024-46704-y
Informations sur le journal : Communications naturelles
Fourni par l'Institut national des sciences et technologies d'Ulsan