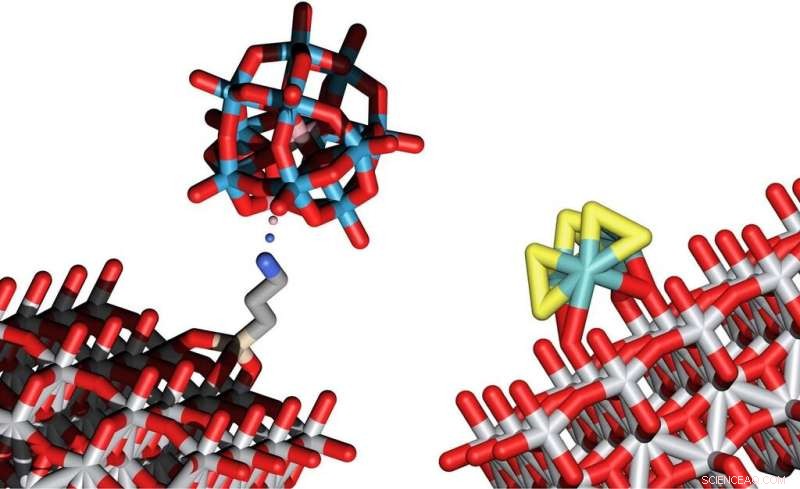
Modèles structuraux de deux clusters qui permettent la séparation de l'eau en O2 et H2 au moyen de l'énergie lumineuse. Crédit :Université de technologie de Vienne
L'hydrogène pourrait constituer une partie importante de notre futur approvisionnement énergétique :il peut être stocké, transporté et brûlé selon les besoins. Cependant, la majeure partie de l'hydrogène disponible aujourd'hui est un sous-produit de la production de gaz naturel, et cela doit changer pour des raisons de protection du climat. La meilleure stratégie à ce jour pour produire de l'« hydrogène vert » respectueux de l'environnement consiste à séparer l'eau en hydrogène et en oxygène en utilisant de l'électricité provenant de sources d'énergie renouvelables, par exemple des cellules photovoltaïques.
Cependant, ce serait beaucoup plus facile si la lumière du soleil pouvait être utilisée directement pour diviser l'eau. C'est exactement ce que les nouveaux catalyseurs rendent désormais possible, dans un processus appelé « fractionnement photocatalytique de l'eau ». Le concept n'est pas encore utilisé industriellement. À TU Wien, des étapes importantes ont maintenant été franchies dans cette direction :à l'échelle atomique, les scientifiques ont réalisé une nouvelle combinaison de catalyseurs moléculaires et à l'état solide qui peuvent faire le travail tout en utilisant des matériaux relativement peu coûteux.
Interaction des atomes
"En fait, pour pouvoir séparer l'eau avec la lumière, vous devez résoudre deux tâches en même temps", explique Alexey Cherevan de l'Institut de chimie des matériaux de la TU Wien. "Il faut penser à l'oxygène et à l'hydrogène. Les atomes d'oxygène de l'eau doivent être transformés en O2 molécules, et les ions hydrogène restants, qui ne sont que des protons, doivent être transformés en molécules H2."
Des solutions ont maintenant été trouvées pour les deux tâches. De minuscules amas inorganiques constitués d'un petit nombre d'atomes seulement sont ancrés sur une surface de structures de support absorbant la lumière telles que l'oxyde de titane. La combinaison de clusters et de supports semi-conducteurs soigneusement choisis conduit au comportement souhaité.
Les amas responsables de l'oxydation de l'oxygène sont constitués de cobalt, de tungstène et d'oxygène, tandis que les amas de soufre et de molybdène sont particulièrement adaptés à la création de molécules d'hydrogène. Les chercheurs de la TU Wien ont été les premiers à déposer ces amas sur une surface en oxyde de titane, où ils peuvent servir de catalyseurs pour la séparation de l'eau.
"L'oxyde de titane est sensible à la lumière, c'était déjà bien connu", explique Alexey Cherevan. "L'énergie de la lumière absorbée conduit à la création d'électrons libres et de charges positives libres dans l'oxyde de titane. Ces charges permettent ensuite aux amas d'atomes assis sur cette surface de faciliter la division de l'eau en oxygène et hydrogène. "
Contrôle précis, atome par atome
"D'autres groupes de recherche travaillant sur la séparation de l'eau par la lumière s'appuient sur des nanoparticules qui peuvent prendre des formes et des propriétés de surface très différentes", explique Alexey Cherevan. "Les tailles sont difficiles à contrôler, les atomes ne sont pas tout à fait disposés de la même manière. Par conséquent, dans ce cas, il n'est pas possible d'expliquer exactement comment se déroule le processus de catalyse en détail." À TU Wien, en revanche, la structure exacte des clusters est déterminée avec une précision atomique, ce qui permet une compréhension complète du cycle catalytique.
"C'est le seul moyen d'obtenir un retour d'information sur ce dont dépend réellement l'efficacité du processus", déclare Alexey Cherevan. "Nous ne voulons pas nous contenter d'une approche par essais et erreurs et essayer différentes nanoparticules jusqu'à ce que nous trouvions la meilleure. Nous voulons découvrir au niveau atomique quel est réellement le catalyseur optimal."
Maintenant que les matériaux sélectionnés se sont révélés adaptés à la séparation de l'eau, l'étape suivante consiste à affiner leur structure exacte pour atteindre des rendements encore plus élevés.
Simple et prometteur
"L'avantage décisif de notre méthode par rapport à la séparation de l'eau par électrolyse est sa simplicité", souligne Alexey Cherevan. La production d'hydrogène électrique nécessite d'abord une source d'énergie durable, telle que des cellules photovoltaïques, éventuellement un dispositif de stockage d'énergie électrique et une cellule d'électrolyse. Au total, cela se traduit par un système relativement complexe constitué d'une multitude de matières premières. Pour la séparation photocatalytique de l'eau, en revanche, il suffit d'une surface convenablement revêtue, recouverte d'eau et irradiée par le soleil.
A terme, cette méthode pourrait également être utilisée pour produire des molécules plus compliquées en utilisant le concept de photosynthèse artificielle. Il pourrait même être possible d'utiliser l'énergie du rayonnement solaire pour produire des hydrocarbures avec du dioxyde de carbone de l'atmosphère et de l'eau, qui peuvent ensuite être utilisés pour d'autres applications.
Les études associées apparaissent dans ACS Catalysis et ACS Matériaux Au . Surface du catalyseur analysée à résolution atomique