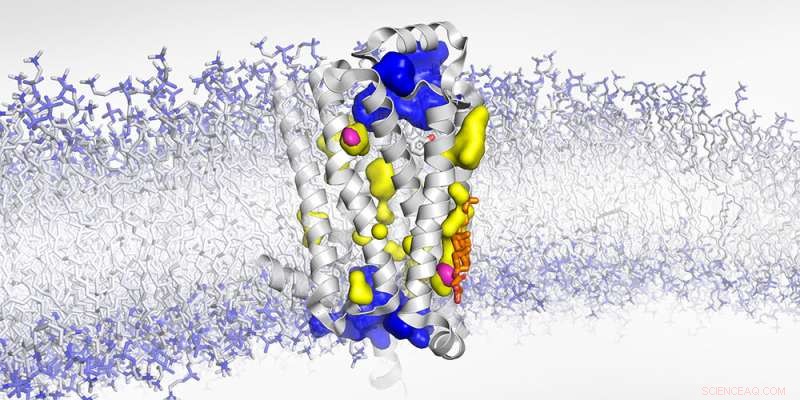
Structure du récepteur β1-adrénergique lié à la membrane avec des cavités exposées à l'eau (bleu), non accessibles à l'eau (jaune) et des vides secs (magenta). Crédit :Biozentrum, Université de Bâle
Presque toutes les fonctions vitales du corps humain sont régulées par des récepteurs dits couplés aux protéines G à la surface des cellules. Ces récepteurs servent ainsi de cibles médicamenteuses attrayantes pour traiter diverses maladies. Les chercheurs ont maintenant découvert que les espaces vides à l'intérieur de ces récepteurs sont importants pour leur activation et donc pour relayer les messages vers la cellule interne. Leur approche pour localiser ces vides peut aider à orienter la recherche de nouveaux médicaments.
Les récepteurs couplés aux protéines G (RCPG) nous permettent de voir, de goûter les aliments, d'avoir froid ou chaud ou de réagir au stress, entre autres. Situés à la surface des cellules, les GPCR détectent une grande variété de signaux tels que les nutriments, la lumière, les odeurs ou les hormones. En changeant de conformation, ils transmettent ces informations de l'extérieur vers l'intérieur de la cellule. Les connaissances accumulées sur les RCPG ont énormément affecté la médecine moderne :environ un tiers de tous les médicaments commercialisés ciblent les RCPG.
Espaces vides importants pour l'activation des récepteurs
Utilisant une technologie de pointe, l'équipe de recherche dirigée par le professeur Stephan Grzesiek, en collaboration avec des collaborateurs du Biozentrum de l'Université de Bâle et de l'Institut Paul Scherrer, a maintenant découvert que les GPCR contiennent des cavités complètement vides qui sont importantes pour leur activation. Leur approche expérimentale récente, publiée dans Nature Chemistry , peut orienter et accélérer la recherche de médicaments candidats nouveaux et plus spécifiques avec moins d'effets secondaires.
Bien que les 826 RCPG du corps humain répondent à de nombreux stimuli différents, ils partagent tous une architecture commune. "Notre objectif est de comprendre au niveau atomique comment les GPCR transmettent les signaux", explique le Dr Layara Abiko, qui a co-dirigé l'étude. "Depuis de nombreuses années, nous étudions donc le récepteur β1-adrénergique, un RCPG qui prépare l'organisme au combat ou à la fuite." L'adrénaline, une hormone, se lie à et active le récepteur qui déclenche une réponse au stress, provoquant par exemple une augmentation de la fréquence cardiaque et de la pression artérielle." Les bêta-bloquants inhibent ce récepteur et sont donc des médicaments efficaces pour traiter l'hypertension ou les maladies cardiovasculaires.
Localisation exacte des vides secs
"Grâce à la RMN à haute pression et à notre approche expérimentale utilisant la diffusion des rayons X sur des cristaux récepteurs incorporant le xénon, un gaz rare, nous avons pu compléter davantage l'image de ce récepteur hautement dynamique", explique Abiko. "Auparavant, on supposait que les cavités à l'intérieur du récepteur étaient remplies d'eau. Nous avons maintenant révélé que certaines d'entre elles sont vides." Lors de l'activation, la conformation du récepteur change de telle manière que ces vides secs se compriment et disparaissent. Par conséquent, le récepteur rétrécit comme lorsque vous pressez une éponge. Dans le cas du récepteur β1-adrénergique, ce changement conformationnel est essentiel pour initier la réponse de combat ou de fuite du corps.
Les chercheurs ont maintenant été en mesure de localiser exactement deux de ces cavités vides et ont révélé que le cholestérol, un composant important de la membrane cellulaire, peut remplir l'une d'entre elles. Comme un coin, le cholestérol empêche le récepteur de se comprimer et de passer à son état pleinement actif. "Bloquer ce vide obstrue les mouvements subtils mais essentiels nécessaires pour activer le GPCR", explique Abiko. "Nous pensons que cet effet de coin pourrait être une autre couche de régulation des récepteurs."
De nouvelles voies pour le développement de médicaments
Mais pourquoi le dépistage des vides secs peut-il être important ? Les sites de liaison aux médicaments classiques sont souvent similaires parmi les sous-classes de GPCR. Un médicament dirigé vers un tel site peut se lier à plus d'un récepteur et donc provoquer des effets secondaires indésirables. En revanche, les cavités sèches diffèrent considérablement entre les GPCR, même lorsqu'ils appartiennent à la même sous-classe. Cela en fait des cibles médicamenteuses hautement sélectives.
"De cette façon, vous pouvez concevoir des médicaments hautement spécifiques pour un récepteur", explique Abiko. La nouvelle approche développée peut localiser ces sites de liaison de médicaments non conventionnels qui diffèrent fortement entre les récepteurs. Cela peut faciliter le processus de sélection de nouveaux traitements, faire gagner du temps et réduire les coûts. Explorer les limites des récepteurs couplés aux protéines G