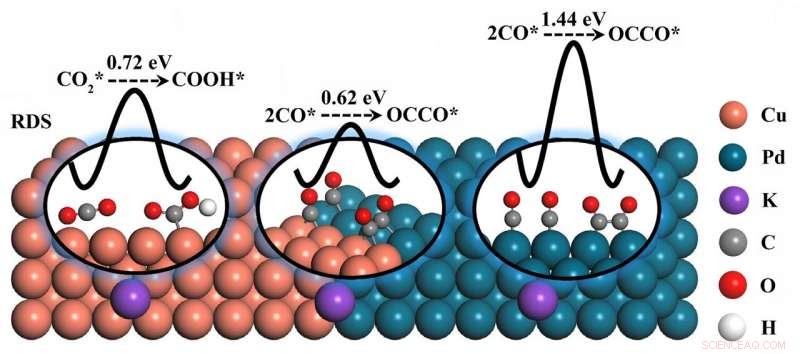
Une interface CuPd(100) intime a été conçue pour abaisser les barrières énergétiques de la réaction intermédiaire (hydrogénation CO2* et couplage C-C) et améliorer l'efficacité des produits C2. Le catalyseur d'interface CuPd (100) optimal a présenté une efficacité faradique C2 de 50,3 %, qui était 2,1 fois supérieur à celui du catalyseur Cu (23,6%) à ? 1,4 VRHE dans 0,1 M KHCO3. Crédit :Chinese Journal of Catalysis
Utilisation d'énergie électrique intermittente pour convertir un excès de CO
Récemment, une équipe de recherche dirigée par le professeur Min Liu de la Central South University, Chine, conçu un électrocatalyseur bimétallique Cu-Pd avec une interface CuPd (100) qui peut abaisser la barrière énergétique de la génération de produits C2. L'électrocatalyseur a été obtenu via une méthode de croissance in situ basée sur la réduction thermique pour fournir des nanoparticules de Pd sous forme de graines nucléées. Les résultats ont été publiés dans Journal chinois de catalyse .
Généralement, il y a deux facteurs limitants pour réaliser l'électroréduction du CO
Le calcul de la théorie fonctionnelle de la densité (DFT) montre que l'interface CuPd (100) améliore l'adsorption du CO
Ensuite, le catalyseur d'interface CuPd (100) cible a été préparé par une méthode chimique humide simple et prouvé par différentes méthodes de caractérisation. Les résultats de l'expérience de désorption programmée en température et de capteur de gaz ont prouvé l'amélioration du CO