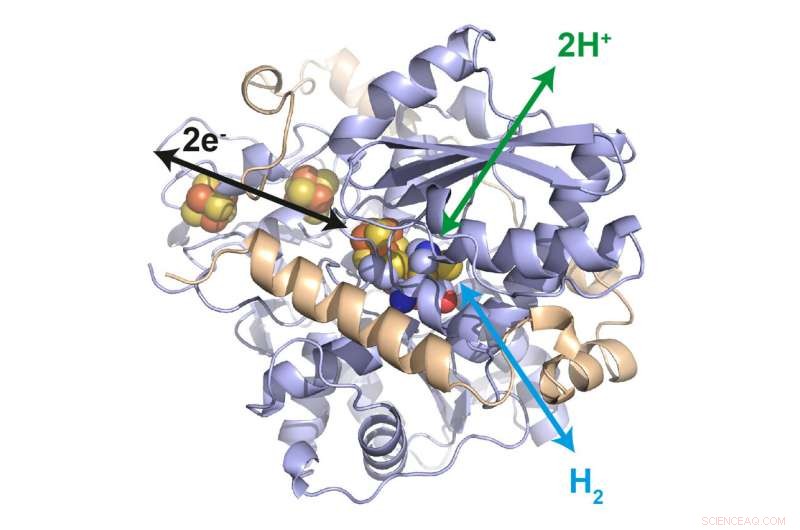
Structure de l'hydrogénase de Desulfovibrio desulfuricans. Dans son centre actif, un amas fer-soufre catalyse l'oxydation de l'hydrogène en protons ainsi que la réduction des protons en hydrogène. Des amas fer-soufre supplémentaires permettent le transfert d'électrons vers le polymère environnant. Crédit :Dr James Birrell / MPI CEC
Une enzyme pourrait réaliser un rêve pour l'industrie de l'énergie :elle peut produire efficacement de l'hydrogène à l'aide d'électricité et peut également produire de l'électricité à partir d'hydrogène. L'enzyme est protégée en l'enrobant dans un polymère. Une équipe de recherche internationale avec une participation significative de scientifiques de l'Université technique de Munich (TUM) a présenté le système dans la célèbre revue scientifique Catalyse naturelle .
Les piles à combustible transforment l'hydrogène en électricité, tandis que les électrolyseurs utilisent l'électricité pour diviser l'eau pour produire de l'hydrogène. Les deux ont besoin du platine, un métal précieux rare et donc coûteux, comme catalyseur. La nature a créé une solution différente :Enzymes, appelées hydrogénases. Ils catalysent la conversion de l'hydrogène très rapidement et presque sans perte d'énergie.
Cependant, dans le passé, ces biocatalyseurs n'étaient pas considérés comme adaptés à une utilisation industrielle en raison de leur grande sensibilité à l'oxygène. Aujourd'hui une équipe de recherche de l'Université technique de Munich (TUM), Ruhr-Universität Bochum (RUB), le Centre national français de la recherche scientifique (CNRS) à Marseille et l'Institut Max-Planck de conversion chimique de l'énergie ont réussi à intégrer les enzymes sensibles dans un polymère protecteur de manière à les rendre viables pour une utilisation dans la conversion technique de l'hydrogène.
Durabilité vs activité
"Lorsque les hydrogénases sensibles sont intégrées dans des polymères appropriés, elles continuent à fonctionner pendant plusieurs semaines, même en présence d'oxygène, " dit Nicolas Plumeré, Professeur d'électrobiotechnologie au TUM Campus Straubing pour la biotechnologie et la durabilité. "Sans cette protection, ils perdent leur activité en quelques minutes."
L'incorporation des hydrogénases dans des polymères dont les chaînes latérales peuvent transférer des électrons, appelés polymères redox, présente néanmoins deux inconvénients décisifs :une résistance élevée contrebalance le flux d'électrons à travers le polymère redox. Cela nécessite l'investissement d'énergie qui est ensuite perdue sous forme de chaleur. Et les hydrogénases intégrées perdent complètement leur capacité à générer de l'hydrogène.
Potentiel de réglage fin
Avec une sélection intelligente des bonnes chaînes latérales polymères, l'équipe de recherche a maintenant réussi à régler le potentiel redox du polymère de telle sorte que seule une petite surtension est nécessaire pour vaincre la résistance.
Des investigations plus détaillées ont ensuite révélé que le potentiel des chaînes latérales s'était légèrement déplacé vers des valeurs positives en raison de l'inclusion dans la matrice polymère. Dans une autre tentative, ils ont utilisé une chaîne latérale avec un potentiel négatif correspondant. Cette astuce a été la percée :l'hydrogénase était désormais capable de catalyser la réaction dans les deux sens sans perte d'énergie.
Biocatalyseur pour la conversion d'hydrogène
En utilisant ce système, l'équipe de recherche a ensuite construit une pile à combustible, dans lequel l'oxygène est réduit par l'enzyme bilirubine oxydase de la bactérie Myrothecium verrucaria, tandis que l'hydrogénase noyée dans le film polymère oxyde l'hydrogène de la bactérie desulfovibrio desulfuricans, produire de l'électricité dans le processus.
La cellule a atteint une valeur, avec une tension à vide de 1,16 V, le plus élevé jamais mesuré pour un système de ce type et proche du maximum thermodynamique. Avec trois milliampères par centimètre carré, la cellule atteint en même temps une densité de puissance très élevée pour les cellules biologiques.
Le système peut également être utilisé pour la réaction inverse, produire de l'hydrogène en consommant des électrons :le rendement de conversion énergétique est proche de 100 %, même avec des densités de puissance de plus de quatre milliampères par centimètre carré.
Plan directeur pour de nouveaux biocatalyseurs
« La réduction des déperditions énergétiques a deux avantages décisifs, " dit Nicolas Plumeré. " D'abord, il rend le système nettement plus efficace; seconde, la chaleur générée dans une pile à combustible à des niveaux de performance élevés poserait un problème pour les systèmes biologiques. »
Afin de rendre leur système compétitif par rapport aux systèmes utilisant des catalyseurs à base de platine, les recherches en cours de l'équipe se concentrent désormais sur l'amélioration de la stabilité des hydrogénases à des densités de puissance plus élevées.
Par ailleurs, les résultats peuvent également être transférés à d'autres catalyseurs hautement actifs mais sensibles pour la conversion d'énergie et l'électrosynthèse. Les objectifs directs ici sont principalement les enzymes de réduction du dioxyde de carbone qui peuvent utiliser l'électricité pour produire des carburants liquides ou des produits intermédiaires à partir du dioxyde de carbone.