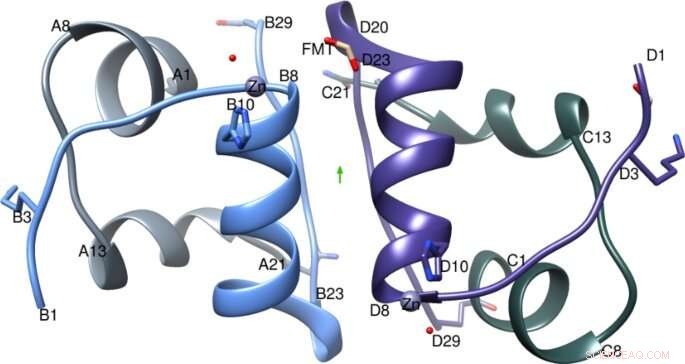
Dimère IGlu avec l'axe double (flèche verte), La chaîne en A est de couleur gris clair, Chaîne B en bleu clair, Chaîne en C en gris foncé et chaîne en D en violet. Figure créée à l'aide de Chimera v1.8.1 cgl.ucsf.edu/chimera/. Crédit: Rapports scientifiques (2021). DOI :10.1038/s41598-021-81251-2
Pour la première fois, les scientifiques ont proposé une explication atomique précise pour laquelle la glulisine - un médicament couramment utilisé pour traiter le diabète - agit plus rapidement que l'insuline.
Les résultats, publié aujourd'hui dans Rapports scientifiques , pourrait avoir des avantages pour les patients diabétiques en veillant à ce qu'une insuline plus améliorée puisse être développée pour un traitement futur.
L'étude a été réalisée par des experts des universités de Nottingham et de Manchester et de l'Imperial College de Londres, ainsi que la Diamond Light Source, l'installation scientifique nationale de rayonnement synchrotron du Royaume-Uni.
La glulisine est une insuline synthétique à action rapide développée par Sanofi-Aventis, sous le nom commercial d'Apidra. Il est utilisé pour améliorer le contrôle de la glycémie chez les adultes et les enfants diabétiques.
Dans cette nouvelle étude, les scientifiques ont entrepris d'établir la structure exacte de la gluisine, et comment cette structure pourrait affecter la façon dont elle se comporte physiologiquement.
L'équipe visait à établir, en examinant la structure, quel rôle fondamental joue la gluisine dans la gestion du diabète. Ces résultats pourraient potentiellement conduire à une amélioration de l'insuline synthétique pour les patients, avec moins d'effets secondaires.
Dr Gary Adams Professeur agrégé et lecteur en santé appliquée du diabète à l'Université de Nottingham, et auteur principal de l'étude, dit :« Pour la première fois, notre recherche fournit de nouveaux, des informations structurelles sur une insuline synthétique cliniquement pertinente, glulisine, qui est un traitement important pour les patients présentant un diabète.
"Cette information met en lumière la dissociation de la glulisine et peut expliquer sa dissociation rapide en dimères et monomères et donc sa fonction en tant qu'insuline à action rapide. Cette nouvelle information peut conduire à une meilleure compréhension du comportement pharmacocinétique et pharmacodynamique de la glulisine et, à son tour, pourrait aider à améliorer sa formulation et à réduire les effets secondaires de ce médicament."
Pour mener à bien la recherche, l'équipe a créé un cristal parfait de glulisine. Les chercheurs ont ensuite appliqué une combinaison de méthodes pour fournir un aperçu détaillé de la structure et de la fonction de la glulisine.
Dr Hodaya Salomon, membre de l'équipe de l'Imperial College, et le premier auteur conjoint a déclaré :« Les principales comparaisons au niveau moléculaire entre cette structure cristalline de la glulisine et les structures cristallines précédentes de l'insuline ont montré qu'une position unique de l'acide glutamique (un acide aminé), pas présent dans d'autres analogues à action rapide, pointé vers l'intérieur plutôt que vers la surface extérieure. Cela réduit les interactions avec les molécules voisines et augmente ainsi la préférence pour la forme dimère la plus active pour les patients, donnant aux experts une meilleure compréhension du comportement de la glulisine."
John Helliwell, Professeur émérite de chimie à l'Université de Manchester, et l'un des auteurs de l'article, a déclaré:"Une découverte inattendue a été que la formulation de glulisine est documentée comme un analogue de l'insuline sans zinc pour son action d'absorption rapide. La cristallographie de l'insuline a montré que le zinc est essentiel pour la formation d'hexamères. La nouvelle structure cristalline de la glulisine a montré que le zinc était lié de la même manière comme dans l'insuline native, par trois acides aminés histidine. Cette découverte doit signifier que des traces d'ions zinc sont présentes dans le commerce, tel que fourni, solution de formulation. Une optimisation supplémentaire pour la glulisine est maintenant claire, celui d'enlever enfin le zinc."