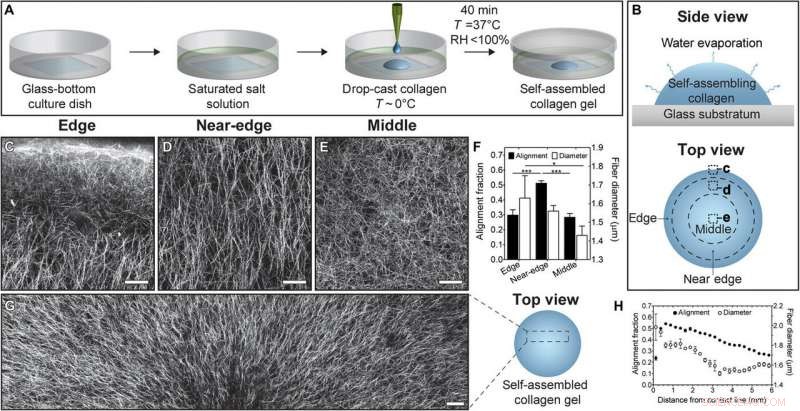
L'auto-assemblage de collagène dans des gouttelettes en évaporation génère des réseaux alignés de fibres de collagène. Schéma de (A) procédure de coulée en gouttes et (B) vues de dessus et de côté d'une gouttelette de collagène en évaporation. Images CRM d'une gouttelette de collagène auto-assemblée dans le bord (C), (D) près du bord, et (E) les régions moyennes d'intérêt. Les images sont orientées de telle sorte que le haut de l'image pointe vers la ligne de contact de la gouttelette. L'emplacement de chaque image est mis en évidence dans les cases en pointillés en (B). Les barres d'échelle représentent 50 um. (F) Fraction d'alignement et diamètre de fibre pour les gels de collagène coulés en gouttes. (G) Image CRM d'une gouttelette de collagène auto-assemblée. Cinq images CRM distinctes sont cousues ensemble pour révéler l'alignement radial des fibres de collagène. Barre d'échelle, 100 µm. (H) Fraction d'alignement et diamètre de fibre en fonction de la distance par rapport à la ligne de contact pour les gels de collagène coulés en gouttes. Les solutions de collagène (pH 11) ont été gélifiées à RH contrôlée en utilisant une solution saturée de MgCl2 (RH ~ 31 %) sur verre traité aux UVO. *P 0,05 et ***P ≤ 0,001. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aaz7748
Lorsqu'une gouttelette fixe contenant un soluté dans un solvant volatil s'évapore, le flux dans la gouttelette peut s'assembler en motifs complexes. Les chercheurs ont examiné un tel transport dans l'évaporation de gouttelettes sessiles dans des solvants. Dans un nouveau rapport maintenant publié le Avancées scientifiques , Bryan A. Nerger et une équipe de scientifiques en génie chimique et biologique, et biologie moléculaire à l'Université de Princeton, NOUS., a démontré un écoulement dans l'évaporation de gouttelettes sessiles aqueuses contenant le polymère auto-assemblant de collagène de type I. Le matériau peut être utilisé pour concevoir des réseaux hydratés de fibres de collagène alignées. L'équipe a noté l'effet Marangoni (un terme provenant de la propagation de gouttelettes d'huile sur l'eau) pour diriger l'assemblage de fibres de collagène à travers des zones millimétriques par rapport à l'humidité environnementale et à la forme géométrique de la gouttelette. Nerger et al. incorporé et cultivé des cellules musculaires squelettiques dans les gouttelettes en évaporation pour observer leur orientation collective et leur différenciation ultérieure en myotubes en réponse aux réseaux alignés de collagène. Le travail démontre un simple, approche accordable et à haut débit pour concevoir des hydrogels fibrillaires alignés pour créer des matériaux biomimétiques chargés de cellules.
La myriade de modèles de dépôts solides qui découlent de l'écoulement de fluide entraîné par l'évaporation a été signalée pour la première fois par Robert Brown en 1828 et a ensuite été étudiée pour une variété d'applications actuelles, y compris la microfabrication et l'impression à jet d'encre. L'anneau de café ou l'écoulement radial vers l'extérieur peut également se produire lorsque le solvant est volatil, et le flux de Marangoni entraîné par la chaleur latente d'évaporation est supprimé. Les écoulements de Marangoni résultant de gradients thermiques ou induits par des solutés dans la tension superficielle peuvent également générer des écoulements en recirculation. Les chercheurs ont décrit l'écoulement dans les gouttelettes en évaporation principalement dans le contexte de particules en suspension dans des solvants qui s'évaporent complètement. Dans ce travail, Nerger et al. ont montré comment le flux dans les gouttelettes en évaporation pouvait réguler le taux d'auto-assemblage des protéines et contrôler l'alignement des réseaux de protéines fibreuses chargées de cellules. L'équipe a démontré que le flux d'évaporation de gouttelettes aqueuses de collagène de type I neutralisé générait des réseaux de fibres de collagène alignés.
Les effets Marangoni thermiques et induits par le soluté ont permis un écoulement radial dans la gouttelette en évaporation pour orienter les fibres de collagène par auto-assemblage. Les scientifiques ont ajusté l'orientation des fibres en modifiant le taux d'auto-assemblage, l'humidité ambiante et la géométrie de la gouttelette. Les cellules musculaires squelettiques incorporées dans les gouttelettes en évaporation se sont orientées et différenciées en myotubes multinucléés en réponse à l'alignement des fibres de collagène et seule une fraction de l'eau s'est évaporée de la gouttelette, donnant lieu à une construction d'hydrogel chargée de cellules. L'hydrogel résultant a de larges applications pour concevoir des échafaudages biomimétiques pour des études en ingénierie tissulaire, biologie du développement et matériaux d'auto-assemblage.
Des vidéos CRM time-lapse représentatives des mouvements de billes dans le bord, proximité, et les régions moyennes du collagène coulé par goutte. L'HR a été contrôlée à l'aide d'une solution saturée de MgCl2 (RH ~ 31 %) et les solutions de collagène ont été gélifiées sur verre traité aux UVO. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aaz7748
Auto-assemblage de fibres de collagène dans des gouttelettes de collagène en évaporation
L'équipe a coulé des solutions neutralisées de collagène de type I sur des boîtes de culture à fond de verre traitées aux ultraviolets (UV)/ozone en contrôlant l'humidité relative (HR) des boîtes de culture avant de déposer du collagène à l'intérieur de la boîte. Ils ont ensuite placé la boîte de culture dans une plus grande boîte de Pétri scellée pour initier l'auto-assemblage du collagène. Les constructions de collagène s'auto-assemblent tandis que l'eau s'évapore de la gouttelette, et l'équipe a visualisé l'orientation des fibres de collagène dans trois régions distinctes de la gouttelette, y compris le bord, près du bord, et le milieu. L'équipe a observé les orientations des fibres de collagène au sein de la gouttelette et a montré leur variation au sein des gouttelettes en évaporation.
Nerger et al. incorporé des billes fluorescentes dans les gouttelettes pour comprendre si l'orientation des fibres de collagène était en corrélation avec les modèles internes d'écoulement pendant l'évaporation. Ils ont ensuite observé le mouvement des billes et l'auto-assemblage du collagène pour suggérer que le flux de Marangoni a entraîné la recirculation au sein des gouttelettes en évaporation. Les mouvements des billes étaient cohérents avec les modèles d'alignement des fibres de collagène à travers la gouttelette. Les scientifiques ont quantifié le débit en calculant des paramètres moyennés dans le temps et l'ensemble, y compris le déplacement quadratique moyen (MSD), déplacement, et la vitesse des trajectoires des billes. Les mesures ont montré une mobilité accrue des billes dans la région proche du bord de la gouttelette, tandis que la vitesse moyenne des billes était cinq à dix fois plus élevée dans les régions de bord ou du milieu.
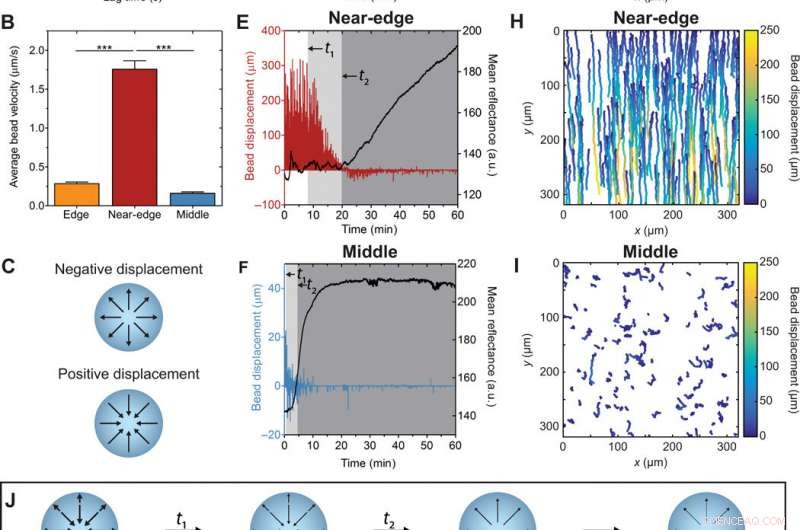
L'évaporation entraîne des schémas d'écoulement régionaux distincts, qui sont atténués par l'auto-assemblage du collagène. (A) MSD moyennée dans le temps et l'ensemble pour les trajectoires des billes. Les trajectoires dans la région médiane dépassant 300 images de longueur ont été éliminées pour améliorer l'efficacité des calculs. La pente, la descente, , représente l'exposant de la loi de puissance qui a été ajusté aux données. (B) Vitesse radiale moyenne des billes pour 500 trajectoires de billes identifiées dans chacune des trois répétitions. (C) Direction du flux radial correspondant au déplacement positif ou négatif. Déplacement radial du bourrelet dans le bord (D), (E) près du bord, et (F) les régions médianes d'une gouttelette de collagène en évaporation. Les lignes noires représentent la réflectance moyenne à 488 nm. Temps caractéristiques associés à la formation de fibres de collagène fluides, t1, et la formation d'un réseau stable de fibres de collagène, t2, sont annotées sur des plots (D à F). a.u., unités arbitraires. Trajectoires à un seul cordon codées par couleur en fonction du déplacement du cordon pour le bord (G), (H) près du bord, et (I) les régions médianes d'une gouttelette de collagène en évaporation. Les 500 premières trajectoires qui ont dépassé 20 trames de longueur dans chaque région d'intérêt sont tracées. (J) Champs d'écoulement observés dans une gouttelette en évaporation de collagène contenant des billes fluorescentes. Les solutions de collagène ont été gélifiées à RH contrôlée en utilisant une solution saturée de MgCl2 (RH ~ 31 %) sur du verre traité aux UVO. ***P 0,001. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aaz7748
Réglage de l'alignement et du diamètre des fibres de collagène
Nerger et al. ensuite exploré l'alignement des fibres de collagène dans les gouttelettes où la vitesse du flux de Marangoni était proportionnelle au taux d'évaporation. L'alignement des fibres de collagène dépendait du taux de cisaillement induit par l'écoulement. Par conséquent, l'équipe a émis l'hypothèse qu'ils pourraient régler l'alignement du collagène en ajustant la variation de l'HR (humidité relative). Le processus leur a également permis de contrôler le taux d'évaporation des gouttelettes. Ils ont testé cela en utilisant de l'eau pure et des solutions salines saturées dans la boîte de culture et ont utilisé la microscopie confocale à réflexion (CRM) pour montrer que l'alignement des fibres de collagène diminuait dans les conditions d'HR élevée fournies par l'eau ou le chlorure de sodium (NaCl). Lorsqu'ils ont diminué l'HR en utilisant du bromure de lithium (LiBr), la fraction d'alignement a diminué, tout en augmentant le diamètre du collagène en raison de la cinétique réduite d'auto-assemblage du collagène. L'HR régule l'alignement des fibres de collagène en régulant les débits. Des débits suffisamment importants pourraient donc perturber la formation d'un réseau de collagène stable. L'équipe a également fait varier le pH de la solution et en a déduit que l'alignement des fibres de collagène était fonction de la cinétique d'auto-assemblage dans une gouttelette en évaporation. Les scientifiques pourraient contrôler le modèle d'alignement du collagène en contrôlant la géométrie de la gouttelette.
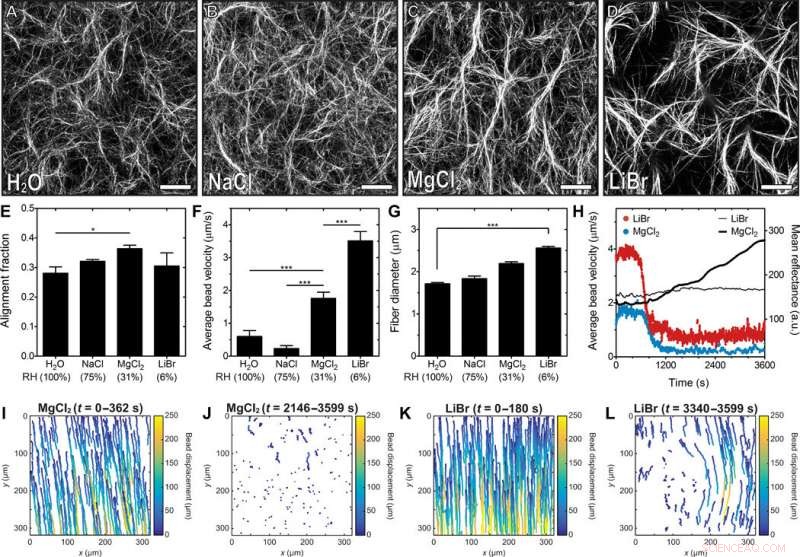
L'HR (humidité relative) affecte la fraction d'alignement et la géométrie des fibres de collagène. Images CRM représentatives dans la région proche du bord de gouttelettes de collagène auto-assemblées en présence de (A) eau (RH ~ 100 %) et de solutions saturées de (B) NaCl (RH ~ 75 %), (C) MgCl2 (HR ~ 31 %), ou (D) LiBr (HR ~ 6%). Barres d'échelle, 50 µm. (E) Fraction d'alignement des fibres de collagène dans la région proche du bord des gouttelettes de collagène. (F) Vitesse radiale moyenne des billes dans la région proche du bord des gouttelettes de collagène. La vitesse a été déterminée à partir de la moyenne de 500 trajectoires de billes. (G) Diamètre moyen des fibres de collagène dans la région proche du bord des gouttelettes de collagène. (H) Vitesse radiale moyenne des billes en fonction du temps dans la région proche du bord des gouttelettes de collagène. Les données de vitesse des billes ont été lissées en utilisant une moyenne mobile de 10. Les lignes noires représentent la réflectance moyenne à 488 nm. Déplacement des billes dans la région proche du bord des gouttelettes incubées avec des solutions saturées de (I et J) MgCl2 ou (K et L) LiBr. (I) et (K) représentent des trajectoires de billes au début d'une expérience et (J) et (L) représentent des trajectoires après le temps caractéristique t2. Le temps total pendant lequel les trajectoires sont tracées est noté au-dessus de chaque tracé. Les solutions de collagène ont été gélifiées sur du verre traité aux UVO. *P 0,05 et ***P ≤ 0,001. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aaz7748
Alignement cellulaire de structuration pour la différenciation
Les réseaux alignés de fibres de collagène peuvent généralement influencer le comportement physiologique des cellules et des tissus ainsi que les processus biologiques en tant que voie prometteuse en ingénierie tissulaire. Pour déterminer si les cellules sont restées viables sur le collagène après évaporation des gouttelettes, Nerger et al. inclus le cancer du sein humain ou les cellules musculaires squelettiques dans la solution de collagène avant la coulée et l'évaporation des gouttes. Les cellules cancéreuses du sein orientées radialement le long des fibres de collagène dans la gouttelette, et les cellules musculaires squelettiques orientées dans le sens de l'alignement des fibres de collagène. Après quatre jours de culture cellulaire, les cellules musculaires squelettiques se sont différenciées pour former des myotubes multinucléés alignés dans la direction des fibres de collagène à travers la gouttelette. Pour confirmer l'influence du collagène sur la différenciation, les scientifiques ont cultivé des cellules sur un substrat de verre dans les mêmes conditions et ont noté que les structures sarcomériques étaient par contraste plus petites et orientées de manière aléatoire. Les données ont démontré comment l'évaporation des gouttelettes de collagène modelait l'alignement et la différenciation des cellules sur des échelles de longueur millimétrique.

Vidéos CRM time-lapse représentatives de l'auto-assemblage de fibres de collagène dans le bord, près du bord, et les régions moyennes du collagène coulé par goutte. L'HR a été contrôlée à l'aide d'une solution saturée de MgCl2 (RH ~ 31 %) et les solutions de collagène ont été gélifiées sur verre traité aux UVO. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aaz7748
De cette façon, Bryan A. Nerger et ses collègues ont utilisé le flux de Marangoni généré dans l'évaporation de gouttelettes de collagène de type I pour réguler l'auto-assemblage du collagène et produire des réseaux tridimensionnels (3-D) avec un alignement des fibres accordable, diamètre et porosité. Ils ont empêché l'évaporation complète des gouttelettes pour former des réseaux de fibres de collagène hydratées 3-D pour soutenir la croissance et la différenciation des cellules de mammifères. Le système a le potentiel de générer un approche à haut débit pour incorporer des explants de tissus ou des organoïdes dans des réseaux alignés de collagène. L'approche permettra la production de constructions tissulaires alignées physiologiquement pertinentes pour de larges applications en sciences de la vie et en médecine.
© 2020 Réseau Science X