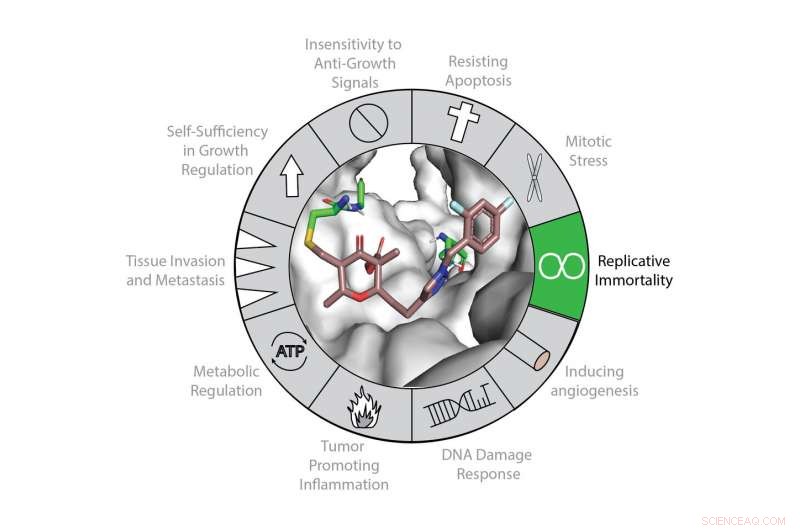
L'expression de la télomérase contribue aux "Hallmarks of Cancer" principalement par son rôle canonique dans le maintien des télomères et la mortalité réplicative. La télomérase (affichée en gris) peut être inhibée avec une nouvelle classe d'inactivateurs covalents (affichée en couleur). Crédit :Université Northwestern
L'immortalité cellulaire est l'une des caractéristiques du cancer. Un chimiste organique de la Northwestern University et son équipe ont maintenant développé un outil moléculaire prometteur qui cible et inhibe l'un des rouages sous-jacents de l'immortalité cellulaire :l'enzyme télomérase.
Cette enzyme se trouve surexprimée dans environ 90 % des cellules cancéreuses humaines et est devenue un important sujet d'étude pour les chercheurs sur le cancer. Les cellules normales ont le gène de la télomérase, mais il n'est généralement pas exprimé.
"La télomérase est la principale enzyme qui permet aux cellules cancéreuses de vivre éternellement, " a déclaré Karl A. Scheidt, qui a dirigé la recherche. "Nous voulons court-circuiter cette immortalité. Nous avons maintenant conçu une petite molécule unique en son genre qui se lie de manière irréversible à la télomérase, l'arrêt de son activité. Ce mécanisme offre une nouvelle voie pour traiter le cancer et comprendre le vieillissement cellulaire."
Scheidt est professeur de chimie au Weinberg College of Arts and Sciences et professeur de pharmacologie à la Northwestern University Feinberg School of Medicine.
La grande idée de la conception de petites molécules est venue de la nature. Il y a une décennie, Scheidt a été intrigué par l'activité biologique de la chloractomycine, qui est produit par des bactéries et il a été démontré qu'il inhibe la télomérase.
Scheidt et son équipe ont utilisé la chloractomycine comme point de départ dans la conception de leurs petites molécules. Ils ont produit plus de 200 composés au fil des ans, et le composé qu'ils appellent NU-1 était le plus efficace de ceux testés. Sa synthèse est très efficace, faire moins de cinq pas.
"NU-1 inhibe la télomérase contrairement à tout ce qui l'a précédé, " a déclaré Scheidt. " Il le fait en formant une liaison covalente. Un autre avantage de NU-1 est que sa structure moléculaire devrait permettre aux scientifiques d'ajouter du fret, comme une thérapeutique. »
L'étude a été publiée la semaine dernière par la revue ACS Biologie Chimique .
Toutes les cellules humaines ont des télomères, courtes séquences d'ADN qui coiffent les extrémités de chaque brin d'ADN. Leur travail consiste à protéger nos chromosomes et notre ADN. Lorsqu'une cellule se divise, les télomères raccourcissent jusqu'à ce qu'ils ne puissent plus faire leur travail. La mort cellulaire naturelle s'ensuit.
En revanche, cellules cancéreuses, avec leur activité télomérase accrue, devenir immortel en inversant le processus normal de raccourcissement des télomères. L'enzyme télomérase copie les télomères encore et encore, allonger les télomères. Le résultat est une division cellulaire illimitée et l'immortalité. Les fameuses cellules HeLa, isolé du tissu de cancer du col d'Henrietta Lacks dans les années 1950, se divisent encore.
La télomérase est une cible de la recherche thérapeutique contre le cancer depuis des décennies. En 2009, trois scientifiques ont reçu le prix Nobel de physiologie ou médecine pour leurs recherches antérieures sur les télomères et la télomérase.
Après avoir développé leurs nouveaux composés, Scheidt et son équipe ont initié des collaborations avec le professeur Stephen Kron à l'Université de Chicago et Scott Cohen au Children's Medical Research Institute de Sydney pour étudier le rôle extra-télomérique de l'inhibition de la télomérase.
Les études se sont concentrées sur la façon dont les nouveaux composés interagissent avec la télomérase au niveau moléculaire et comment l'inhibition de la télomérase sensibilise les cellules aux chimiothérapies et à l'irradiation. De ce travail, NU-1 a atteint le sommet.
« En publiant cette étude, nous testons cet outil exquis pour voir ce qu'il peut faire et en savoir plus sur la télomérase, " Scheidt a déclaré. "Nous continuons également à l'améliorer."
La recherche a été effectuée sur des cellules humaines. Les prochaines étapes, Scheidt a dit, sont de fabriquer des composés plus puissants et de les étudier dans des modèles animaux.