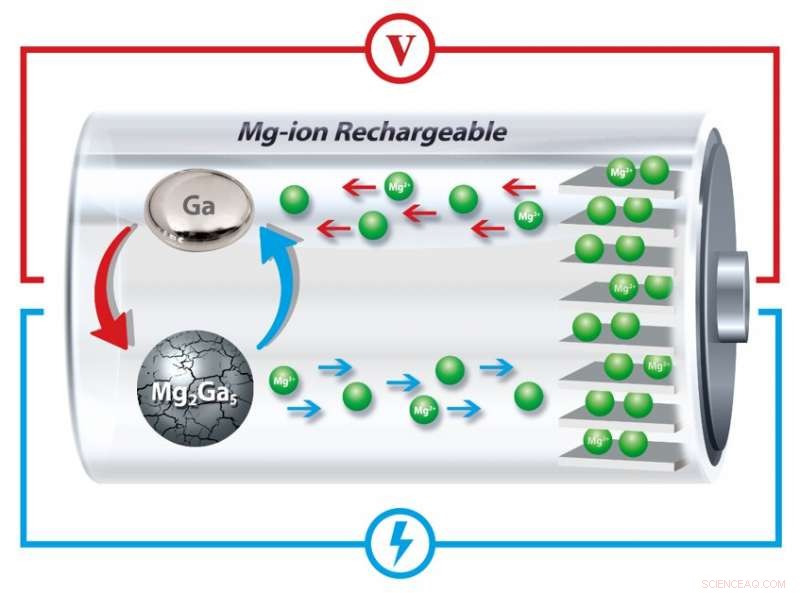
Dans la nouvelle conception d'anode des chercheurs, le gallium fond et se solidifie à plusieurs reprises, « cicatriser » les fissures qui, autrement, diminueraient progressivement la capacité de la batterie à maintenir une charge. Crédit :Université de Pennsylvanie
Les batteries lithium-ion rechargeables (Li-ion) sont une technologie révolutionnaire, trouvé dans tout, des téléphones portables aux voitures. Leur omniprésence et leur rôle dans la rupture de la dépendance aux combustibles fossiles ont valu à un trio de chercheurs le prix Nobel de chimie cette année.
Mais même si la technologie des batteries Li-ion est reconnue par l'un des meilleurs prix de la science, la chimie derrière eux fait face à un défi imminent. Les batteries lithium-ion ne peuvent pas être rechargées indéfiniment; les matériaux des électrodes de ces batteries se dilatent et se fissurent à chaque cycle, diminuant progressivement leurs performances de stockage jusqu'à ce qu'elles soient inutiles. La demande de lithium frais qui en résulte, le cobalt et d'autres éléments nécessaires mettent à rude épreuve les ressources naturelles.
Avec ce défi en tête, Les ingénieurs de Penn cherchent à concevoir des électrodes de batterie rechargeables capables de fonctionner efficacement avec des ions métalliques autres que le lithium. Les batteries magnésium-ion sont une alternative prometteuse, mais les matériaux qui peuvent stocker de manière réversible le magnésium ont jusqu'à présent été encore plus sensibles à la fissuration et à d'autres problèmes que leurs cousins Li-ion.
Les chercheurs de Penn ont maintenant trouvé une solution en incorporant du gallium, un métal dont le point de fusion est supérieur de quelques degrés à la température ambiante, dans l'anode d'une batterie magnésium-ion. En fondant et en se solidifiant à chaque cycle de charge et de décharge, ces anodes peuvent « guérir » la fissuration et l'expansion ultérieure qui dégradent normalement le stockage des batteries rechargeables.
Leurs expériences montrent que cette nouvelle anode prolonge considérablement la durée de vie des batteries magnésium-ion, et le fait sans avoir besoin de matériaux nanométriques coûteux. Ces caractéristiques pourraient faire des batteries magnésium-ion un bon choix pour les applications à grande échelle, pression sur les ressources en lithium.
Les chercheurs ont démontré leur anode à base de gallium dans une étude publiée dans Matériaux énergétiques avancés .
L'étude a été dirigée par Eric Detsi, Professeur adjoint à terme Stephenson au Département de science et génie des matériaux, avec Lin Wang et Samuel Welborn, étudiants diplômés dans son laboratoire. Ils ont collaboré avec Vivek Shenoy, Eduardo D. Glandt, professeur distingué du président au Département de science et génie des matériaux.
"Pour la plupart des véhicules électriques, le poids de la batterie représente environ un cinquième du poids total du véhicule. Compter uniquement sur les batteries lithium-ion pour alimenter ces véhicules dans le monde entier mettra à rude épreuve les ressources de lithium et de cobalt utilisées dans les batteries, " dit Detsi. " Ils deviennent déjà plus chers en raison de la demande, et le marché mondial du cobalt dépend fortement des approvisionnements en provenance de pays à haut risque géopolitique. »
« Il est évident que des technologies alternatives de batteries sont nécessaires, " dit-il. " Ne pas remplacer le lithium, mais pour soutenir le lithium."
Charger et décharger une batterie implique des réactions chimiques qui permettent aux ions de se déplacer d'une électrode de la batterie à l'autre, gagner ou libérer des électrons dans le processus. Cependant, toute personne possédant un téléphone portable ou un ordinateur portable vieillissant sait que ces batteries perdent leur capacité à conserver une charge au fil du temps. L'une des principales raisons pour lesquelles ces batteries échouent est que le cycle de charge et de décharge implique une transformation physique des matériaux des électrodes. Lorsque des ions sont incorporés dans l'électrode, ces matériaux se dilatent, et lorsque les ions sont libérés de l'électrode, les matériaux se fissurent. Ce processus se poursuit jusqu'à ce que les matériaux se brisent et perdent physiquement le contact électrique avec les électrodes, rendant la batterie inutilisable.
"Le changement de volume qui se produit dans la plupart des matériaux d'électrode en raison de l'incorporation et de la libération d'ions conduit à la fissuration et à la pulvérisation. C'est l'une des choses qui tuent une batterie, " dit Wang. " Cette pulvérisation est associée à l'accumulation de contraintes qui accompagne une transformation en phase solide-solide. "
« Dans notre nouveau travail, cependant, " Welborn dit, "au lieu d'une transformation d'un type de solide en un autre, le matériau solide d'origine se transforme en liquide. Cela inhibe la fissuration et la pulvérisation car les contraintes associées à la transformation solide-solide normale ne sont plus présentes."
À température ambiante, le gallium pur est un malléable, métal argenté qui pourrait facilement être confondu avec de l'aluminium ou du nickel. Tenant un peu dans votre main, cependant, révèle rapidement une propriété unique :avec un point de fusion de 85 degrés Fahrenheit, la température corporelle est suffisante pour transformer un morceau solide de gallium en un liquide semblable au mercure.
Dans la nouvelle étude des chercheurs, le gallium se présente sous une forme solide car il est allié au magnésium en particules de la taille d'un micron.
"Afin de connecter électroniquement ces petites pièces, " Wang dit, "on les met dans un réseau conducteur de fibres de carbone, du noir de carbone et du graphène qui sont tous liés ensemble avec un liant."
Lorsque les ions magnésium se séparent du gallium, il se transforme en son état liquide car la batterie fonctionne à des températures légèrement supérieures au point de fusion du gallium.
« Comme il est regroupé dans ce réseau d'autres matériaux, " Welborn dit, "quand le gallium passe du solide au liquide, il ne bouge pas comme on pourrait s'y attendre d'un liquide."
En utilisant des rayons X pour examiner la structure cristalline des matériaux à l'intérieur de la batterie, les chercheurs ont montré que lorsque la batterie se charge, les ions retournent à l'anode et reforment des particules solides de gallium-magnésium.
De manière critique, puisque ces particules sont reconstituées à chaque cycle, ils ne subissent pas le genre de fissuration qui finit par dégrader les autres batteries.
La batterie expérimentale des chercheurs a résisté à plus d'un millier de cycles de charge, environ cinq fois plus que la batterie magnésium-ion de pointe actuelle.
« Les mille cycles démontrés dans ce travail représentent une amélioration significative, " Detsi dit, "mais notre rêve est de profiter de ce comportement d'auto-guérison unique pour concevoir une batterie qui peut être chargée et déchargée pour toujours."
La limite de la durée de vie de mille cycles de la nouvelle batterie n'est pas due à l'électrode, mais plutôt l'électrolyte, le milieu liquide qui déplace les ions d'une électrode à l'autre. Des recherches antérieures du groupe Detsi ont montré le rôle de l'électrolyte dans la dégradation lente des électrodes de la batterie, et les travaux futurs se concentreront sur la façon d'améliorer ce processus.
Heureusement, comme pour la conception des électrodes auto-cicatrisantes de l'étude, travailler sur cet aspect de la conception des batteries implique des applications intelligentes de la chimie, plutôt que des techniques de nanotechnologie au coût prohibitif, d'autres tentatives d'allongement de la durée de vie de la batterie impliquent.
"Pour résoudre les problèmes avec les batteries lithium-ion, la communauté des batteries utilise couramment des nanomatériaux, " dit Detsi. " Cependant, la synthèse des nanomatériaux peut être complexe, ce qui signifie que la fabrication de tonnes de nanomatériaux à l'échelle industrielle pour des applications de batterie peut être très coûteuse. Une chose remarquable avec notre conception est qu'il n'est pas nécessaire d'utiliser des nanomatériaux, ce qui rend cette classe de batteries très attrayante pour les applications à grande échelle."