Crédit :Université RUDN
Les bio-ingénieurs de l'Université RUDN ont créé des nanoconteneurs magnétiques pour l'administration intelligente de médicaments aux organes ou tissus souhaités, ce qui réduit le risque d'effets secondaires. Une expérience sur des souris a déterminé que les nanoconteneurs ne sont pas toxiques. Les résultats de l'étude sont publiés dans la revue Polymères .
Les effets secondaires pharmaceutiques se produisent souvent parce que la substance active du médicament pénètre dans les organes sains. C'est pourquoi, par exemple, la chimiothérapie est si difficile pour les patients dans le traitement du cancer :les médicaments toxiques n'affectent pas seulement les cellules tumorales, mais tout le corps. Les systèmes d'administration de médicaments ciblés résolvent ce problème. De nombreux vecteurs potentiels ont été proposés ces dernières années :des microcapsules à enveloppe de polyélectrolytes, des liposomes artificiels à l'échelle micro et nanométrique, et des nanoparticules de protéines, par exemple. Plusieurs dizaines de médicaments conditionnés dans de tels conteneurs sont déjà utilisés en pratique ou sont en cours d'essais cliniques.
Cependant, il existe encore de nombreux problèmes qui empêchent l'utilisation généralisée des transporteurs intelligents. La première est que la dépendance du processus de biodistribution du médicament dans les tissus dicte la taille des conteneurs. Plus la taille est petite, plus la probabilité que le médicament atteigne le bon organe est grande, et plus la dose du médicament est faible, réduire les effets toxiques. Un autre problème est le manque d'informations sur la toxicité, effets sur le corps et distribution dans les tissus vivants. Ces deux problèmes ont été résolus avec succès par les biochimistes de l'Université RUDN en collaboration avec des collègues de Russie et du Royaume-Uni.
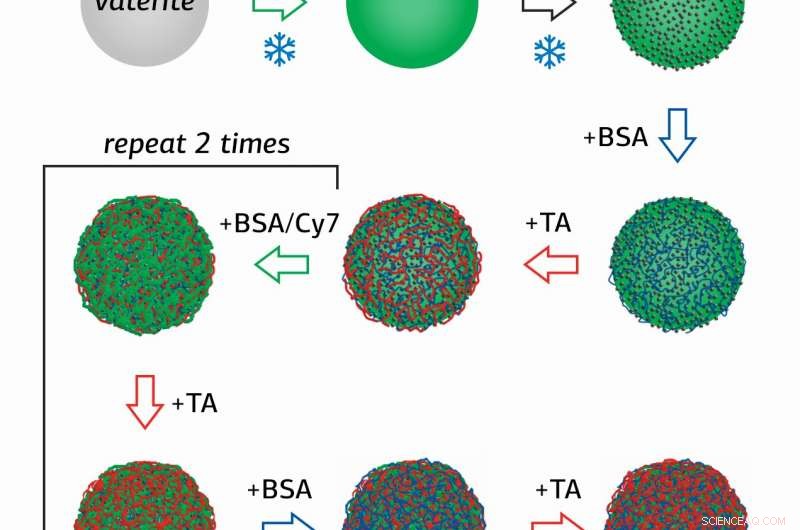
La chercheuse du Laboratoire d'ingénierie de surface de l'Université RUDN Olga Sindeeva et ses co-auteurs ont créé des conteneurs magnétiques sensibles à l'échelle submicronique – des particules de 400 à 600 nanomètres, avec une coquille de plusieurs couches d'albumine de sérum bovin (BSA) avec une étiquette fluorescente Cy7, et l'acide tannique (AT).
La nouveauté de l'étude réside dans la méthode d'obtention des contenants, dans laquelle des nanoparticules de magnétite (MNP), oxyde de fer mixte (II, III) ont d'abord été adsorbés à la surface de granules poreux de carbonate de calcium, qui ont ensuite été enduites séquentiellement de plusieurs couches de BSA-Cy7 et TA. Puis, Le carbonate de calcium a été lavé des conteneurs en utilisant une solution aqueuse avec un agent chélatant.
« Avec cette méthode, il a été possible de doubler la quantité de magnétite dans les conteneurs par rapport à ce qui est obtenu par les méthodes d'adsorption et de co-dépôt. Ainsi, il est possible d'augmenter le moment magnétique des nanoconteneurs et d'augmenter la vitesse de leur déplacement dans le système vasculaire, " a expliqué Olga Sindeeva.
Les bio-ingénieurs de l'Université RUDN s'attendent à ce que la taille submicronique des conteneurs augmente la biodisponibilité du médicament chargé dans le conteneur MNP (BSA-Cy7-TA).
Expériences préliminaires sur deux lignées cellulaires, HeLa et fibroblastes, ont montré que les conteneurs n'affectent pas la viabilité cellulaire et peuvent être utilisés in vivo.
Les contenants sans médicament ont ensuite été testés sur des souris BALB/c vivantes des deux sexes pesant environ 20 grammes, 10 individus par groupe. Des récipients sous forme de suspension en solution saline ont été injectés dans la veine caudale de souris anesthésiées. Une suspension de conteneurs sans magnétite (BSA-Cy7-TA) a été utilisée comme témoin. Puis, l'une des pattes postérieures des souris a été exposée à un champ magnétique pendant une heure tandis que l'autre a été laissée libre pour comparaison. La distribution des nanoconteneurs dans les tissus de souris vivantes a été observée en utilisant l'imagerie par résonance magnétique (IRM) et la tomographie par fluorescence. L'analyse magnétométrique et l'examen histologique des tissus de souris post mortem ont également été effectués une heure après le retrait de l'aimant.
Des biologistes de l'Université RUDN ont montré que dans les vaisseaux périphériques des membres postérieurs au repos à faible débit sanguin, Les particules MNPs (BSA-Cy7-TA) se déplacent dans la première heure après l'injection intraveineuse en direction du membre auquel l'aimant est attaché.
L'IRM a montré que la concentration de magnétite dans le muscle près de l'aimant passe par le maximum. La quantité de magnétite s'est avérée être 70 pour cent plus élevée que dans le membre libre. Puis, le signal de magnétite est tombé aux valeurs de fond.
D'après les résultats des études histologiques et de la magnétométrie, les chercheurs ont découvert que les MNP (BSA-Cy7-TA) se concentraient principalement dans les poumons, et, dans une moindre mesure, dans le foie et la rate. De plus, leur concentration dans les poumons était quatre à cinq fois plus élevée. Une petite quantité du transporteur a également été trouvée dans d'autres organes internes et muscles, mais la concentration était significativement plus faible que dans les poumons. Ainsi, les biochimistes ont conclu que la distribution des récipients intraveineux dépend de l'apport sanguin aux organes, C'est, sur la vitesse du flux sanguin, mais est sensible à la localisation du champ magnétique.
Une attention particulière a été portée à la toxicité des récipients intraveineux et à leurs effets sur l'organisme. Des tests préliminaires ont montré qu'in vitro dans le plasma ou le sang, un pourcentage important des conteneurs est détruit au cours d'une journée. Les résultats des études suggèrent que les conteneurs ont le temps d'atteindre l'objectif avec l'injection intraveineuse. Puis, en changeant le signal de fluorescence, les particules porteuses se dégradent progressivement et sont excrétées par le corps.
Les particules sont non toxiques et hémocompatibles, et leur taille leur permet de pénétrer les tissus du corps, mais à doses de travail, ils ne nuisent pas au système respiratoire ou circulatoire, et n'affectent pas les fonctions rénales ou hépatiques. L'activation du système du complément nécessaire à la biodégradation de la membrane protéique des récipients n'affecte pas le taux de leucocytes, et n'entraîne donc pas d'inflammation systématique notable.
Ainsi, les chercheurs de l'Université RUDN ont pu concevoir et distribuer des conteneurs avec une grande quantité de magnétite dans le corps, et gérer efficacement leur déploiement à l'aide d'un champ magnétique.
À l'avenir, les participants au projet ont l'intention de créer des nanocapsules intelligentes qui peuvent délivrer le médicament au bon organe et s'ouvrir pour libérer la substance active. Cette méthode d'administration du médicament permettrait d'éviter les effets secondaires du traitement. Les patients atteints de diverses maladies, y compris les enfants ou les personnes âgées en mauvaise santé, pourrait être traité à l'aide de médicaments qui pourraient autrement être évités en raison d'effets secondaires qui aggravent l'état du patient.