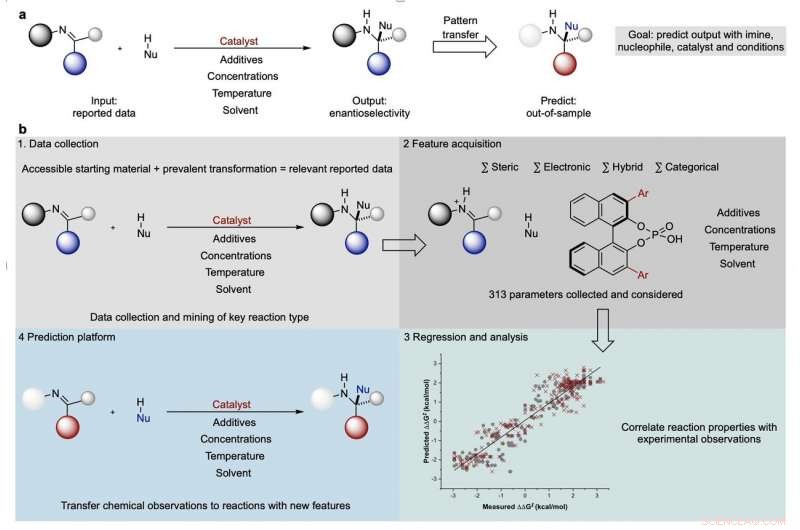
Le processus de développement de modèles prédictifs de réactions chimiques. Crédit :Jolene Reid et Matthew Sigman.
La chimie est plus que le simple mélange du composé A avec le composé B pour faire le composé C. Il existe des catalyseurs qui affectent la vitesse de réaction, ainsi que les conditions physiques de la réaction et toutes les étapes intermédiaires qui conduisent au produit final. Si vous essayez de créer un nouveau processus chimique pour, dire, recherche pharmaceutique ou de matériaux, vous devez trouver le meilleur de chacune de ces variables. C'est un processus d'essais et d'erreurs qui prend du temps.
Ou, au moins, c'était.
Dans une nouvelle publication en La nature , Les chimistes de l'Université de l'Utah, Jolene Reid et Matthew Sigman, montrent comment l'analyse des données de réactions chimiques précédemment publiées peut prédire comment des réactions hypothétiques peuvent se dérouler, rétrécissant l'éventail des conditions que les chimistes doivent explorer. Leur processus de prédiction algorithmique, qui comprend des aspects de l'apprentissage automatique, peut économiser un temps et des ressources précieux dans la recherche chimique.
"Nous essayons de trouver la meilleure combinaison de paramètres, " dit Reid. " Une fois que nous avons cela, nous pouvons ajuster les caractéristiques de n'importe quelle réaction et prédire comment cet ajustement l'affectera. "
Essai et erreur
Précédemment, des chimistes qui voulaient faire une réaction qui n'avait pas été essayée auparavant, comme une réaction pour attacher une petite molécule particulière à un endroit particulier sur une molécule plus grosse, a abordé le problème en recherchant une réaction similaire et en imitant les mêmes conditions.
« Presque à chaque fois, Tout du moins selon moi, ça marche pas bien, " Sigman dit. "Alors vous changez systématiquement les conditions."
Mais avec plusieurs variables dans chaque réaction - Sigman estime environ sept à 10 dans une réaction pharmaceutique typique - le nombre de combinaisons possibles de conditions devient écrasant. "Vous ne pouvez pas couvrir tout cet espace variable avec n'importe quel type d'opération à haut débit, " dit Sigman. "Nous parlons de milliards de possibilités."
rétrécir le champ
Donc, Sigman et Reid ont cherché un moyen de se concentrer sur une gamme de conditions plus gérable. Pour leur test de réaction, ils ont examiné des réactions impliquant des molécules avec des images miroir opposées les unes des autres (de la même manière que vos mains droite et gauche sont des images miroir l'une de l'autre) et qui sélectionnent plus pour une configuration que pour une autre. Une telle réaction est dite "énantiosélective, " et le laboratoire de Sigman étudie les types de catalyseurs impliqués dans les réactions énantiosélectives.
Reid a recueilli des rapports scientifiques publiés sur 367 formes de réactions impliquant des imines, qui ont une base azotée, et utilisé des algorithmes d'apprentissage automatique pour corréler les caractéristiques des réactions avec leur sélectivité pour les deux formes différentes d'imines. Les algorithmes ont examiné les catalyseurs des réactions, solvants et réactifs, et construit des relations mathématiques entre ces propriétés et la finale sélective de la réaction.
"Il y a un motif caché sous la surface expliquant pourquoi cela fonctionne et ne fonctionne pas avec cette condition, ce catalyseur, ce substrat, etc, " dit Sigman.
"La clé de notre succès est que nous utilisons les informations provenant de nombreuses réactions, " ajoute Reid.
Soulager la douleur
Dans quelle mesure leur modèle prédictif fonctionne-t-il bien ? Il a prédit avec succès les résultats de 15 réactions impliquant un réactif qui n'était pas dans l'ensemble d'origine, et les résultats de 13 réactions où à la fois un type de réactif et de catalyseur n'étaient pas dans l'ensemble d'origine. Finalement, Reid et Sigman ont examiné une étude récente qui a mené 2, 150 expériences pour trouver les conditions optimales de 34 réactions. Sans salir un seul bécher, Le modèle de Reid et Sigman est arrivé aux mêmes résultats et au même catalyseur optimal.
Reid attend avec impatience d'appliquer le modèle pour prédire des réactions impliquant de grandes, molécules complexes. "Souvent, vous constatez que les nouvelles méthodologies ne sont pas adaptées à des systèmes complexes, " dit-elle. " Nous pourrions peut-être le faire maintenant en prédisant à l'avance le meilleur type de catalyseur. "
Sigman ajoute que les modèles prédictifs peuvent réduire les obstacles au développement de nouveaux médicaments.
"L'industrie pharmaceutique ne veut pas investir de l'argent dans quelque chose dont elle ne sait pas si ça va marcher, " dit-il. " Alors, si vous avez un algorithme qui suggère que cela a une forte probabilité de fonctionner, tu soulages la douleur."
Après parution, retrouvez l'étude complète ici.