
La pulvérisation de sel sur les routes est une mesure de sécurité. Crédit:stoatphoto/Shutterstock.com
Brrr… il fait froid dehors ! Les enfants affluent vers la télévision dans l'espoir d'entendre qu'il y aura un jour de neige; les allées du pain et du lait des épiceries sont vides en raison d'une tempête de neige imminente; et des camions utilitaires pulvérisent du sel ou de l'eau salée sur les routes.
Nous savons tous pourquoi les deux premiers se produisent – les enfants sont ravis d'une journée de congé remplie de chocolat chaud et de bonhommes de neige. Les adultes font le plein de produits de première nécessité. Mais qu'est-ce qui se passe avec ces camions ?
Ils s'efforcent de protéger les conducteurs des conditions glissantes en pulvérisant du sel gemme ou une solution d'eau salée pour empêcher la formation de glace. Ce sel est très similaire au sel que vous avez sur votre table - c'est le même chlorure de sodium, NaCl. Certains mélanges exclusifs contiennent d'autres sels, tels que le chlorure de potassium (KCl) et le chlorure de magnésium (MgCl), mais ils ne sont pas aussi couramment utilisés.
Le sel de voirie n'est pas aussi pur que celui que vous utilisez sur votre nourriture; il a une couleur gris brunâtre, principalement en raison de la contamination minérale. Soumettre l'environnement à ce sel par ruissellement peut avoir des conséquences inattendues, notamment des effets négatifs sur les plantes, les animaux aquatiques et les zones humides.
Mais c'est un moyen peu coûteux et efficace de protéger les routes du verglas grâce à un principe scientifique simple :l'abaissement du point de congélation des solutions. Le point de congélation de l'eau pure, la température à laquelle il devient de la glace, est de 32 degrés Fahrenheit. Alors s'il y a de la neige, grésil ou pluie verglaçante et le sol est de 32 F ou plus froid, de la glace solide se formera sur les rues et les trottoirs.
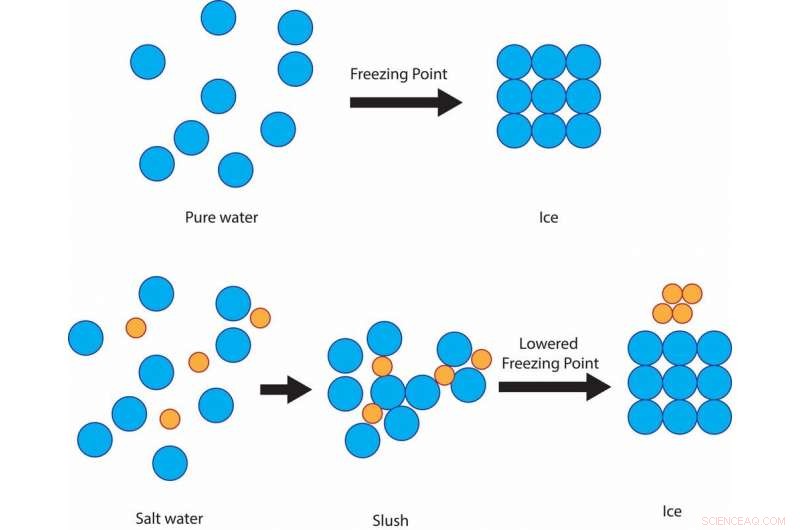
Le sel empêche les molécules d'eau de se solidifier en cristaux de glace à 32 F, au lieu de rester dans la neige fondante à cette température, avant de finalement geler aux alentours de 15 F. Crédit :Julie Pollock, CC BY-ND
Si l'eau est mélangée avec du sel, bien que, la température de congélation de la solution est inférieure à 32 F. Le sel entrave la capacité des molécules d'eau à former des cristaux de glace solides. Le degré d'abaissement du point de congélation dépend de la salinité de la solution.
Il est important de noter que le sel doit être en solution avec de l'eau liquide pour que ce principe soit respecté. C'est pourquoi de nombreuses villes vaporisent une solution saline avant la formation de glace.
Le sel déversé sur la glace dépend du soleil ou de la friction des pneus de voiture qui roulent dessus pour faire fondre la glace en une neige fondante qui peut se mélanger au sel et ne pas recongeler ensuite. Le prétraitement avec du sel solide repose sur la surface plus chaude de la route pour faire fondre initialement la neige ou la pluie verglaçante afin qu'elle puisse se mélanger correctement avec le sel. C'est aussi pourquoi le prétraitement des ponts - qui sont plus froids que les autres routes - ne fonctionne généralement pas, et pourquoi vous voyez des panneaux "le pont gèle avant la route".
Ces solutions salines diminuent la température de congélation de l'eau à environ 15 F. Ainsi, malheureusement pour les personnes confrontées à des températures vraiment glaciales, traiter avec du sel n'éliminera pas la glace sur leurs routes.
Une stratégie alternative utilisée à ces températures plus basses consiste à mettre du sable sur la glace. Le sable ne change pas la température de fusion, il fournit simplement une surface rugueuse à vos pneus pour éviter de glisser et de glisser.
La science de l'abaissement du point de congélation peut être appliquée à n'importe quelle solution, et de nombreux groupes de recherche se sont concentrés sur le développement d'alternatives ayant moins de conséquences environnementales négatives. Ils comprennent des additifs tels que la mélasse et le jus de betterave. Alors peut-être que vous pouvez vous attendre à nettoyer non seulement le sel blanc du bas de votre jean après une promenade hivernale, mais aussi du sel rose.
Cet article est republié à partir de The Conversation sous une licence Creative Commons. Lire l'article original. 