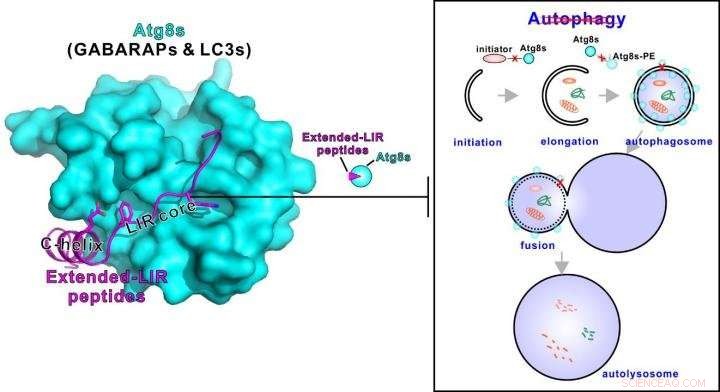
Ce résumé visuel présente les peptides de liaison Atg8s super puissants qui peuvent inhiber efficacement l'autophagie. Crédit :Division des sciences de la vie, HKUST
Autophagie, signifiant « se manger soi-même » en grec, est un mécanisme métabolique général caractéristique de presque toutes les espèces eucaryotes, de la levure unicellulaire à l'homme. C'est un processus par lequel les cellules dégradent les composants inutiles pour le recyclage des matériaux et la production d'énergie pour survivre au stress ou maintenir l'homéostasie.
L'autophagie peut protéger les cellules en éliminant les substances nocives comme les agents pathogènes et les agrégats amyloïdes dans les maladies neurodégénératives, mais les défauts de l'autophagie sont souvent liés à des maladies telles que la maladie d'Alzheimer ou la maladie de Parkinson; en cas de tumeurs, la voie de l'autophagie peut être détournée pour fournir suffisamment de nutriments pour une croissance massive. Par conséquent, activer ou inhiber l'autophagie d'une manière précisément contrôlée dans l'espace et le temps pourrait être un traitement prometteur contre divers types de maladies.
Récemment, une équipe de recherche dirigée par le biologiste structurel Prof. Mingjie Zhang de HKUST a découvert des peptides inhibiteurs puissants et spécifiques pour cibler les protéines de la famille Atg8 (y compris les LC3 et les GABARAP), composants centraux de la voie de l'autophagie. Ces peptides inhibiteurs de l'autophagie génétiquement codables peuvent être utilisés pour occlure spatio-temporellement l'autophagie chez les animaux vivants, ce qui conduit à de nombreuses situations où ils peuvent être utilisés dans une variété de conceptions.
Leurs conclusions ont été publiées le 4 juin 2018 dans la revue Nature Chimie Biologie .
Au cours de leur étude sur les ankyrines, un intérêt à long terme pour leur laboratoire, les chercheurs ont d'abord identifié un peptide inhibiteur sélectif de GABARAP naturellement hébergé dans l'ankyrine-G de 270/480 kDa et un peptide inhibiteur super puissant du pan-Atg8 à partir de l'ankyrine-B de 440 kDa. Sur la base des structures cristallines qu'ils ont résolues, ils ont encore optimisé le peptide dérivé de l'ankyrine-G pour qu'il soit plus sélectif pour le GABARAP. "La fonction distincte des LC3 et des GABARAP dans la voie de l'autophagie est encore un domaine largement ouvert. Au stade actuel, la fonction tardive de ces protéines est toujours masquée par leur effet précoce et/ou leur redondance. Les peptides développés ici serviront probablement d'un excellent outil pour disséquer les différents rôles de ces deux sous-familles de protéines Atg8 dans l'autophagie, " a déclaré le professeur Hong Zhang, l'un des principaux co-auteurs de cet article de l'Institute of Biophysics, Académie chinoise des sciences.
Les chercheurs ont également fourni la preuve que les peptides qu'ils ont développés peuvent bloquer efficacement l'autophagie dans les cellules COS7 en culture ainsi que chez les animaux vivants C. elegans à un moment et à un endroit donnés. « Les peptides de liaison Atg8 super puissants sont génétiquement codables et peuvent être exprimés de manière spécifique aux tissus et au temps chez les animaux vivants, comme nous l'avons démontré, et sont donc bien meilleurs que tous les médicaments à base de petites molécules existant dans la recherche sur l'autophagie dans les cultures cellulaires et, plus important encore, chez les animaux vivants, ", a déclaré le professeur Mingjie Zhang.
"Les peptides inhibiteurs peuvent directement servir de pistes pour développer des médicaments pour des traitements potentiels contre le cancer. Ils peuvent également être indirectement utilisés comme outil de recherche pour rechercher des inducteurs de l'autophagie pour le traitement des maladies neurodégénératives, " dit Jianchao Li, l'un des principaux auteurs du laboratoire du professeur Mingjie Zhang.