La compréhension des phénomènes biologiques à partir d'une approche multidisciplinaire permet le développement et l'optimisation de matériaux bioinspirés. Crédit :Ingénierie Bioinspirée
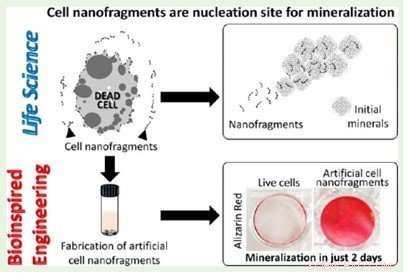
L'éclatement des cellules formant le cartilage est associé à une minéralisation au cours des premiers stades de la formation osseuse, et des nanofragments des membranes cellulaires peuvent servir de sites de nucléation pour le phosphate de calcium amorphe, comme indiqué dans deux études qui viennent d'être publiées dans Biologie intégrative et ASC Science et Ingénierie des Biomatériaux .
Le cartilage a une fonction d'échafaudage très importante pour le développement des os; lors de l'ossification endochondrale, les chondrocytes, les cellules formant le cartilage, sécrètent des protéines matricielles et des facteurs de minéralisation qui optimisent l'environnement pour la minéralisation. Les mécanismes de la formation osseuse ne sont pas complètement élucidés, et la manipulation de la minéralisation est encore difficile. La maîtrise de ce processus est pertinente car elle permettrait d'améliorer les techniques de bio-ingénierie pour la synthèse et la reconstruction des tissus cartilagineux, et pour le contrôle de la formation osseuse.
Pour mieux comprendre les étapes initiales de la formation minérale, Le professeur Takuya Matsumoto et le professeur assistant Emilio Satoshi Hara de la Graduate School of Medicine de l'Université d'Okayama, La dentisterie et les sciences pharmaceutiques ont étudié la formation osseuse dans l'épiphyse du fémur (c'est-à-dire l'extrémité arrondie de l'os) chez la souris au cours de l'ossification secondaire dans les premiers jours postnatals.
Dans une première étude, les chercheurs ont observé que les chondrocytes éclataient près de la zone minéralisée, qu'ils suggèrent pourrait être un mécanisme de création d'espace pour l'expansion minérale. L'espace créé après l'éclatement cellulaire correspond en effet bien à celui occupé plus tard par les minéraux à la fin du processus, comme le montrent les images en accéléré du processus initial de formation osseuse. Pour démontrer le lien entre l'éclatement et la formation et l'expansion minérales, Le professeur Matsumoto et ses collègues ont utilisé des stimuli externes pour induire l'éclatement et manipuler la formation du tissu osseux. En particulier, deux facteurs externes étaient liés au déclenchement de l'éclatement :la pression mécanique et la pression osmotique. En effet, la culture ex-vivo de l'épiphyse fémorale en condition hypotonique ou sous pression mécanique a favorisé la formation minérale, et des études in-vivo sur le rôle de la pression mécanique ont montré qu'une pression réduite sur les articulations entraîne une suppression de la formation osseuse dans l'épiphyse du fémur.
Dans la recherche présentée dans le deuxième article, les scientifiques ont utilisé une variété de techniques pour observer les changements dynamiques de la matière organique et inorganique dans le cartilage d'une manière spécifique au temps et à l'étape, confirmant que les premières étapes de la minéralisation reposent sur l'activité des chondrocytes. Une analyse minutieuse des nanofragments observés près de la zone minéralisée a révélé qu'il s'agissait de nanofragments de membrane de chondrocytes, et pourraient être les sites de nucléation du phosphate de calcium amorphe, qui se sont ensuite transformés en cristaux d'apatite. Les phospholipides contenus dans les fragments pourraient fournir le phosphate nécessaire à ce processus. Les chercheurs ont également synthétisé des nanofragments de cellules artificielles, et ont montré qu'ils favorisent la formation de minéraux in vitro.
Le contrôle de l'éclatement des chondrocytes au moyen de stimuli externes pourrait déboucher sur de nouvelles approches de l'ingénierie du cartilage et du tissu osseux. De plus, parce que les nanofragments de membrane cellulaire fournissent des sites de nucléation pour la formation minérale, ceux-ci pourraient être utilisés pour manipuler la biominéralisation, comme le commentent les auteurs :« la manipulation de l'éclatement des chondrocytes avec des stimuli mécano-chimiques externes pourrait être une approche supplémentaire pour l'ingénierie du cartilage et du tissu osseux, " et " à l'avenir, des matériaux à base de fragments de membrane cellulaire peuvent également être développés et appliqués dans l'ingénierie et la régénération des tissus osseux".
Il existe deux types de centres d'ossification, primaire et secondaire. Le centre d'ossification primaire apparaît au cours du développement prénatal, tandis que le centre d'ossification secondaire apparaît pendant les années postnatales et adolescentes. Dans les os longs, le centre d'ossification primaire se situe dans la partie centrale de l'os, le centre d'ossification secondaire aux extrémités.
Deux processus conduisent à la formation de tissu osseux :l'ossification intramembraneuse, l'os est déposé directement dans le tissu conjonctif primitif. Dans l'ossification endochondrale, celui étudié dans la recherche discutée ici, le cartilage agit comme un précurseur, et est progressivement dégradé et remplacé par de l'os.
Parce que cette recherche révèle deux façons d'induire l'éclatement des chondrocytes (qui à leur tour contrôlent la formation osseuse en faisant de la place pour les tissus minéralisés), en utilisant la pression mécanique et osmotique, il ouvre la voie à de nouvelles méthodes pour fabriquer du tissu osseux. Le dévoilement du rôle des fragments membranaires en tant que centres de nucléation pour la formation osseuse offre une nouvelle voie pour le développement de biomatériaux pour l'ingénierie et la régénération des tissus osseux. Les deux résultats ouvrent de nouvelles opportunités pour la bio-ingénierie du tissu osseux.