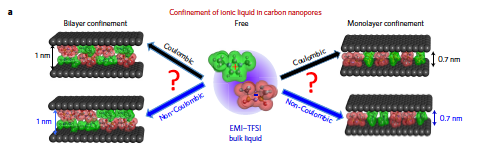
Lorsqu'il est emballé dans des canaux de pores aussi étroits qu'un nanomètre ou moins, les ions renonceront à leur ordre de charge alterné positif-négatif typique. Ils formeront une ligne simple (droite) ou double file (gauche), plusieurs fois en file d'attente à côté d'ions de la même charge. Crédit :Université Drexel
Il s'avère que lorsqu'ils sont pressés et que l'espace est limité, ions, comme les gens, trouvera un moyen de s'entasser, même si cela signifie défier les normes de la nature. Recherche récemment publiée par une équipe internationale de scientifiques, y compris Yury Gogotsi de l'Université Drexel, Doctorat, montre que les particules chargées renonceront en fait à leur comportement « d'attraction des contraires », appelé ordre coulombien, lorsqu'il est confiné dans les minuscules pores d'un nanomatériau. Cette découverte pourrait être un développement pivot pour le stockage de l'énergie, technologies de traitement de l'eau et de production d'énergie alternative, qui impliquent tous des ions s'entassant dans des matériaux nanoporeux.
Dans leur papier, qui vient d'être publié dans la revue Matériaux naturels , les chercheurs expliquent comment l'ordre coulombien dans les sels liquides commence à se décomposer lorsque les ions sont confinés dans de petits espaces, en particulier des pores de carbone de moins d'un nanomètre de diamètre. Et plus le pore est étroit, moins les ions adhèrent à l'ordre coulombien.
"C'est la première fois que la rupture de l'ordre coulombien dans les pores subnanométriques est démontrée de manière convaincante, " dit Gogotsi, un auteur de l'article, qui est la Distinguished University et professeur Bach au Drexel's College of Engineering. "La rupture des principes de symétrie, comme la commande coulombienne, joue un rôle essentiel dans la nature. Mais beaucoup de ces processus se produisent sans que nous les comprenions et connaissions leurs mécanismes. La science peut révéler ces processus cachés. Et si nous les comprenons, nous pouvons éventuellement développer une meilleure technologie en travaillant aux mêmes échelles nanométriques et subnanométriques que la nature. »
Pour faire sa découverte, l'équipe, y compris des chercheurs de l'Université de Shinshu au Japon ; Université de Loughborough au Royaume-Uni; L'Université d'Adélaïde en Australie; et Sorbonne Université, le Réseau français de recherche sur le stockage électrochimique de l'énergie, et l'Université Paul Sabatier en France, ont créé deux ensembles de nanomatériaux de carbone. L'un avait des pores d'au moins un nanomètre de diamètre et l'autre des pores de moins d'un nanomètre. Ils ont ensuite utilisé les matériaux pour aspirer un liquide ionique comme s'il s'agissait d'une éponge absorbant l'eau.
Dans les liquides ioniques, qui sont des sels liquides à température ambiante souvent utilisés comme solvants dans l'industrie chimique, les ions sont superposés en totale conformité avec le modèle alterné positif-négatif de l'ordre coulombien. Mais à mesure que le liquide ionique pénétrait dans les nanopores de carbone, il forçait les ions à s'aligner en lignes à une ou deux files. Et, comme un troupeau d'écoliers courant pour le bus, ils ne finissaient pas toujours en file à côté de leurs cohortes habituelles.
"Dans cet état, l'ordre coulombien du liquide est rompu, ", écrivent les auteurs. "Des ions de même charge sont voisins les uns des autres en raison d'un écran de leurs interactions électrostatiques par les charges d'image induites dans les parois des pores."
L'équipe a observé cette perturbation dans l'ordre naturel des ions par diffusion des rayons X et a modélisé le processus pour expliquer les observations expérimentales. Ils ont également signalé que l'ordre non coulombique devenait plus prononcé lorsqu'une charge électrique était appliquée au matériau carboné.
"Nos résultats suggèrent l'existence d'un mécanisme à l'échelle moléculaire qui réduit l'énergie de répulsion coulombienne entre les co-ions qui se rapprochent les uns des autres, " ont-ils écrit. Ce mécanisme, ils théorisent, est liée à la charge imposée temporairement sur les parois des pores de carbone. Cette "charge d'image, " ils écrivent, compense la répulsion électrostatique naturelle des ions de même charge, pour permettre aux canaux de se remplir d'ions de même charge alignés les uns à côté des autres.
Gogotsi suggère que cette découverte pourrait rendre plus faisable l'utilisation de liquides ioniques dans les batteries et autres dispositifs de stockage d'énergie, qui a été examinée comme une méthode pour rendre les batteries plus sûres, mais n'a pas encore fait son chemin car elle limite leurs performances.
"Nous pouvons obtenir des batteries et des supercondensateurs plus sûrs lors de l'utilisation d'électrolytes liquides ioniques car ils ne sont pas inflammables comme la solution d'électrolyte actuellement utilisée dans ces appareils, " dit Gogotsi. " Aussi, puisqu'il n'y a pas de solvant, tout le volume est occupé par des ions et nous pourrons peut-être stocker plus d'énergie que les électrolytes conventionnels qui utilisent des solvants organiques."
Il considère également cette découverte comme une découverte qui pourrait avoir un impact significatif sur la poussée de la technologie de dessalement de l'eau. Les membranes actuellement développées pour transformer l'eau salée en eau potable pourraient être améliorées grâce à cette connaissance du comportement des ions dans les pores subnanométriques.