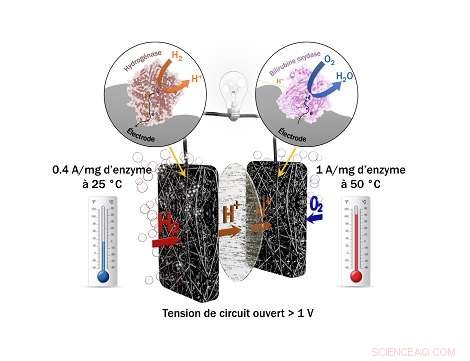
Biocellule utilisant du carburant H2/O2 à base d'une hydrogénase thermostable qui résiste à l'oxygène et au monoxyde de carbone à l'anode et une bilirubine oxydase thermostable à la cathode qui fournissent des courants de l'ordre de l'ampère par milligramme d'enzymes. Crédit :Ievgen Mazurenko, BIP
Fabriquer une biopile aussi efficace qu'une pile à combustible au platine :c'est l'exploit qu'ont réussi les chercheurs du Laboratoire de Bioénergétique et Ingénierie des Protéines (CNRS/Aix-Marseille Université), en collaboration avec le Centre de Recherche Paul Pascal (CNRS/Université de Bordeaux) et l'Institut Universitaire des Systèmes Thermiques Industriels (CNRS/Aix-Marseille Université). Trois ans après avoir réalisé leur premier prototype de biocellule, les chercheurs viennent de franchir une nouvelle étape et d'augmenter ses performances et sa stabilité. Cette biocellule pourrait, à long terme, offrir une alternative aux piles à combustible qui nécessitent des métaux rares et coûteux, comme le platine. Leurs travaux ont été publiés dans Sciences de l'énergie et de l'environnement le 17 août, 2017.
Une pile à combustible convertit l'énergie chimique en énergie électrique via la combustion d'hydrogène. Bien qu'elle soit considérée comme une technologie propre - car elle n'émet pas de gaz à effet de serre - les piles à combustible utilisent des catalyseurs de métaux rares coûteux, comme le platine, pour oxyder l'hydrogène et réduire l'oxygène. Dans les années récentes, l'identification de biocatalyseurs, des enzymes aux propriétés remarquables, a redynamisé la recherche dans ce domaine :leur oxygène, et surtout l'hydrogène, l'activité de transformation est comparable à celle du platine. L'activité hydrogénase était, jusque récemment, inhibée par l'oxygène et donc incompatible avec une utilisation en cellule.
Pour plusieurs années, des chercheurs du Laboratoire de Bioénergétique et Ingénierie des Protéines (CNRS/Aix-Marseille Université) ont développé une nouvelle génération de biocellules. Ils ont remplacé le catalyseur chimique (platine) par des enzymes bactériennes :à l'anode, l'hydrogénase (clé pour convertir l'hydrogène en de nombreux micro-organismes), et à la cathode, bilirubine oxydase. Ils ont maintenant identifié une hydrogénase active en présence d'oxygène et résistante à certains inhibiteurs du platine comme le monoxyde de carbone. En collaboration avec le Centre de Recherche Paul Pascal (CNRS/Université de Bordeaux), ils ont également exploré la biodiversité pour identifier des enzymes thermostables capables de résister à des températures comprises entre 25 °C et 80 °C.
Pour faire passer ces bioprocédés du laboratoire au développement industriel, deux obstacles majeurs ont dû être surmontés. En 2014, leur premier prototype était limité à la fois par la faible puissance qu'il générait et par le manque de stabilité enzymatique. Ils avaient donc besoin d'un changement d'échelle, devait pourtant conserver l'activité des enzymes et les protéger de tout inhibiteur. Un troisième problème majeur était de savoir comment réduire les coûts, donc entre autres, ils devaient minimiser la quantité d'enzyme utilisée. Toutes ces questions ont nécessité une étude fondamentale et pluridisciplinaire destinée à mettre en lumière les facteurs limitant la bioélectrocatalyse.
En incorporant progressivement les deux enzymes thermostables dans une architecture carbonée, les chercheurs ont résolu ces trois problèmes. Un feutre de carbone à porosité adaptée est la structure hôte des enzymes, et sert également de protection contre les espèces chimiques générées lorsque l'oxygène est réduit, qui modifient l'activité enzymatique. Ainsi, la cellule peut fonctionner sans perte de performances pendant plusieurs jours.
Grâce à cette architecture maîtrisée et aux propriétés intrinsèques des enzymes, les chercheurs sont parvenus pour la première fois à quantifier la proportion d'enzymes participant effectivement au courant, démontrant que les courants délivrés par le biocatalyseur sont très similaires aux résultats cibles pour le platine. Ils ont également développé un modèle numérique pour déterminer la géométrie optimale de la cellule. Ces biopiles apparaissent donc comme une alternative aux piles à combustible classiques :la biomasse peut être utilisée pour fournir à la fois le carburant (l'hydrogène) et le catalyseur (les enzymes), qui sont par nature, renouvelable.