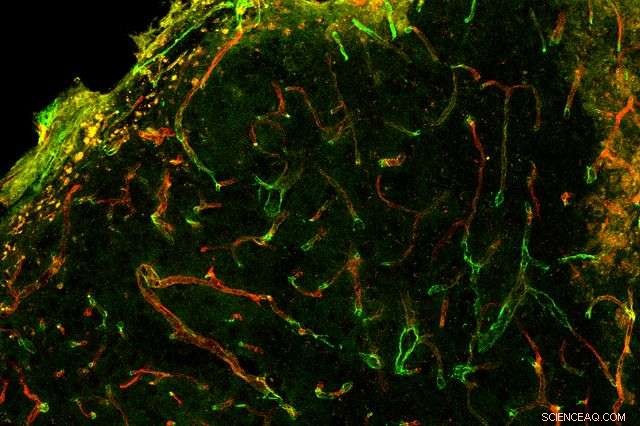
Une image au microscope améliorée par fluorescence montrant une croissance de vaisseaux sanguins d'apparence saine après un AVC, dans une souris. Crédit :UCLA
Une équipe de recherche dirigée par des ingénieurs et des médecins biomoléculaires de l'UCLA a démontré un matériau thérapeutique qui pourrait un jour favoriser une meilleure régénération des tissus après une plaie ou un accident vasculaire cérébral.
Pendant le processus de guérison typique du corps, lorsque des tissus comme la peau sont endommagés, le corps produit des cellules de remplacement. Les intégrines sont une classe de protéines qui sont importantes dans les processus cellulaires essentiels à la création de nouveaux tissus. L'un des processus est l'adhésion cellulaire, lorsque de nouvelles cellules "collent" aux matériaux entre les cellules, appelée matrice extracellulaire. Une autre est la migration cellulaire, où à la surface de la cellule, les intégrines aident à « tirer » la cellule à travers la matrice extracellulaire pour déplacer les cellules en place. Cependant, ces processus ne se produisent pas dans le tissu cérébral qui a été endommagé lors d'un accident vasculaire cérébral. C'est pourquoi les scientifiques tentent de développer des matériaux thérapeutiques qui pourraient favoriser cette forme de guérison.
Le matériau de type gel injectable, qui s'appelle un hydrogel, que les chercheurs de l'UCLA ont développé aide ce processus de réparation en formant un échafaudage à l'intérieur de la plaie qui agit comme une matrice extracellulaire artificielle, et le nouveau tissu se développe autour de cela.
L'utilisation d'un gel injectable n'est pas nouvelle, mais les échafaudages de gel précédents ont entraîné des vaisseaux sanguins faibles dans le tissu nouvellement formé. Les nouvelles découvertes, Publié dans Matériaux naturels , montrent que lorsque l'échafaudage contient une molécule spécifique de liaison à l'intégrine, les nouveaux vaisseaux sanguins qui se forment sont plus forts.
"L'échafaudage en gel injectable est un peu comme un treillis de jardin sur lequel les plantes poussent, " dit Tatiana Segura, professeur de génie chimique et biomoléculaire, bio-ingénierie et dermatologie, qui a dirigé la recherche. "En soi, c'est bien car les nouveaux tissus entrants ont quelque chose pour soutenir sa croissance. Ce nouveau matériau est similaire à un treillis avec un engrais très spécifique pour aider la plante à pousser sainement et fort."
Même en combinant des gels avec une protéine qui favorise la formation de vaisseaux sanguins, tels que le facteur de croissance endothélial vasculaire, connu sous le nom de VEGF, les vaisseaux sanguins dans le nouveau tissu à l'intérieur de l'échafaudage ont tendance à fuir et ont également tendance à s'agglomérer trop près les uns des autres.
Pour surmonter cela, les chercheurs ont examiné plus en détail comment les molécules de liaison aux intégrines interagissaient avec le gel et comment ces molécules influençaient la croissance des vaisseaux sanguins.
Ils ont testé deux types d'échafaudages avec différentes molécules de liaison aux intégrines. Les deux échafaudages contenaient également la protéine VEGF. Ils ont découvert que l'un des échafaudages - qui se liait à l'intégrine connue sous le nom de "α3/α5β1" - fonctionnait très bien. Il a dirigé une meilleure qualité de réparation et de régénération des vaisseaux sanguins. En outre, ils ont découvert que les échafaudages de liaison α3/α5β1 guidaient également la forme du vaisseau sanguin, un processus appelé signalisation morphogénique.
L'autre échafaudage de liaison aux intégrines qu'ils ont testé présentait toujours des problèmes de fuites et d'agglutination des vaisseaux sanguins.
"Au-delà du support structurel pour les nouveaux tissus et vaisseaux sanguins, l'ajout de molécules spécifiques de liaison à l'intégrine pour α3/α5β1, dit aux tissus environnants de développer des vaisseaux sanguins forts et bien définis par opposition aux autres que nous avons testés, où les nouveaux vaisseaux sanguins avaient tendance à fuir et à s'agglomérer trop près les uns des autres, " dit Segura.
L'auteur principal de la recherche était Shuoran Li, un doctorat UCLA 2017 qui a été conseillé par Segura. Les collaborateurs comprennent également le Dr Thomas Carmichael, neurologue et neuroscientifique à la David Geffen School of Medicine de l'UCLA et Thomas Barker, professeur de génie biomédical à l'Université de Virginie.
Dans ce travail récent, les chercheurs ont démontré que la liaison à l'intégrine peut dicter la structure des vaisseaux sanguins in vitro avec l'échafaudage de liaison α3/α5β1 résultant en des réseaux étendus qui se connectent aux branches des vaisseaux sanguins existants. Ensuite, les chercheurs ont utilisé les mêmes échafaudages α3/α5β1 chez la souris et ont vu se former des vaisseaux sanguins qui fuyaient moins après un AVC.
L'étape suivante, les chercheurs ont dit, utiliserait des molécules se liant à l'intégrine avec d'autres technologies d'hydrogel qui se sont révélées prometteuses pour la récupération fonctionnelle à long terme après un AVC, mais dans lequel les vaisseaux sanguins nouvellement développés n'étaient pas robustes.
"Actuellement, il n'y a pas de thérapie qui favorise la réparation et la récupération du cerveau après un AVC, " a déclaré Carmichael. " Toutes les thérapies de l'AVC se concentrent sur le blocage initial des vaisseaux sanguins du cerveau qui conduisent à l'AVC. Cela signifie que l'AVC est la cause la plus fréquente d'invalidité chez l'adulte. Cette recherche est passionnante car elle montre un moyen viable de transformer les tissus morts et cicatriciels lors d'un AVC en faisant pousser de nouveaux vaisseaux sanguins bien formés dans la zone de l'AVC."
Segura et ses collaborateurs ont travaillé sur des biomatériaux pour la réparation tissulaire, notamment, un gel injectable (distinct de cette recherche actuelle) et plus récemment, des travaux qui ont montré que le gel pouvait réduire l'inflammation et favoriser la migration des cellules progénitrices neurales vers le site de l'AVC.