
Les chimistes du Brookhaven Lab, Ping Liu et José Rodriguez, ont aidé à caractériser les détails structurels et mécaniques d'un nouveau catalyseur à basse température pour la production d'hydrogène gazeux de haute pureté à partir d'eau et de monoxyde de carbone. Crédit :Laboratoire national de Brookhaven
Les scientifiques ont développé un nouveau catalyseur à basse température pour produire de l'hydrogène gazeux de haute pureté tout en utilisant simultanément du monoxyde de carbone (CO). La découverte décrite dans un article à publier en ligne dans la revue Science jeudi, 22 juin 2017-pourrait améliorer les performances des piles à combustible fonctionnant à l'hydrogène mais pouvant être empoisonnées par le CO.
"Ce catalyseur produit une forme plus pure d'hydrogène pour alimenter la pile à combustible, " a déclaré José Rodriguez, chimiste au laboratoire national de Brookhaven du département de l'Énergie des États-Unis (DOE). Rodriguez et ses collègues de la division de chimie de Brookhaven - Ping Liu et Wenqian Xu - faisaient partie de l'équipe de scientifiques qui ont aidé à caractériser les détails structurels et mécaniques du catalyseur, qui a été synthétisé et testé par des collaborateurs de l'Université de Pékin dans le cadre d'un effort dirigé par le professeur de chimie Ding Ma.
Parce que le catalyseur fonctionne à basse température et basse pression pour convertir l'eau (H2O) et le monoxyde de carbone (CO) en hydrogène gazeux (H2) et en dioxyde de carbone (CO2), cela pourrait également réduire le coût de fonctionnement de cette réaction dite de "transfert eau-gaz".
"Avec basse température et pression, la consommation d'énergie sera moindre et le montage expérimental sera moins coûteux et plus facile à utiliser dans les petites installations, comme les piles à combustible pour les voitures, ", a déclaré Rodriguez.
La connexion or-carbure
Le catalyseur est constitué d'amas de nanoparticules d'or en couches sur un substrat de carbure de molybdène. Cette combinaison chimique est assez différente des catalyseurs à base d'oxydes utilisés pour alimenter la réaction de conversion eau-gaz dans les installations industrielles de production d'hydrogène à grande échelle.
"Les carbures sont chimiquement plus réactifs que les oxydes, " dit Rodriguez, "et l'interface or-carbure a de bonnes propriétés pour la réaction de changement de gaz d'eau; elle interagit mieux avec l'eau que les métaux purs."
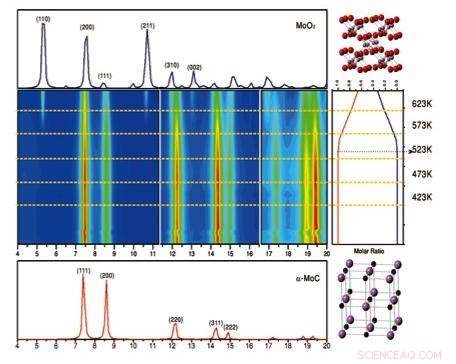
Wenqian Xu et José Rodriguez de Brookhaven Lab et Siyu Yao, puis étudiant à l'Université de Pékin mais maintenant chercheur postdoctoral à Brookhaven, a mené des études de diffraction des rayons X operando du catalyseur or-molybdène-carbure sur une plage de températures (423 Kelvin à 623K) à la National Synchrotron Light Source (NSLS) à Brookhaven Lab. L'étude a révélé qu'à des températures supérieures à 500K, le carbure de molybdène se transforme en oxyde de molybdène, avec une diminution de l'activité catalytique. Crédit :Laboratoire national de Brookhaven
"Le groupe de l'Université de Pékin a découvert une nouvelle méthode de synthèse, et c'était une vraie percée, " Rodriguez a déclaré. "Ils ont trouvé un moyen d'obtenir une phase spécifique ou une configuration des atomes qui est très active pour cette réaction."
Les scientifiques de Brookhaven ont joué un rôle clé dans le décryptage des raisons de la forte activité catalytique de cette configuration. Rodriguez, Wenqian Xu, et Siyu Yao (alors étudiant à l'Université de Pékin mais maintenant chercheur postdoctoral à Brookhaven) ont mené des études structurelles utilisant la diffraction des rayons X à la National Synchrotron Light Source (NSLS) alors que le catalyseur fonctionnait dans des conditions industrielles ou techniques. Ces expériences operando ont révélé des détails cruciaux sur la façon dont la structure a changé dans différentes conditions de fonctionnement, y compris à différentes températures.
Avec ces détails structurels en main, Zhijun Zuo, professeur invité à Brookhaven de l'Université de technologie de Taiyuan, Chine, et le chimiste de Brookhaven Ping Liu ont aidé à développer des modèles et un cadre théorique pour expliquer pourquoi le catalyseur fonctionne comme il le fait, en utilisant les ressources informatiques du Centre pour les nanomatériaux fonctionnels (CFN) de Brookhaven.
"Nous avons modélisé différentes interfaces d'or et de carbure de molybdène et étudié le mécanisme de réaction pour identifier exactement où les réactions ont lieu - les sites actifs où les atomes se lient, et comment les liens se brisent et se reforment, " elle a dit.
Études supplémentaires au Centre des sciences des matériaux en nanophase du Laboratoire national d'Oak Ridge (CNMS), la source lumineuse avancée (ALS) du Lawrence Berkeley National Laboratory, et deux installations de recherche synchrotron en Chine ont contribué à la compréhension des scientifiques.
"Il s'agit d'une réaction complexe en plusieurs parties, " dit Liu, mais elle a noté un facteur essentiel :"L'interaction entre l'or et le substrat de carbure est très importante. L'or lie généralement les choses très faiblement. Avec cette méthode de synthèse, nous obtenons une adhérence plus forte de l'or au carbure de molybdène de manière contrôlée."
Cette configuration stabilise l'intermédiaire clé qui se forme au cours de la réaction, et la stabilité de cet intermédiaire détermine le taux de production d'hydrogène, elle a dit.
L'équipe de Brookhaven continuera d'étudier ce catalyseur et d'autres catalyseurs au carbure avec de nouvelles capacités à la National Synchrotron Light Source II (NSLS-II), une nouvelle installation qui a ouvert ses portes au Brookhaven Lab en 2014, remplacer le NSLS et produire des radiographies au nombre de 10, 000 fois plus lumineux. Avec ces rayons X plus brillants, les scientifiques espèrent capturer plus de détails sur la chimie en action, y compris les détails des intermédiaires qui se forment tout au long du processus de réaction pour valider les prédictions théoriques faites dans cette étude.