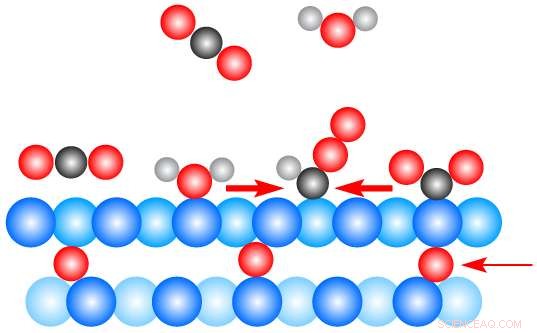
Dans cette illustration à l'échelle atomique, des traces d'oxygène (rouge) juste sous une surface de cuivre (bleue), jouent un rôle clé dans la conduite d'une réaction catalytique dans laquelle le dioxyde de carbone (molécules noires et rouges) et l'eau (molécules rouges et blanches) interagissent au début de la formation d'éthanol. Les molécules de dioxyde de carbone planent à la surface du cuivre, puis se plient pour accepter les atomes d'hydrogène des molécules d'eau. Des expériences de rayons X à la source lumineuse avancée du Berkeley Lab ont aidé les chercheurs à comprendre le rôle de l'oxygène souterrain dans ce processus. Crédit :Berkeley Lab
Tout en utilisant les rayons X pour étudier les premières étapes d'un processus chimique qui peut reformuler le dioxyde de carbone en composés plus utiles, y compris les combustibles liquides, les chercheurs ont été surpris lorsque l'expérience leur a appris quelque chose de nouveau sur les causes de cette réaction.
Une technique aux rayons X au Lawrence Berkeley National Laboratory (Berkeley Lab) du ministère de l'Énergie, couplé aux travaux théoriques d'une équipe du California Institute of Technology, Pasadena (Caltech), a révélé comment les atomes d'oxygène incrustés très près de la surface d'un échantillon de cuivre avaient un effet plus dramatique sur les premiers stades de la réaction avec le dioxyde de carbone que les théories antérieures ne pouvaient en rendre compte.
Ces informations pourraient s'avérer utiles dans la conception de nouveaux types de matériaux pour améliorer davantage les réactions et les rendre plus efficaces dans la conversion du dioxyde de carbone en d'autres produits. De fortes concentrations de dioxyde de carbone sont nocives pour la santé et l'environnement, les chercheurs ont donc cherché des moyens de le retirer de l'atmosphère et de le stocker en toute sécurité ou de le convertir chimiquement en des formes plus bénéfiques.
Pour expliquer ce qui se passait, l'équipe de recherche a développé des modèles informatiques, et révisé les théories existantes pour expliquer ce dont ils étaient témoins dans les expériences. Leurs résultats ont été publiés en ligne le 12 juin dans le Actes de l'Académie nationale des sciences journal.
Le cuivre est un catalyseur commun - un matériau utilisé pour activer et accélérer les réactions chimiques - et, bien qu'il ne soit pas efficace, il aide à la production d'éthanol lorsqu'il est exposé au dioxyde de carbone et à l'eau. Dans la réaction étudiée, le cuivre aide à décomposer chimiquement et à réassembler les molécules de dioxyde de carbone et d'eau en d'autres molécules.
"Nous avons trouvé plus que ce que nous pensions que nous allions trouver à partir de cette enquête fondamentale, " a déclaré Ethan Crumlin, un scientifique de l'Advanced Light Source (ALS) de Berkeley Lab qui a co-dirigé l'étude avec les chercheurs du Joint Center for Artificial Photosynthèse (JCAP) Junko Yano, au laboratoire de Berkeley, et Guillaume Goddard III, chez Caltech.
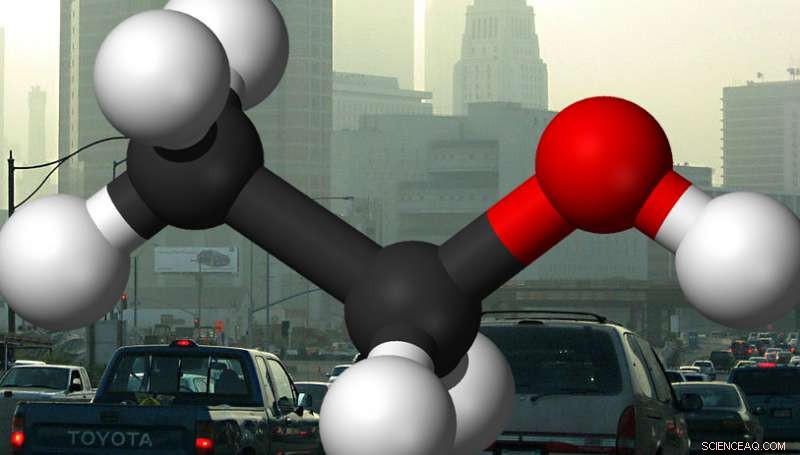
Les scientifiques cherchent des moyens de réduire les niveaux nocifs pour l'environnement de dioxyde de carbone provenant des émissions des véhicules et d'autres sources en améliorant les processus chimiques qui convertissent le dioxyde de carbone gazeux en éthanol (structure moléculaire illustrée ici) pour une utilisation dans les carburants liquides, par exemple. Les expériences aux rayons X au Berkeley Lab ont aidé à montrer ce qui est à l'œuvre dans les premiers stades des réactions chimiques qui convertissent le dioxyde de carbone et l'eau en éthanol. Crédit :Image composite/Wikimedia Commons
L'ALS est une installation de recherche en rayons X connue sous le nom de synchrotron qui possède des dizaines de lignes de faisceaux expérimentales pour explorer un large éventail de propriétés microscopiques de la matière, et JCAP se concentre sur la façon de convertir le dioxyde de carbone, l'eau, et la lumière du soleil en carburants renouvelables.
"Le fait d'avoir des atomes d'oxygène juste sous la surface - une couche de sous-oxyde - est un aspect critique pour cela, " a déclaré Crumlin. Le travail aux rayons X a apporté une nouvelle clarté dans la détermination de la bonne quantité de cet oxygène souterrain - et son rôle dans les interactions avec le dioxyde de carbone et l'eau - pour améliorer la réaction.
"Comprenant cette couche de sous-oxyde, et le sous-oxyde au contact de l'eau, fait partie intégrante de la façon dont l'eau interagit avec le dioxyde de carbone" dans ce type de réaction, il ajouta.
Goddard et ses collègues de Caltech ont travaillé en étroite collaboration avec les chercheurs du Berkeley Lab pour développer et affiner une théorie de la mécanique quantique qui correspond aux observations aux rayons X et explique la structure électronique des molécules dans la réaction.
"C'était une bonne boucle, processus itératif, " dit Crumlin. " Le simple fait d'être curieux et de ne pas se contenter d'une réponse simple a payé. Tout a commencé à se rassembler comme une histoire cohérente."
Goddard a dit, "Ce va-et-vient entre la théorie et l'expérimentation est un aspect passionnant de la recherche moderne et une partie importante de la stratégie du JCAP pour fabriquer des carburants à partir de dioxyde de carbone." L'équipe de Caltech a utilisé des ordinateurs pour aider à comprendre comment les électrons et les atomes se réorganisent dans la réaction.

Cette image de microscopie électronique à balayage en fausses couleurs montre des détails microscopiques à la surface d'une feuille de cuivre qui a été utilisée comme catalyseur dans une réaction chimique étudiée à la source lumineuse avancée de Berkeley Lab. La barre d'échelle représente 50 microns, ou des millionièmes de mètre. Crédit :Berkeley Lab
À l'ALS de Berkeley Lab, les chercheurs ont fait appel à une technique aux rayons X connue sous le nom d'APXPS (spectroscopie photoélectronique à rayons X à pression ambiante lorsqu'ils ont exposé une fine feuille de cuivre spécialement traité - connu sous le nom de Cu (111) - au dioxyde de carbone gazeux et ajouté de l'eau à température ambiante.
Au cours des expériences, ils ont légèrement chauffé l'échantillon dans de l'oxygène pour faire varier la concentration d'oxygène incorporé dans la feuille, et utilisé des rayons X pour sonder les premières étapes de la réaction synergique du dioxyde de carbone et de l'eau avec différentes quantités d'oxyde de subsurface à la surface du cuivre.
Les études aux rayons X, planifié et interprété par Marco Favaro, l'auteur principal de l'étude, a révélé comment les molécules de dioxyde de carbone entrent en collision avec la surface du cuivre, puis survolez-le dans un état faiblement lié. Les interactions avec les molécules d'eau servent à plier les molécules de dioxyde de carbone de manière à leur permettre d'éliminer les atomes d'hydrogène des molécules d'eau. Ce processus finit par former de l'éthanol, un type de carburant liquide.
"La quantité modeste d'oxygène sous la surface aide à générer un mélange de cuivre métallique et chargé qui peut faciliter l'interaction avec le dioxyde de carbone et favoriser d'autres réactions en présence d'eau, " a déclaré Crumlin.
Le cuivre a quelques défauts en tant que catalyseur, Yano a noté, et il est actuellement difficile de contrôler le produit final qu'un catalyseur donné va générer.
« Si nous savons ce que fait la surface, et quel est le modèle de cette interaction chimique, alors il y a un moyen d'imiter cela et de l'améliorer, ", a déclaré Yano. Les travaux en cours peuvent également aider à prédire la sortie finale d'un catalyseur donné dans une réaction. "Nous savons que le cuivre fonctionne - qu'en est-il des différentes surfaces de cuivre, alliages de cuivre, ou différents types de métaux et alliages ?"