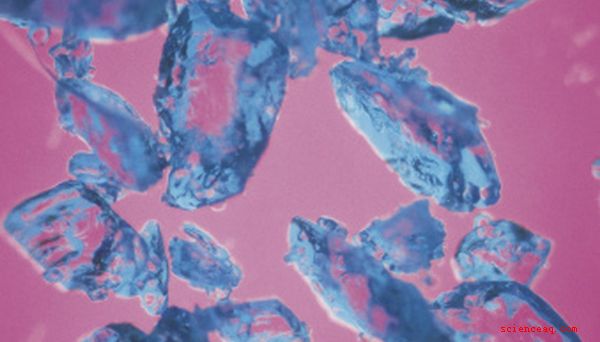
Comme de nombreux complexes de métaux de transition, le sulfate de cuivre (II) pentahydraté est de couleur vive; les cristaux de cette belle substance sont d'un bleu pâle. Sa couleur provient de la chimie et de la physique de sa composition - ou, plus précisément, du type de liaisons qu'il forme avec les ions sulfates et les molécules d'eau attachées au cuivre.
Orbitales
Les électrons présentent des ondes - la dualité des particules, ce qui signifie qu'elles ont à la fois des propriétés ondulatoires et des propriétés particulaires. Le comportement d'un électron dans un atome est décrit par une équation ondulatoire appelée fonction d'onde. Le carré de la fonction d'onde donne la probabilité que l'électron soit trouvé à n'importe quel point particulier à un moment donné. Les fonctions d'onde des électrons dans les atomes sont également appelées orbitales atomiques. Les chimistes nomment les orbitales atomiques en utilisant un nombre pour désigner le niveau d'énergie de l'orbitale suivi d'une lettre pour désigner le type d'orbitale. Pour les éléments de la quatrième période du tableau périodique ou ci-dessus, il vous suffit de vous concentrer sur trois types d'orbitales, à savoir s, p et d. Pour avoir une idée de la forme de ces orbitales, consultez le lien dans la section des ressources.
Fractionnement du champ cristallin
L'ion cuivre dans le sulfate de cuivre (II) a perdu deux électrons, il a donc un + 2 charge. Il a neuf électrons dans son niveau d'énergie ou enveloppe la plus externe; ces soi-disant électrons de valence occupent tous des orbitales 3D. Les molécules d'eau et les ions sulfate sont attirés par la charge positive de l'ion cuivre, ils s'en approchent donc et s'organisent autour de lui en configuration octaédrique. Par conséquent, deux des cinq orbitales 3d de l'ion cuivre s'alignent le long des axes par lesquels les ions sulfate et les molécules d'eau se rapprochent; puisque les électrons dans ces orbitales et les électrons dans les molécules /ions ont tous deux une charge négative, ils se repoussent. En fin de compte, alors, deux des cinq orbitales 3d ont augmenté l'énergie; on les appelle par exemple les orbitales. Les trois autres, en revanche, ont une énergie diminuée et sont appelés les orbitales t2g.
Absorption de la lumière
Un photon de lumière sera absorbé par le complexe de coordination s'il a une énergie équivalente à la différence entre l'état qu'un électron occupe maintenant et l'énergie d'un autre état à sa disposition. Par conséquent, le complexe de sulfate de cuivre peut absorber des photons de lumière avec des énergies équivalentes à la différence d'énergie entre le t2g et par exemple les orbitales. En l'occurrence, la différence d'énergie pour le complexe de sulfate de cuivre est équivalente à la différence d'énergie pour les photons de lumière dans la région rouge-orange du spectre. La lumière rougeâtre étant absorbée pendant la transmission de la lumière bleue, le sulfate de cuivre apparaît bleu.
Dissolution dans l'eau
Lorsque le sulfate de cuivre se dissout dans l'eau, les ions cuivre et sulfate se dissocient. Maintenant, l'ion cuivre forme un complexe octaédrique où il est entouré de six molécules d'eau. L'effet est toujours très similaire, cependant, car la séparation entre les orbitales t2g et par exemple les orbitales dans ce nouveau complexe est toujours telle que la lumière orange rougeâtre est absorbée et vous voyez une solution de couleur bleue.